El cáncer primario de cerebro se refiere a los tumores malignos que se forman en el cerebro o en los nervios cerebrales.1 La propagación del cáncer de cerebro (hace metástasis) fuera del sistema nervioso central no ocurre con frecuencia. El sistema nervioso central es la parte del sistema nervioso que incluye al cerebro y a la médula espinal.2, 3, 4 El cáncer cerebral primario representa el 2% al 3% de todos los casos nuevos de cáncer en los adultos y es la segunda forma más común de cáncer infantil (después de la leucemia). El cáncer cerebral es la principal causa de muerte por cáncer en niños entre 1 a 19 años de edad y también fue la causa del 40% de las muertes por cáncer en adultos entre el 2012 y el 2016. 5, 6
El cáncer secundario del cerebro se refiere a los tumores malignos que se desarrollaron en otra parte del cuerpo y se movilizaron (metástasis) al cerebro. Por ejemplo, la metástasis del cáncer de mama o de pulmón al cerebro es algo común. El cáncer de cerebro secundario es más frecuente que el cáncer cerebral primario. 7, 1
La incidencia del cáncer cerebral es más alta en los países más desarrollados que en los países menos desarrollados.8, 9 La sociedad americana de cáncer estima que en el 2021 se diagnosticarán a 24 530 individuos con cáncer cerebral o de la médula espinal y que 18 600 individuos fallecerán a causa de estas mismas enfermedades en los Estados Unidos. 9
Visite las siguientes secciones para obtener más información sobre el cáncer de cerebro:
- Anatomía y función del cerebro
- Tipos
- Factores de riesgo
- Síntomas y detección
- Etapas y patología
- Biología tumoral
- Tratamientos
- Fuentes de información
- Resumen
Anatomía y función del cerebro
El cerebro y la médula espinal componen al sistema nervioso central. El cerebro es un órgano extremadamente complejo que tiene más de un billón de neuronas que nos brindan la capacidad de comprender, razonar y recordar. Ya que las regiones del cerebro se mantienen activas al mismo tiempo, es difícil vincular a una sola región con una sola actividad cerebral.
Las 3 partes principales del cerebro son el prosencéfalo, el cerebelo y el tronco encefálico. El prosencéfalo contiene el cerebro y el diencéfalo. El cerebro se separa en el hemisferio izquierdo y derecho y es la parte más frontal del órgano. Dentro del diencéfalo se encuentran el tálamo y el hipotálamo; estas regiones son responsables de controlar las emociones, el dolor, la temperatura corporal y el estrés. El siguiente gráfico detalla esta información con más claridad. El cerebro y la médula espinal están protegidos por varias capas de tejido de membranas conectivas que se conocen colectivamente como meninges.10, 11 El sistema nervioso central también está protegido por el líquido cerebroespinal, un líquido transparente que proviene de los ventrículos (cuatro estructuras huecas). El líquido cerebroespinal ayuda a absorber los impactos o golpes en la cabeza y es responsable de regular y mantener el entorno químico adecuado necesario para la función óptima del sistema nervioso central. 12
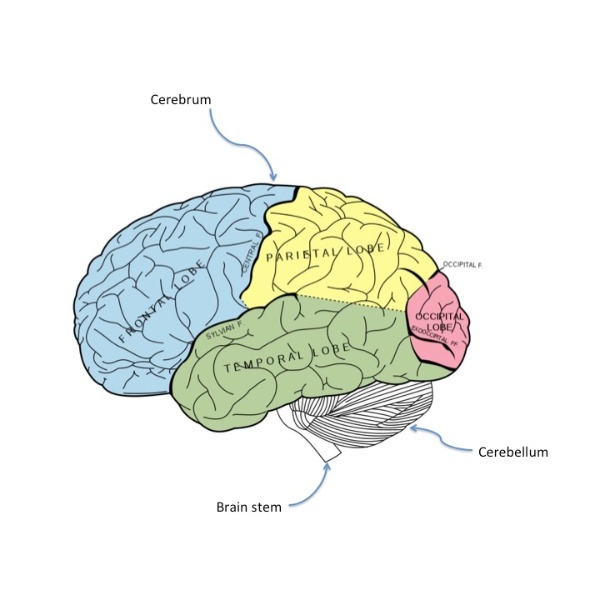
Vista lateral de las cisuras (aperturas) y lóbulos principales del cerebro. Figura 728 de Gray's Anatomy.13
Funciones de las regiones del cerebro:
- Prosencéfalo: el prosencéfalo está constituido por el cerebro y el diencéfalo y es la parte que se encarga de la percepción, el aprendizaje, la memoria, la coordinación del músculo esquelético, la consciencia, la regulación de los comportamientos (por ejemplo, comer y beber), el control de la temperatura corporal y la generación de emociones.
- Cerebelo: el cerebelo es la región responsable de regular la coordinación del movimiento y el control de la postura y el equilibrio. 12
- Tronco cerebral: el tronco encefálico está formado por el mesencéfalo, el puente troncoencefálico y el bulbo raquídeo.12 Esta región transmite información entre la médula espinal, el prosencéfalo y el cerebelo, y tiene varias funciones importantes propias. El tronco encefálico controla el movimiento, la respiración, las funciones cardíacas y la regulación del sueño y la conciencia.10, 11
Células cerebrales
Como todos los demás órganos, el cerebro también está compuesto por distintos tipos de células. Las células que tienen mayor prevalencia de cáncer de cerebro son:
- Células nerviosas (neuronas): las neuronas son responsables de transmitir señales del cerebro a la médula espinal y al cuerpo, y estas células también son responsables de llevar señales del resto del cuerpo al cerebro.
- Células gliales: las células gliales apoyan a las neuronas aislándolas, alimentándolas y proporcionándoles soporte estructural. Estas células también son responsables de deshacerse de las neuronas muertas. Hay varios tipos diferentes de células gliales, cada una con su propia función. Los tipos de células gliales incluyen astrocitos, oligodendrocitos y células ependimarias.
Tipos
Hay más de 100 tipos de cáncer que pueden afectar el sistema nervioso central (CNS).14 Para reiterar, los cánceres que emergen en otros lugares (mama, pulmón, etc.) y se propagan hacia (hacen metástasis) el cerebro no son cánceres cerebrales primarios, y por ende, su nombre aún corresponde con el nombre de su sitio de origen. La siguiente sección solamente detallará a los cánceres cerebrales primarios (aquellos que se originan en el cerebro).
Gliomas
Los gliomas malignos son el tipo cáncer cerebral más común y mortal y se desarrollan en las células gliales del sistema nervioso central. Los gliomas se clasifican en 3 categorías: astrocitomas, oligodendrogliomas y ependimomas.15 La tasa de supervivencia de los pacientes con glioma ha mejorado en los últimos años, sin embargo, no ha logrado pasar de los 15 meses, pues pocos pacientes logran vivir más de dos años.16 Las investigaciones indican que este tipo de cáncer de cerebro puede resistir el tratamiento ya que los tumores tienen células madre que impulsan el crecimiento de vasos sanguíneos (angiogénesis), la propagación del tumor (metástasis) y la resistencia a los tratamientos.17, 18
- Astrocitomas: los astrocitomas son tumores que se desarrollan en los astrocitos y se encuentran en el cerebro y el cerebelo. Los astrocitomas constituyen aproximadamente el 50% de todos los tumores cerebrales primarios. El glioblastoma multiforme, un subtipo de astrocitoma, es la forma más agresiva del cáncer cerebral y su recuperación es bastante difícil.19
- Oligodendrogliomas: los oligodendrogliomas son tumores que se desarrollan en los oligodendrocitos; estas células abundan en ambos hemisferios del cerebro y son un tipo de célula glial que construye la mielina, una parte del cerebro que aumenta la velocidad del potencial de acción . Los oligodendrogliomas constituyen aproximadamente el 4% de los tumores cerebrales primarios. Aproximadamente el 55% de todos los casos de oligodendrogliomas aparecen en personas de entre 40 y 64 años de edad.20, 21
- Ependimomas: los ependimomas son tumores que se desarrollan en las células del epéndimo que producen y almacenan el líquido cerebroespinal. Los ependimomas representan solamente del 2% al 3% de todos los tumores cerebrales primarios, pero representan del 8% al 10% de los tumores cerebrales en niños. Los tumores del ependimoma generalmente se encuentran en los revestimientos de los ventrículos, la médula espinal o las regiones cercanas al cerebelo. 22
Otros tipos
Los meningiomas y los meduloblastomas son los tipos más comunes del cáncer cerebral que no se desarrollan en las células gliales. Por otro lado, los adenomas medulopituitarios, los linfomas primarios del sistema nervioso central y los tumores de las células germinales del sistema nervioso central.
- Meningiomas: los meningiomas son tumores que se desarrollan en las meninges, las membranas que cubren el cerebro y la médula espinal. Los tumores del meningioma suelen emerger de las células de la aracnoides que absorben el líquido cerebroespinal. Los tumores del meningioma representan del 13% al 30% de todos los tumores que se desarrollan dentro del cráneo. Los tumores que surgen dentro del cráneo se denominan tumores intracraneales. La mayoría de los meningiomas son benignos. Los meningiomas malignos son extremadamente raros, pues tienen una de incidencia de aproximadamente dos de cada millón de personas por año. El riesgo de desarrollar un meningioma aumenta con la edad y es más frecuente en las mujeres.23, 24
- Meduloblastomas: los meduloblastomas son las neoplasias malignas cerebrales más comunes en los niños. Estos cánceres crecen en la fosa posterior, una región específica del espacio dentro del cráneo (cavidad intracraneal) que contiene el tronco del encéfalo y el cerebelo. La región del cuarto ventrículo está involucrada en el desarrollo de aproximadamente el 80% de los casos infantiles.25, 26
Riesgos
Desafortunadamente, los expertos aún no logran nombrar a todos los factores que aumentan el riesgo de desarrollar la mayoría de los tipos de cáncer cerebral. Sin embargo, se han descrito algunos factores de riesgo (y factores de riesgo potenciales), como por ejemplo:
- Edad: el riesgo de la mayoría de los cánceres aumenta con la edad. Sin embargo, el neuroblastoma es una excepción, pues ocurre con mayor frecuencia en niños pequeños.
- Historial familiar: Existen varios trastornos genéticos que se presumen ser factores de riesgo para el cáncer de cerebro, como por ejemplo:
a. Neurofibromastosis tipo 1: una enfermedad caracterizada por cambios en el color de la piel y el crecimiento de tumores pequeños en la piel, el cerebro y en otras partes del cuerpo. Las personas que padecen de la neurofibromatosis tipo 1 están expuestas a un mayor riesgo de desarrollar neurilemomas, meningiomas, neurofibromas y otros tipos de gliomas. Los adultos que sufren de esta enfermedad suelen tener tumores cancerígenos que crecen a lo largo de los nervios.27
b. Neurofibromatosis tipo 2: esta condición es menos común que la neurofibromatosis tipo 1. Las mutaciones que se presentan en el gen NF2 están vinculadas a esta enfermedad. En aproximadamente 50% de todos los casos de neurofibromatosis tipo 2, la mutación del gen NF2 se hereda de los padres; esta enfermedad puede asociarse con neuromas acústicos, meingiomas y ependimomas de la médula espinal. Por lo general, los síntomas de esta enfermedad aparecen durante la adolescencia o pasados los veinte años de edad (18-24 años). Algunos síntomas incluyen disfunción del equilibrio y pérdida auditiva.28
c. Esclerosis tuberosa: un trastorno genético hereditario que causa el crecimiento de tumores en la piel, el cerebro/sistema nervioso, los riñones y el corazón. Los tumores de esta enfermedad suelen ser benignos (no cancerígenos), pero siempre existe la posibilidad de que se conviertan en masas cancerígenas. La mayoría de los casos de esclerosis tuberosa provienen de mutaciones aleatorias en los genes TSC1 y TSC2. No se ha determinado ningún factor de riesgo de esta enfermedad con certeza además de tener un historial familiar con la enfermedad. Sin embargo, la mayoría de los pacientes no tienen antecedentes familiares con la esclerosis tuberosa. 29
d. Síndrome de Von Hippel-Lindau (VHL): esta condición está asociada con el desarrollo de tumores benignos y malignos en varias partes del cuerpo. El gen VHL es un gen de supresión de tumores y las mutaciones es él son las responsables de provocar este síndrome. Estos cambios genéticos producen variaciones anormales de las proteínas VHL que no logran regular la supervivencia y la proliferación celular de manera adecuada. 30
e. Síndrome de Li-Fraumeni: esta condición no es muy común y está asociada con un mayor riesgo de desarrollar gliomas y otros tipos de cáncer. Varios estudios demuestran que el gen CHEK2 y el gen TP53 están vinculados al síndrome de Li-Fraumeni. Alrededor de la mitad de las familias con síndrome de Li-Fraumeni han heredado mutaciones en el gen TP53. 31
3. Infecciones: se ha observado que los virus, como los retrovirus, los papovirus y los adenovirus, pueden causar el crecimiento de tumores cerebrales en algunos animales, sin embargo pocos estudios han indicado la existencia de vínculos entre las infecciones virales y el cáncer cerebral humano. No obstante, los virus aún no se han descartado como un posible factor de riesgo y por lo cual se lo sigue investigando.32
4. Lesiones en la cabeza y traumas: Varias investigaciones actuales se enfocan en la posible relación entre los traumatismos craneoencefálicos y los meningiomas. Estos estudios revelan que muchos niños que han sido diagnosticados con tumores cerebrales sufrieron lesiones en la cabeza o traumatismos craneales durante el parto. 32
5. Vitaminas: Algunos estudios indican una posible relación entre el consumo de compuestos N-nitroso durante el embarazo y un riesgo elevado del desarrollo de tumores cerebrales en los hijos. 32, 33, 34
Síntomas y detección
Los síntomas del tumor cerebral dependen del tamaño, la ubicación, el tipo del tumor y si el tumor ha invadido otras áreas del cuerpo y la magnitud de esta invasión. El síntoma más común es el dolor de cabeza, pues presenta en el 35% de los pacientes y suele venir acompañado por náuseas, vómitos o complicaciones con algunas funciones nerviosas, denominadas déficits neurológicos focales. Los dolores de cabeza pueden ser una señal de advertencia, especialmente para aquellos pacientes que normalmente no los tienen. Los problemas localizados (focales) varían según la ubicación del tumor. También es importante informar al médico del paciente si los dolores de cabeza se vuelven cada vez más frecuentes o intensos.35
Existen diferentes pruebas médicas que pueden ser utilizadas para detectar o descartar un tumor cerebral.
- Examen neurológico: el examen neurológico se refiere a un conjunto preliminar de pruebas que se realizan a un paciente para recopilar información acerca de su estado mental, del sistema sensorial, nervioso y sus funciones motoras. Según los resultados del examen neurológico, el médico determina si se necesitan realizar pruebas adicionales.35 Obtenga más información acerca de los exámenes neurológicos.
- Angiografía cerebral: un procedimiento que se realiza para visualizar el flujo de la sangre en los vasos sanguíneos del cerebro del paciente. Este procedimiento detecta la presencia de coágulos en la sangre u otros problemas que se presentan los vasos sanguíneos del cerebro, como las aneurismas, las obstrucciones arteriales y la vasculitis. Este procedimiento también puede confirmar la presencia de un tumor cerebral.
- Cómo funciona: La angiografía cerebral generalmente se realiza en el hospital o en un centro de radiología. Es posible que se le indique al paciente que no consuma alimentos sólidos o líquidos durante un cierto período de tiempo antes de la prueba. Para el procedimiento, el paciente permanece acostado en una mesa de rayos X con la cabeza inmovilizada con una correa o cinta para evitar cualquier movimiento que pueda interrumpir el examen. La actividad cardíaca del paciente se monitorea por medio de un electrocardiograma. Justo antes del inicio del procedimiento, se administra una inyección de anestesia local en la región del cuerpo del paciente (generalmente la ingle) donde se introduce un catéter (tubo delgado). El catéter entra al interior de una arteria y se lo mueve cuidadosamente hacia arriba, a través del área abdominal, hacia una arteria en el cuello del paciente. Una vez que el catéter se encuentra en la posición deseada, se le inyecta un tinte especial y se toman radiografías para rastrear el movimiento del tinte a través de las arterias y los vasos sanguíneos del cerebro. Estas radiografías facilitan la identificación de la ubicación de cualquier bloqueo arterial y vascular y localizar cualquier defecto estructural vascular y arterial anormal que pueda tener el paciente en su cerebro.36
- Tomografía computarizada: aprenda más acerca de las tomografías computarizadas
- Imagen por resonancia magnética: aprenda más acerca de las imágenes por resonancia magnética
- Biopsia quirúrgica: aprenda más acerca de las biopsias
Clasificación y patología
Si existe la sospecha de que una persona tiene cáncer cerebral, se suelen extraer muestras de tejidos (biopsias) para confirmar o descartar la presencia del cáncer . Después de realizar la biopsia quirúrgica, el médico envía la muestra a un neuropatólogo, Un neuropatólogo es un patólogo que se especializa en los trastornos del sistema nervioso. El neuropatólogo examina la muestra tanto a nivel macroscópico (visible a simple vista) como microscópico (por medio de imágenes magnificadas) y le devuelve un informe patológico al médico. El informe de patología contiene información sobre la apariencia del tejido, la composición celular y el estado de enfermedad o normalidad. Para más información acerca de los reportes patológicos acuda a la sección de diagnóstico y detección.
Para poder producir un reporte patológico con información válida, el estudio de la muestra se debe llevar a cabo por un experto de la neuropatología. 35
Según la Sociedad americana de cáncer, no existe un sistema de clasificación para el cáncer cerebral que pueda predecir la progresión de la enfermedad con exactitud ya que hay una cantidad abundante de factores que están involucrados en los cánceres del sistema nervioso central. Desafortunadamente, el sistema de clasificación T/N/M no es una herramienta apropiada para el cáncer cerebral, pues la mayoría de cánceres que se desarrollan en el cerebro o de la espina dorsal no suele propagarse hacia otros órganos (metástasis).37 Sin embargo, la Organización Mundial de la Salud (OMS), ha establecido un sistema de clasificación histológica que se centra en el comportamiento biológico del tumor. Este sistema puede califica a los cánceres del sistema nervioso central (del I al IV) según sus características. Una vez que esta clasificación se analiza en conjunto con los otros datos clínicos del paciente, se determina un pronóstico. Los tumores de grado I a II (tumores de grado inferior) tienen algunas estructuras anormales, pero por lo general, se asemejan a los tejidos cerebrales normales. Los tumores de grado III tienen más anormalidades, mayor número de vasos sanguíneos y densidades celulares más altas. Los tumores de grado IV son los tumores cerebrales primarios más malignos, pues las células cancerígenas de este tipo de tumor tienen las características más anormales: un mayor número de vasos sanguíneos, un mayor crecimiento celular y densidades celulares muy altas. 38
Biología tumoral
Dentro de los últimos años, varios estudios han indicado que las células madre de los gliomas pueden desempeñar un rol importante en el desarrollo del cáncer cerebral y la reincidencia del mismo. La CD133 es una proteína que se encuentra en la superficie de las células que sirve como marcador de células madre. Por lo tanto, la detección de esta proteína indica la presencia de células madre de tumores cerebrales. Este tipo de célula madre suele formar parte de los tumores de los glioblastomas multiformes, ependimomas, astrocitomas, meduloblastomas, y de otras gliomas y cánceres cerebrales. Para agregar, estas células pueden desarrollar una resistencia a la quimio o radioterapia ya que son capaces de sobre-producir agentes anti-apoptóticos, de activar los puntos de control en el ciclo de celular para de reparar el ADN, y de impulsar la formación de los vasos sanguíneos (angiogénesis).39
Hay muchos genes que tienen un vínculo directo con el desarrollo y la propagación del cáncer de cerebro, como por ejemplo:
- TP53: este gen es un gen de supresión tumoral que se encarga de regular la división celular y la muerte celular (apoptosis). Aproximadamente la mitad de todos los tumores humanos tienen una mutación en este gen. Los estudios han demostrado que aproximadamente el 40% de los astrocitomas tienen un gen TP53 mutado o eliminado.32
- NF1: este gen codifica la producción de la neurofibromina, una proteína que funciona como supresor de tumores al regular la expresión de la Ras, otra proteína involucrada en el desarrollo del cáncer.40
- NF2: este gen codifica la producción de la merlina, una proteína que controla la forma de las células, el movimiento y la comunicación celular. La merlina también actúa como supresor de tumores en las células del sistema nervioso. Los estudios demuestran que el gen NF2 se elimina o se muta en aproximadamente 40 a 50% de los pacientes con meningioma.41, 32
- Bcl2: este gen codifica la producción de la proteína Bcl2 que inhibe la muerte celular. Estudios indican que la sobre-producción de la proteína Bcl2 aumenta la resistencia a los fármacos citotóxicos.42
- Myc: esta familia de genes codifica la producción de las proteínas del factor de transcripción Myc que participan en la formación de tumores y la regulación del ciclo celular. Las proteínas Myc se sobre-producen en varios tipos de gliomas, como en el meduloblastoma, astrocitomas, y en el glioblastoma multiforme.43, 44
- EGFR: este gen codifica la producción del receptor del factor de crecimiento epidérmico.45 Este receptor pertenece a la familia de receptores de tirosina quinasas. Estos tipos de receptores se encuentran sobre la superficie celular para que puedan formar uniones con los factores de crecimiento, las citoquinas, y otros factores de señalización celular. Un nivel elevado de la señalización de los receptores de tirosina quinasas por medio de la vía oncogénica PI3K-AKT-mTOR y la vía de Ras-MAPK parece estar vinculado a ciertos casos de gliomas malignos.46Algunos estudios indican que aproximadamente el 40% de glioblastomas y astrocitomas anaplásicos tienen demasiadas copias del gen EGFR (amplificación génética) y/o una cantidad excesiva de cambios (mutaciones) en el mismo.32, 47
- VEGF: este gen codifica la producción del factor de crecimiento endotelial vascular, una proteína clave para la formación de los vasos sanguíneos (angiogénesis) y la permeabilidad vascular. Su receptor, el receptor del factor de crecimiento endotelial vascular, también pertenece a la familia de receptores tirosina quinasa. Las investigaciones indican que el este VEGF se sobre-expresa con frecuencia en los meningiomas, así como en los gliomas malignos, como los astrocitomas y los glioblastomas pilocíticos.48
Tratamiento
La elección del tratamiento del cáncer de cerebro depende de la ubicación del tumor, la magnitud de los efectos dañinos en las funciones del cerebro y la médula espinal y el historial de salud del paciente. El tratamiento puede llevarse a cabo mediante: la quimioterapia, radioterapia, cirugía, administración de agentes terapéuticos auxiliares y la remoción quirúrgica del tumor. 35
Como organización CancerQuest se enfoca en proporcionar información acerca de la biología del cáncer y de sus posibles tratamientos, por lo cual no brindamos consejos o recomendaciones detalladas acerca de los tratamientos. A continuación se encuentran los enlaces a las páginas web de algunas organizaciones en los Estados Unidos que sí proveen estos servicios..
Aprenda más acerca de los tratamientos recomendados por la National Comprehensive Cancer Network (NCCN) para cánceres del sistema nervioso central.
Para más información acerca de cómo funcionan los tratamientos que hemos mencionado, acuda a nuestra sección dedicada a los tratamientos del cáncer.
Información acerca de los ensayos clínicos:
Información general de ensayos clínicos en CancerQuest
Información acerca de ensayos clínicos del Instituto nacional de cáncer.
Información acerca de ensayos clínicos en Georgia Clinical Trials Online.
Información acerca de ensayos clínicos del Winship Cancer Institute of Emory University
Fuentes de información acerca del cáncer cerebral
Factores de riesgo del cáncer cerebral
Factores de riesgo del desarrollo de tumores cerebrales (ABTA)
Factores de riesgo del desarrollo de tumores cerebrales y de la médula espinal (ACS)
Factores de riesgo del cáncer cerebral (CTCA)
La detección y el diagnóstico del cáncer cerebral
Instituto de cáncer: el diagnóstico y las etapas del cáncer
Tumores cerebrales y de la médula espinal en adultos (ACS)
Tumores cerebrales y de la médula espinal en niños (ACS)
Tratamientos del cáncer cerebral
Los ensayos clínicos del tratamiento del cáncer cerebral
Tratamiento de los tumores del sistema nervioso central en adultos (NCI)
Tratamiento de los tumores cerebrales y de la médula espinal en niños (NCI)
Opciones para el tratamiento del cáncer cerebral
Supervivencia del cáncer cerebral
Childhood Brain Tumor Foundation (Fundación para los niños con tumores cerebrales)
National Brain Tumor Society (Sociedad nacional del tumor cerebral)
Family Resources (PBTF) (Recursos de familia)
Riesgos de largo plazo para los supervivientes del cáncer cerebral
Efectos secundarios de la radioterapia para los tumores cerebrales (OncoLink)
Efectos secundarios de la radioterapia al cerebro
Fuentes internacionales información
Brain Tumor Foundation of Canada (Fundación canadiense por el tumor cerebral)
Dharamshila Hospital Brain Cancer Information - India (Información del hospital Dharamshila acerca de los tumores cerebrales)
Brain Tumors and Treatment in India - Mediconnect (Tumores cerebrales y su tratamiento en India)
Cancer Council Australia: Brain Cancer (Consejo australiano del cáncer: Cáncer cerebral)
Brain Tumours - Cancer Research UK (Tumores cerebrales - Cancer Research UK)
Resumen
Introducción
- El cáncer cerebral primario es la causa principal de muertes por cáncer en niños.
- El cáncer cerebral primario es la tercera causa más común de muertes por cáncer en adultos entre los 15 y 34 años de edad.
Tipos de cáncer cerebral
- El cáncer cerebral primario se puede clasificar en 2 tipos: gliomas y otros.
- Los gliomas malignos se originan en las células gliales del sistema nervioso central y son las formas más comunes y letales entre las malignidades cerebrales. Existen 3 tipos principales de gliomas: astrocitomas, oligodendrogliomas y ependinomas.
- Los otros tipos de cáncer cerebral no se originan en las células gliales del sistema nervioso central. Estos tumores se desarrollan en otras partes del cerebro, como por ejemplo los meningiomas y meduloblastomas.
Factores de riesgo
- Algunos trastornos genéticos, como la neufibromatosis tipo 1 y tipo 2, han sido identificados como posibles factores de riesgo para el cáncer cerebral.
- El riesgo de cáncer cerebral incrementa con la edad, con la excepción del neuroblastoma, mismo que comúnmente ocurre en niños pequeños.
- La posible relación entre las heridas en la cabeza y los meningiomas aún se investiga.
- El consumo de compuestos N-nitrosos durante el embarazo puede estar vinculado a un incremento en el riesgo del desarrollo del cáncer cerebral en los hijos.
Síntomas y detección
- Los dolores de cabeza pueden ser una señal de tumores cerebrales.
- Existen varias pruebas médicas que detectan o descartan la presencia de un tumor cerebral, como por ejemplo: exámenes neurológicos, angiografías cerebrales, tomografías computarizadas, imágenes por resonancia magnética y biopsias quirúrgicas.
Severidad y patología
- El cáncer cerebral no tiene un sistema de clasificación específico para predecir la progresión de la enfermedad con exactitud. El sistema T/N/M no es una herramienta apropiada para el cáncer cerebral ya que gran parte de los cánceres cerebrales y espinales no se propagan hacia otros órganos (metástasis).
- El cáncer cerebral se clasifica en base al sistema de clasificación histológica de la Organización Mundial de la Salud (OMS), que se basa en el comportamiento biológico del tumor.
Tratamiento
- Los tratamientos difieren dependiendo de factores específicos como: edad del paciente, condiciones de salud, etapa del cáncer, ubicación del tumor y más.
- Los tratamientos incluyen a: la cirugía, radioterapia, quimioterapia, y la administración de agentes terapéuticos auxiliares.
- 1ab Lu-Emerson C, Eichler AF. Brain metastases. Continuum (Minneap Minn). 2012 Apr;18(2):295-311. [PUBMED]
- 2 Volavsek M, Lamovec J, Popovic M. Extraneural metastases of anaplastic oligodendroglial tumors. Pathol Res Pract. 2009;205(7):502-7. Epub 2009 May 2. [PUBMED]
- 3 Kural C, Pusat S, Sentürk T, Seçer HI, Izci Y. Extracranial metastases of anaplastic oligodendroglioma. J Clin Neurosci. 2011 Jan;18(1):136-8. [PUBMED]
- 4 Overview of the Nervous System. Nachum Dafny, Ph.D., Department of Neurobiology and Anatomy, The UT Medical School at Houston. Copyright 2012 [http://nba.uth.tmc.edu/neuroscience/s2/chapter01.html]
- 5 Cancer Facts and Figures 2012. American Cancer Society [http://www.cancer.org/acs/groups/content/@epidemiologysurveilance/documents/document/acspc-031941.pdf]
- 6 Ries LAG, Smith MA, Gurney JG, Linet M, Tamra T, Young JL, Bunin GR (eds). Cancer Incidence and Survival among Children and Adolescents: United States SEER Program 1975-1995, National Cancer Institute, SEER Program. NIH Pub. No. 99-4649. Bethesda, MD, 1999. [http://seer.cancer.gov/publications/childhood/]
- 7 Nguyen TD, Abrey LE. Brain metastases: old problem, new strategies. Hematol Oncol Clin North Am. 2007;21(2):369-388. [PUBMED]
- 8 Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin. 2005 Mar-Apr;55(2):74-108. [PUBMED]
- 9ab American Cancer Society. Cancer Facts & Figures 2021. Atlanta: American Cancer Society; 2021. https://www.cancer.org/research/cancer-facts-statistics/all-cancer-facts-figures/cancer-facts-figures-2021.html]
- 10ab Human Physiology: The Mechanisms of Body Function. AJ Vander, J Sherman, D Luciano, EP Widmaier, H Raff, H Strang; published by McGraw-Hill, New York (2004).
- 11ab Neuroscience. 2nd edition. Purves D, Augustine GJ, Fitzpatrick D, et al., editors. Sunderland (MA): Sinauer Associates; 2001. [http://www.ncbi.nlm.nih.gov/books/NBK10799/]
- 12abc Brain Components. Medline Plus. [http://www.nlm.nih.gov/medlineplus/ency/anatomyvideos/000016.htm]
- 13 Brain Lobe image. Wikipedia [http://www.cancerquest.org/sites/default/files/assets/image/brain-lobes.png]
- 14 Louis DN, Ohgaki H, Wiestler OD, Cavenee WK, Burger PC, Jouvet A, Scheithauer BW, Kleihues P. The 2007 WHO classification of tumours of the central nervous system. Acta Neuropathol. 2007 Aug;114(2):97-109. Epub 2007 Jul 6. [PUBMED]
- 15 Parsons DW, Jones S, Zhang X, Lin JC, Leary RJ, Angenendt P, Mankoo P, Carter H, Siu IM, Gallia GL, Olivi A, McLendon R, Rasheed BA, Keir S, Nikolskaya T, Nikolsky Y, Busam DA, Tekleab H, Diaz LA Jr, Hartigan J, Smith DR, Strausberg RL, Marie SK, Shinjo SM, Yan H, Riggins GJ, Bigner DD, Karchin R, Papadopoulos N, Parmigiani G, Vogelstein B, Velculescu VE, Kinzler KW. An Integrated Genomic Analysis of Human Glioblastoma Multiforme. Science. 2008 Sep 26;321(5897):1807-12. doi: 10.1126/science.1164382. Epub 2008 Sep 4. [PUBMED]
- 16 Van Meir EG, Hadjipanayis CG, Norden AD, Shu HK, Wen PY, Olson JJ. Exciting new advances in neuro-oncology: the avenue to a cure for malignant glioma. CA Cancer J Clin. 2010 May-Jun;60(3):166-93. [PUBMED]
- 17 Huang Z, Cheng L, Guryanova OA, Wu Q, Bao S. Cancer stem cells in glioblastoma--molecular signaling and therapeutic targeting. Protein Cell. 2010 Jul;1(7):638-55. Epub 2010 Jul 29. [PUBMED]
- 18 Frosina G. Frontiers in targeting glioma stem cells. Eur J Cancer. 2011 Mar;47(4):496-507. Epub 2010 Dec 22. [PUBMED]
- 19 Astrocytomas and Glioblastomas. Neurology and Neurosurgery. Johns Hopkins Medicine. [http://www.hopkinsmedicine.org/neurology_neurosurgery/specialty_areas/brain_tumor/center/glioma/types/astrocytoma.html]
- 20 Van den Bent MJ, Reni M, Gatta G, Vecht C. Oligodendroglioma. Crit Rev Oncol Hematol. 2008 Jun;66(3):262-72. Epub 2008 Feb 12. [PUBMED]
- 21 Oligodendroglioma. Neurology and Neurosurgery. Johns Hopkins Medicine. [http://www.hopkinsmedicine.org/neurology_neurosurgery/specialty_areas/brain_tumor/center/glioma/types/oligodendroglioma.html]
- 22 Ependymoma. Neurology and Neurosurgery. Johns Hopkins Medicine. [http://www.hopkinsmedicine.org/neurology_neurosurgery/specialty_areas/brain_tumor/center/glioma/types/ependymoma.html]
- 23 Marta GN, Correa SF, Teixeira MJ. Meningioma: review of the literature with emphasis on the approach to radiotherapy. Expert Rev Anticancer Ther. 2011 Nov;11(11):1749-58. [PUBMED]
- 24 Link M., and Perry, A. Meningioma Tumorigenesis: An Overview of Etiologic Factors. From 'Meningiomas'. Published by Springer London. Joung Lee, Editor (2009) [http://dx.doi.org/10.1007/978-1-84628-784-8_11]
- 25 Schroeder K, Gururangan S. "Molecular variants and mutations in medulloblastoma." Pharmgenomics Pers Med. 2014 Feb 4;7:43-51. eCollection 2014. [PUBMED]
- 26 General Information About Central Nervous System (CNS) Embryonal Tumors. Childhood Central Nervous System Embryonal Tumors Treatment (PDQ®) [http://www.cancer.gov/cancertopics/pdq/treatment/childCNSembryonal/healthprofessional#Section_633]
- 27 Williams VC, Lucas J, Babcock MA, Gutmann DH, Korf B, Maria BL. Neurofibromatosis type 1 revisited. Pediatrics. 2009 Jan;123(1):124-33. doi: 10.1542/peds.2007-3204. [PUBMED]
- 28 Evans GR, Lloyd SK, Ramsden RT. Neurofibromatosis type 2. Adv Otorhinolaryngol. 2011;70:91-8. doi: 10.1159/000322482. Epub 2011 Feb 24. [PUBMED]
- 29 Wu J, Shin J, Xie D, Wang H, Gao J, Zhong XP. Tuberous Sclerosis 1 Promotes Invariant NKT Cell Anergy and Inhibits Invariant NKT Cell-Mediated Antitumor Immunity. J Immunol. 2014 Feb 14. [PUBMED]
- 30 Sharma P, Dhull VS, Bal C, Malhotra A, Kumar R. Von Hippel-Lindau Syndrome: Demonstration of Entire Disease Spectrum with (68)Ga-DOTANOC PET-CT. Korean J Radiol. 2014 Jan;15(1):169-72. doi: 10.3348/kjr.2014.15.1.169. Epub 2014 Jan 8. [PUBMED]
- 31 Malkin D. Li-fraumeni syndrome. Genes Cancer. 2011 Apr;2(4):475-84. doi: 10.1177/1947601911413466. [PUBMED]
- 32abcdef Wrensch M, Minn Y, Chew T, Bondy M, Berger MS. Epidemiology of primary brain tumors: current concepts and review of the literature. Neuro Oncol. 2002 Oct;4(4):278-99. [PUBMED]
- 33 McKean-Cowdin R, Pogoda JM, Lijinsky W, Holly EA, Mueller BA, Preston-Martin S. Maternal prenatal exposure to nitrosatable drugs and childhood brain tumours. Int J Epidemiol. 2003 Apr;32(2):211-7. [PUBMED]
- 34 Huncharek M, Kupelnick B. "A meta-analysis of maternal cured meat consumption during pregnancy and the risk of childhood brain tumors." Neuroepidemiology (2004); 23(1-2):78-84. [PUBMED]
- 35abcd Buckner JC, Brown PD, O'Neill BP, Meyer FB, Wetmore CJ, Uhm JH. Central nervous system tumors. Mayo Clin Proc. 2007 Oct;82(10):1271-86. Review. [PUBMED]
- 36 Cerebral Angiography. MedlinePlus. [http://www.nlm.nih.gov/medlineplus/ency/article/003799.htm]
- 37 "How are brain and spinal cord tumors in adults staged?" American Cancer Society. [http://www.cancer.org/Cancer/BrainCNSTumorsinAdults/DetailedGuide/brain-and-spinal-cord-tumors-in-adults-staging]
- 38 Persano L, Rampazzo E, Basso G, Viola G. "Glioblastoma cancer stem cells: role of the microenvironment and therapeutic targeting." Biochem Pharmacol. 2013 Mar 1;85(5):612-22. doi: 10.1016/j.bcp.2012.10.001. Epub 2012 Oct 11. [PUBMED]
- 39 Cheng JX, Liu BL, Zhang X. "How powerful is CD133 as a cancer stem cell marker in brain tumors?" Cancer Treat Rev. 2009 Aug;35(5):403-8. doi: 10.1016/j.ctrv.2009.03.002. Epub 2009 Apr 14. [PUBMED]
- 40 Friedman JM. Neurofibromatosis 1. GeneReviews [Internet]. [PUBMED]
- 41 Evans DG. Neurofibromatosis 2. GeneReviews [Internet]. [PUBMED]
- 42 Fels C, Schäfer C, Hüppe B, Bahn H, Heidecke V, Kramm CM, Lautenschläger C, Rainov NG. "Bcl-2 expression in higher-grade human glioma: a clinical and experimental study." J Neurooncol. 2000 Jul;48(3):207-16. [PUBMED]
- 43 Faria MH, Khayat AS, Burbano RR, Rabenhorst SH. "c -MYC amplification and expression in astrocytic tumors." Acta Neuropathol. 2008 Jul;116(1):87-95. doi: 10.1007/s00401-008-0368-0. Epub 2008 Mar 28. [PUBMED]
- 44 Swartling FJ. "Myc proteins in brain tumor development and maintenance." Ups J Med Sci. 2012 May;117(2):122-31. doi: 10.3109/03009734.2012.658975. Epub 2012 Feb 21. [PUBMED]
- 45 Lo HW, Hsu SC, Ali-Seyed M, Gunduz M, Xia W, Wei Y, Bartholomeusz G, Shih JY, Hung MC. Nuclear interaction of EGFR and STAT3 in the activation of the iNOS/NO pathway. Cancer Cell. 2005 Jun;7(6):575-89. [PUBMED]
- 46 Huse JT, Holland EC. "Targeting brain cancer: advances in the molecular pathology of malignant glioma and medulloblastoma." Nat Rev Cancer. 2010 May;10(5):319-31. doi: 10.1038/nrc2818. [PUBMED]
- 47 Hatanpaa KJ, Burma S, Zhao D, Habib AA. Epidermal growth factor receptor in glioma: signal transduction, neuropathology, imaging, and radioresistance. Neoplasia. 2010 Sep;12(9):675-84. [PUBMED]
- 48 Stockhammer G, Obwegeser A, Kostron H, Schumacher P, Muigg A, Felber S, Maier H, Slavc I, Gunsilius E, Gastl G. Vascular endothelial growth factor (VEGF) is elevated in brain tumor cysts and correlates with tumor progression. Acta Neuropathol. 2000 Jul;100(1):101-5. [PUBMED]
