Todo tipo de cáncer se distingue por su origen, su estructura y su reacción al tratamiento, por lo cual la prevención exitosa de la enfermedad se complica. Existen pocas evidencias que indiquen que una actividad o un elemento dietético logra impedir el desarrollo del cáncer, pues el objetivo de la prevención del cáncer es producir un resultado en el que nada cambia (es decir, el cáncer no se desarrolla). Además, la prevención del cáncer no se puede lograr con una sola acción, por ende se deben tomar varias medidas preventivas durante muchos años para poder evaluar la eficacia del método de prevención. Incluso si se logra demostrar que algo ayuda a prevenir cierto tipo de cáncer, no hay garantía de que comer o comportarse de cierta manera absolutamente asegure la ausencia del desarrollo del cáncer.
Gran parte de las evidencias que existen para la prevención del cáncer no son definitivas. Por ejemplo, una dieta baja en grasa,1, 2 alta en fibra 3, 4 , frutas y verduras 5, 6 se asocia con un menor riesgo de desarrollar diferentes tipos de cánceres. Por otro lado, varios estudios demuestran que no existe ninguna conexión entre este tipo de dietas y una reducción en los casos de cáncer. 7, 8, 9 De igual modo, mientras que algunos estudios indican que el ejercicio reduce la aparición de cáncer en algunos en otros, el ejercicio no parece marcar la diferencia.10, 11
A pesar de la evidencia contradictoria, el Instituto nacional del cáncer sostiene que la mejor manera de prevenir el cáncer es hacer ejercicio, así como seguir una dieta baja en calorías que contenga fibra, frutas y verduras. También recomiendan evitar una vida sedentaria, comer grasa animal y carnes al carbón para evitar el riesgo de desarrollar cáncer.12 Para agregar, varias investigaciones indican que una combinación de diferentes nutrientes esenciales es mejor que el consumo de una gran cantidad de un solo alimento.13
Otra manera de prevenir el cáncer es evitar aquellas actividades que están asociadas con el desarrollo del cáncer. Algunas de estas actividades son fumar tabaco, 14, 15, 16 tomar bebidas alcohólicas, 17, 18 la obesidad 17, 19, 20 y la exposición al sol 21, 22 . Un estudio de familias suecas demuestra que el desarrollo del cáncer está vinculado con varios factores ambientales, la dieta y la cantidad actividad físicas que con factores hereditarios.23 La Sociedad americana contra el cáncer sugiere que un tercio de las muertes por cáncer en los Estados Unidos están relacionadas con dietas pobres y la falta de actividad física. Además, otro tercio de las muertes por cáncer se pueden prevenir al evitar el consumo de tabaco.24 La Organización mundial de la salud propone que el 40% de las muertes por cáncer en el mundo, se podrían prevenir con buenas dietas, realizar actividad física y no consumir tabaco.25
Aparte de las recomendaciones que se han mencionado, existen algunos suplementos médicos que pueden contribuir a la prevención del cáncer.26
Las siguientes secciones describen los métodos preventivos para el cáncer con mayor detalle.
- El ejercicio y el riesgo del cáncer
- Antioxidantes
- Productos de las plantas (Fitoquímicos)
- Medicamentos
- Vacunas para el cáncer
- Tablas de la prevención del cáncer
Si le parece útil el material, por favor considere apoyar a nuestra página web.
El ejercicio y el riesgo del cáncer
- ¿Qué es la actividad física?
- Epidemiología de la actividad física y la prevención del cáncer
- ¿Cómo se reduce el riesgo del cáncer mediante el ejercicio?
- Racial Diferencias raciales en la relación con el ejercicio y la reducción del riesgo del cáncer
La actividad física se define como el uso de los músculos esqueléticos para consumir más energía en comparación con cuando uno está quieto.27
La actividad física puede tomar varias formas, desde una caminata diaria al levantamiento de pesas. La mayoría de las pautas internacionales recomiendan que los adultos saludables dediquen 150 minutos por semana a la actividad física. Preferiblemente, el ejercicio se debe dividir en el transcurso de la semana. Varias investigaciones indican que una amplia variedad de beneficios para la salud se pueden lograr al realizar más actividad física.28
El ejercicio puede ocasionar varios cambios en el cuerpo humano. Estos tipos de cambios dependen de la cantidad y del tipo de ejercicio. El ejercicio aumenta la cantidad de la sangre que se bombea en el corazón (Gasto cardíaco). Como resultado, el flujo del oxígeno y de la sangre aumenta, lo cual desencadena la secreción de hormonas, pues las glándulas adrenales, los tejidos que se encargan de la secreción de la epinefrina (adrenalina) y de la norepinefrina (noradrenalina), se activan. El ejercicio provoca la elevación temporaria del lactato (producto de la digestión de azúcar en los músculos), la presión arterial y realza la función inmunológica. El ejercicio también acelera el metabolismo y el consumo de la glucosa. Se presume que al combinarse, estos efectos del ejercicio pueden reducir el cáncer.29
La epidemiología del cáncer y su relación con el ejercicio
La actividad física se asocia con un riesgo reducido de desarrollar el cáncer en siete partes distintas del cuerpo: la vejiga, el colon, los senos, el endometrio, los pulmones, el esófago, el riñón y el estómago. La actividad física también se ha vinculado a una reducción en la incidencia del cáncer del páncreas y de los ovarios.30
Algunos ejemplos que ilustran la relación entre la actividad física y el cáncer:
Cáncer de vejiga
La actividad física se ha vinculado con una reducción en los casos del cáncer de vejiga. Para poder confirmar esta relación, se deben realizar más estudios que se enfoquen en otros factores externos..31
Cáncer de seno
Las mujeres que tienen un historial familiar con el cáncer de seno pero que hacen ejercicio con regularidad tienen un riesgo reducido de desarrollar el cáncer de seno pos-menopausia. El efecto que tiene el ejercicio sobre el riesgo de desarrollar el cáncer pre-menopausia sigue bajo investigación..32
Cáncer de colon
Algunos estudios han demostrado que la actividad física puede reducir el riesgo de desarrollar el cáncer de colon, especialmente en personas obesas o que están sobrepeso.33
Cáncer del endometrio
Aunque se deben realizar más investigaciones para poder medir el nivel de la reducción del riesgo que produce la actividad física, el ejercicio moderado está asociado con un riesgo menor a desarrollar el cáncer de endometrio..34
Cáncer de esófago
A pesar de que varios estudios ya indican que la actividad física brinda un cierto tipo de protección en contra del cáncer gástrico y de esófago, para poder evaluar la intensidad del ejercicio que se necesita para gozar de sus beneficios se deben realizar más investigaciones.35
Cáncer de riñón (renal)
Una revisión de las investigaciones disponibles que se realizó en el 2013 concluyó que la actividad física puede reducir el riesgo de desarrollar el cáncer renal en un 22%. Las investigaciones actuales se centran en determinar la intensidad, la frecuencia y la duración del ejercicio que se necesita para reducir el cáncer renal.36
¿Cómo es que el ejercicio reduce el riesgo de desarrollar el cáncer?
Aunque está claro que existe una asociación entre el ejercicio y un riesgo reducido de desarrollar el cáncer, aun se desconocen los mecanismos detrás de cómo esto ocurre. Hasta la fecha, gran parte de lo que han logrado identificar las investigaciones son cambios en las vías metabólicas claves para el desarrollo del cáncer. Al igual que una cantidad elevada de colesterol puede señalar la presencia de una enfermedad cardíaca, se han hallado a varios ‘biomarcadores’ que indican que existe un vínculo entre el ejercicio y un riesgo reducido de desarrollar el cáncer.37
El ejercicio reduce la cantidad de hormonas sexuales
El estrógeno es una hormona sexual que regula al sistema reproductivo femenino. Aunque el estrógeno es esencial para el cuerpo femenino, las mujeres que tienen niveles elevados de estrógeno y otras hormonas sexuales (andrógenos) están expuestas a un riesgo mayor de desarrollar el cáncer de seno. Los estudios demuestran que al realizarlo con suficiente frecuencia e intensidad, el ejercicio puede ocasionar reducciones significativas a los niveles de estas hormonas.37
El ejercicio previene la elevación de los niveles de la insulina
La resistencia a la insulina produce una cantidad alta de insulina y de glucosa dentro de la sangre. La insulina aumenta la probabilidad de que se desarrolle un tumor al activar la proliferación de las células (la división rápida) y la inhibición de la apoptosis (muerte celular programada).37 Gran parte de la investigación que se enfoca en los efectos del ejercicio en el crecimiento del cáncer se centra en la relación de la enfermedad con los agentes metabólicos que circulan por la sangre, particularmente, con la insulina y la glucosa. Se ha demostrado que el ejercicio tiene una correlación con una reducción en los niveles de insulina de los pacientes de cáncer.38, 39
El ejercicio reduce la inflamación y regula los niveles de la insulina39
Un estudio que midió la cantidad, el tipo, y la intensidad de la actividad física en conjunto con la grasa corporal y la dieta, halló que una combinación de actividades aeróbicas y de resistencia está vinculada con una reducción en la cantidad de biomarcadores del cáncer.38
Los biomarcadores de la inflamación incluyen a la proteína reactiva C (una proteína cuya cantidad abunda durante los períodos de inflamación), la interleucina-6 (IL-6) y al factor de necrosis pulmonar alfa (proteínas que regulan al sistema inmunológico).
Los biomarcadores que indican que el cuerpo tiene un nivel alto de insulina incluyen al péptido C, un producto secundario de la producción de la insulina. Los marcadores de la resistencia a la insulina incluyen a una cantidad alta de triglicéridos (TG), una elevación en la proporción entre el colesterol bueno y malo y una escasez de adiponectina (un nivel bajo de adiponectina desempeña un rol importante en el desarrollo de las enfermedades relacionadas a la obesidad.
Varias investigaciones indican que un nivel favorable de biomarcadores de la insulina y de la inflamación está vinculado a la actividad física. Las evidencias resaltan los beneficios de la actividad física de intensidad moderada. El ejercicio que combina el entrenamiento aeróbico y de resistencia tienen un impacto más fuerte en comparación con el ejercicio aeróbico por sí solo.
Varios expertos han observado que un nivel alto de actividad física que preferiblemente combina la actividad aeróbica y de resistencia tiene una relación con cantidades favorables de los biomarcadores de la inflamación y de la insulina. Este suceso se manifestó con bastante semejanza entre múltiples grupos de personas con distintos niveles de grasa corporal (adiposidad) y que siguen dietas distintas. La actividad física también reduce la adiposidad, lo cual es esencial para mantener un buen equilibrio entre los niveles de los biomarcadores de la inflamación y de la insulina.
El ejercicio realza al sistema inmunológico.
El ejercicio promueve la activación de las células asesinas naturales, una clase de células que tienen la capacidad de reconocer y matar a otras células, incluyendo a las células cancerígenas. Como resultado de la elevación del nivel de catecolaminas (un grupo de hormonas que se secretan al hacer ejercicio), la cantidad de células asesinas en la sangre crece.
Las células asesinas naturales de los humanos logran matar al cáncer con bastante eficiencia. La activación de estas células por medio del ejercicio desempeña un rol único en el tratamiento del cáncer. Las investigaciones indican que el ejercicio puede impulsar la reacción inmunológica a los tumores. El uso de inhbidores de puntos de control inmunitario también puede realzar la actividad inmune del cuerpo.29
Aprenda más acerca de los tratamientos con inhibidores de puntos de control inmunitario
El ejercicio cambia los niveles del micro-ARN (miARN)
El ARN es una molécula clave para la circulación de información genética dentro de las células. Mientras que el ADN es una molécula que ‘almacena’ la información genética, el ARN es la estructura ‘funcional’ de la misma. El micro-ARN es una clase de hilo pequeño de ARN que regula cuántas vías metabólicas se mantienen activas a la vez. Se ha demostrado que una cantidad regular de ejercicio a la semana puede cambiar los niveles de varios tipos de micro-ARN en la sangre. El líquido sanguíneo de aquellas personas que hacen más ejercicio ha logrado reducir la supervivencia de células de cáncer de seno dentro del laboratorio. Por lo tanto, los expertos le atribuyen este cambio a la cantidad de micro-ARN en esas muestras.40
Aprenda más acerca del micro-ARN
El ejercicio cambia los niveles de los radicales de oxígeno y de la señalización celular
Los radicales son químicos que se producen en las células. La formación de estos puede resultar de la absorción de comida, la exposición a la radiación y de otros procesos. Los radicales son bastante reactivos y se combinan con o pueden hasta provocar lesiones en otras partes de la célula con facilidad. Varios de los radicales importantes de las células provienen del oxígeno, por lo cual se los denomina radicales de oxígeno.
El desarrollo del cáncer se puede impulsar por medio de mutaciones u otras lesiones celulares que ocasionan los radicales. Los niveles de los radicales de oxígeno y de nitrógeno en los músculos esqueléticos aumentan con ejercicio de intensidad moderada a alta. Mientras tanto, estos niveles elevados provocan la activación de los genes y las proteínas que bloquean o destruyen a los radicales. El aumento de la actividad que destruye a los radicales puede retrasar o matar a las células cancerígenas. La combinación del ejercicio con la radioterapia y/o la quimioterapia puede generar un efecto aditivo, mejorando la eficacia de los tratamientos al matar a las células cancerígenas.41
Se presume que los músculos esqueléticos desempeñan un rol esencial en la relación entre el ejercicio y la reducción del cáncer. Los músculos esqueléticos producen moléculas de señalización celular (citoquinas) y factores de crecimiento. Estos agentes pueden movilizarse en la sangre y afectar a todo el cuerpo. Algunos productos musculares pueden inhibir la actividad de las células de tumores, pues regulan la producción de proteínas que bloquean la reproducción celular, alteran los niveles de los radicales de oxígeno y conllevan a la secreción del mi-ARN de señalización celular dentro del sistema circulatorio.
Una combinación de ejercicio aeróbico y de resistencia parece producir el mejor beneficio para los pacientes y los sobrevivientes de cáncer.
El diseño de las investigaciones que tratan el vínculo entre el cáncer y el ejercicio es algo complicado, por lo cual los resultados no son consistentes. Consecuentemente, es bastante difícil determinar el mecanismo exacto por el cual el ejercicio reduce el riesgo de desarrollar el cáncer. Los estudios que miden la cantidad de ejercicio y lo comparan con algunos aspectos del cáncer, suelen depender de auto-reportes con respecto al ejercicio, y por ende son subjetivos y carecen de autenticidad y validez. A pesar de estas limitaciones, nuestro conocimiento acerca del riesgo del cáncer y el ejercicio continúa avanzando.39
Disparidades raciales relacionadas a la actividad física y a la prevención del cáncer
Las diferencias relacionadas al nivel de actividad física pueden surgir de la raza, la etnicidad y el género. Por ejemplo, un nivel bajo de recursos financieros puede resultar en una mala salud en los niños, lo cual aumenta la probabilidad de desarrollar condiciones críticas y la duración de la hospitalización. El estatus económico también afecta el nivel educativo. Una mala salud en la infancia puede afectar la transferencia del estatus económico y de un bienestar saludable de generación en generación. El 33.8% de los adultos blancos, 23.8% de los adultos hispanos y el 23.2% de los adultos negros practican la actividad física en su tiempo libre con regularidad. El nivel de actividad física no-ocupacional es significativamente menor en la población negra, hispana, y en otras comunidades minoritarias; estas diferencias, en parte se pueden explicar con el nivel de educación, el estatus socio-económico y las ubicación geográfica de las residencias de estas personas. Dentro de estas comunidades, la cantidad de actividad física ocupacional es mayor al nivel de actividad física recreativa. La ausencia de la actividad física no-ocupacional minimiza los beneficios asociados con el ejercicio, incluyendo a la prevención del cáncer.42
Por ejemplo, un estudio de 1735 pacientes de cáncer de seno reveló que la probabilidad de que los pacientes afroamericanos no realicen la cantidad recomendada de ejercicio antes o después de ser diagnosticados era considerablemente alta.43
Antioxidantes
El rol que desempeñan los antioxidantes en la prevención y el tratamiento de una variedad de condiciones médicas ha recibido bastante atención pública por la suposición de que los antioxidantes pueden tener cierta influencia positiva en algunas enfermedades. Desafortunadamente, parte del entusiasmo no se basa en evidencia científica. Para comprender cómo funcionan los antioxidantes, primero es importante comprender el proceso de oxidación.
¿Qué es la oxidación?
La oxidación es el proceso químico que provoca que los metales se oxiden y que las manzanas se vuelvan marrones. Cuando este mismo proceso ocurre dentro del cuerpo, las células y los tejidos pueden sufrir lesiones. Los radicales libres son un grupo de químicos pequeños y son los agentes causantes de estos daños. La exposición a los radicales libres pueden ser el resultado de una variedad de cosas, como de la inhalación del humo del tabaco, el contacto con la radiación (como la luz solar o los rayos X) e incluso el funcionamiento normal del cuerpo humano. Los radicales libres son inestables y pueden interactuar con y alterar a otras moléculas, como al ADN, a los lípidos y a las proteínas. Como resultado de estas reacciones, se presentan cambios (oxidación) que interfieren con la actividad normal de las moléculas que se modificaron, dando paso a varios problemas graves al nivel de la célula y, en última instancia, al nivel corporal.
¿Qué son los antioxidantes?
Como su nombre lo indica, los antioxidantes son moléculas que previenen o revierten el proceso de la oxidación, como por ejemplo, las vitaminas C y E. Los antioxidantes han logrado interactuar con y neutralizar a los radicales libres en ámbitos in vitro, 44, 45además de mejorar y prolongar la salud y vida de los animales 46, 47. Algunas investigaciones contemporáneas se han enfocado en la posibilidad de la prevención del cáncer en los humanos por medio de los antioxidantes. Los antioxidantes son sustancias importantes para el cuerpo humano, pues detienen a las moléculas "radicalizadas" antes de que causen daño al donar un electrón a un radical libre sin necesidad de robar otro electrón. A diferencia de la mayoría de los compuestos, los antioxidantes son estables con o sin el electrón que donan. Algunos antioxidantes funcionan de manera "suicida" y neutralizan a los radicales libres al formar uniones permanentes con ellos.
Fuentes y usos de los antioxidantes
Existen bastantes fuentes de antioxidantes, como el té verde, los frutos rojos, los tomates y la soya. Los antioxidantes abundan en muchas frutas y verduras ya que las plantas suelen producir antioxidantes para ayudar a protegerse de los radicales libres creados por la radiación del sol. Asimismo, el cuerpo humano también produce algunos antioxidantes por sí solo para defenderse en contra del daño de los radicales libres, sin embargo, esta protección no es absoluta. Por lo tanto, los seres humanos deben consumir antioxidantes de otras fuentes si desean disminuir el riesgo de desarrollar enfermedades que aumentan por el daño de los radicales libres. 48 Los antioxidantes también tienen varios usos prácticos no relacionados a la salud humana, por ejemplo: los restauradores de los museos los usan para conservar artefactos que pertenecían a seres vivos. Los antioxidantes también pueden prevenir que los alimentos se pudran. Para agregar, estas sustancias también pueden mejorar la calidad de plásticos, combustibles y pinturas. 48
NOTA: Sólo porque algo sea saludable no significa que su consumo en grandes cantidades sea lo mejor. Aún cuando las sustancias sean saludables es peligroso ingerirlas en grandes cantidades. De hecho, varios estudios recientes han hallado un vínculo entre el consumo de antioxidantes con la propagación del cáncer, pues los beneficios de los antioxidantes no se limitan a las células sanas; parece que también pueden contribuir a la supervivencia y a la propagación de las células cancerígenas. Como parte de una investigación, se le administró un fármaco anti-diabético a un grupo de ratones. Este medicamento activa la proteína NRF2, lo cual aumenta el nivel de antioxidantes en las células. Como resultado, la migración celular y la metástasis pareció haber aumentado en aquellos ratones que tenían tumores preexistentes. Asegúrese de informarle a su médico sobre cualquier medicamento que pueda estar tomando y siempre pregunte antes de comenzar a tomar cualquier suplemento.
Vea una entrevista acerca de los antioxidantes con el urólogo Dr. John Petros.
Vista cercana a los radicales libres
Los átomos están compuestos de un núcleo que contiene protones, neutrones, y un grupo de partículas (electrones) que circulan constantemente alrededor del núcleo, como satélites alrededor del mundo. En la mayoría de moléculas, los electrones se movilizan en pares alrededor del núcleo. Los radicales libres son una excepción. pues solamente tienen un electrón (sin pareja) que rodea al núcleo. Esta cualidad provoca que otras moléculas experimenten bastante atracción hacia los radicales. Se dice que una molécula con un electrón desapareado está "radicalizada". Estos compuestos radicalizados, o radicales libres, tienen la capacidad de reaccionar rápidamente con otras moléculas. Por esta razón, estos compuestos también se denominan especies reactivas. El oxígeno es la especie reactiva más común que se encuentra en el cuerpo humano y cuando adquiere un electrón adicional se denomina especie reactiva de oxígeno (ERO).
Los radicales libres suelen 'robarse' un electrón de otra molécula cercana para que todos sus electrones estén en pares. Consecuentemente, las moléculas que donaron su electrón se convierten en radicales. Esta reacción de 'robo' de electrones suele ocurrir en serie dentro de una célula. Para agregar, los radicales libres pueden afectar a casi cualquier estructura celular, incluyendo al ADN. Si los radicales libres roban un electrón del ADN, la actividad de la célula y el código genético podrían verse afectados. Las lesiones en el ADN que surgen de las reacciones con los radicales libres se han vinculado al proceso de envejecimiento, a la artritis reumatoide, al síndrome del intestino inflamatorio, síndrome de dificultad respiratoria aguda, enfisema, y algunos tipos de cáncer.49, 48, 50
Productos de plantas (Fitoquímicos)
Los fitoquímicos son compuestos que provienen de las plantas. Los siguientes fitoquímicos suelen ser el enfoque de varias investigaciones que evalúan sus posibles beneficios a la salud humana; incluso cuando se extraen de la planta de la que proceden. Dentro de los últimos años se ha realizado una gran cantidad de estudios que investigan la eficacia de estos compuestos naturales, específicamente para la prevención y el tratamiento del cáncer. Tome en cuenta que el siguiente listado no pretende ser completa, pues existen muchos otros productos químicos que se están examinando. Hemos elegido algunos de los agentes más populares y estudiados.
Los items de esta lista contienen un enlace a una sección acerca de los productos de las plantas en nuestra página dedicada a la oncología integrativa.
- Antocianina (Moras: Zarzamoras, Frambuesas, Arándano azul)
- Cúrcuma (Curry)
- EGCG (Té Verde)
- Licopeno (Tomates)
- Fitoestrógenos (Soya)
- Picnogenol (Pinos)
- Resveratrol (Uvas, Vino)
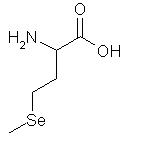
- Selenio (Nuez)
Medicamentos
El gobierno federal regula la administración de los medicamentos que se utilizan para ayudar a prevenir el cáncer se regulan con gran cautela con fines de garantizar la calidad y la seguridad. La eficacia de la mayoría de los medicamentos que recomiendan los médicos para prevenir el cáncer solamente se manifiesta en ciertas poblaciones tienen un alto riesgo de desarrollar la enfermedad. Por lo tanto, no es aconsejable que todas las personas tomen estas medicinas ya que se pueden presentar otras complicaciones. Sin embargo, se ha demostrado que algunos medicamentos logran reducir el riesgo de desarrollar el cáncer y su uso ha sido aprobado por la FDA para la prevención del cáncer, como por ejemplo, los medicamentos antiinflamatorios no esteroides (AINE) y los antagonistas hormonales tamoxifeno y raloxifeno.
Antiinflamatorios no esteroideos (AINES)
Tipos de NSAIDs
Inhibidores COX-1:

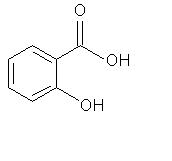
Estructura del acetaminofén Estructura del diclofenaco

Estructura del ibuprofeno Estructura del ácido salicílico
Inhibidores COX-2:

Estructura del celecoxib Estructura del naproxeno

Estructura del rofecoxib Estructura del valdecoxib
Introducción y antecedentes
La respuesta inflamatoria es una función normal del sistema inmunológico humano que ayuda a reparar al cuerpo después de una lesión. Por ejemplo, cuando la piel sufre cortes o lastimados el área generalmente se enrojece, arde y se hincha. El sistema inmunológico lleva cabo gran parte de este proceso, pues sirve para curar al área dañada del cuerpo. Esta reacción corporal trae sangre rica en nutrientes al área para que los tejidos lesionados puedan repararse y reproducir células nuevas.51 A pesar de ser un proceso que usualmente trae beneficios, varias investigaciones han demostrado que la respuesta inflamatoria humana es importante para mantener el entorno óptimo para la supervivencia de las células cancerígenas. Por ejemplo, la inflamación puede promover la angiogénesis así como el desarrollo, el crecimiento y la metástasis del tumor. Las células del sistema inmunológico, como los macrófagos, también pueden verse afectadas negativamente por la inflamación. 52, 53, 54, 55 Además, estas mismas células, que son productos del sistema inmune, pueden averiarse y crecer sin una regulación adecuada; este comportamiento puede conducir al inicio de un crecimiento cancerígeno.51
Aprenda más acerca de la angiogénesis y metástasis
Los medicamentos Antiinflamatorios No Esteroideos (AINEs) interfieren con la actividad de una familia de enzimas llamadas ciclooxigenasas (COX). Los inhibidores COX previenen que estas enzimas produzcan señales químicas que inducen la inflamación, el dolor y posiblemente el crecimiento de un tumor56 Existen dos tipos diferentes de AINEs, y se suelen clasificar según el tipo de COX que inhiben (COX-1 o COX-2). Los AINEs son muy comunes y se suelen tomar para aliviar el dolor [acetaminofén(Tylenol®), diclofenaco (Voltaren®), ibuprofeno (Advil®), ácido salicílico (Aspirin®), celecoxib (Celebrex®), naproxeno (Aleve®), rofecoxib (Vioxx®), y valdecoxib (Bextra®)]. La aspirina también se toma para la prevención de enfermedades del corazón. Para este uso, la dosis promedio de la aspirina que recomiendan los doctores es de 81mg/día.57
Investigación científica
Los investigadores indican que los AINEs son agentes quimiopreventivos efectivos, pero se han identificado efectos secundarios que se deben tomar en cuenta. Se ha demostrado que el uso regular de la aspirina ha reducido el riesgo de desarrollar el cáncer colorrectal y su recurrencia en humanos 58, 59, 56, 60, 61, 62 . Aún se desconoce el mecanismo por el cual estos fármacos logran reducir el riesgo de desarrollar algún cáncer, pero parece ser que tiene algo que ver con la habilidad que poseen para bloquear las ciclooxigenasas (COX).63
El consumo de los inhibidores COX-1 está asociado con algunos problemas digestivos como son las hemorragias y úlceras.57
Algunos estudios se han estado enfocando en los inhibidores COX-2 y en la posibilidad de que estos aumenten el riesgo de sufrir ataques al corazón y parálisis cerebral.64 Por esta razón es que se recomienda que solamente la gente que tiene un alto riesgo de desarrollar el cáncer tome medicinas AINE de manera regular como método preventivo. Varias investigaciones pretenden identificar la sub-población de la gente que debería tomar AINE para reducir el desarrollo de cáncer de colon.65
En algunos casos, la aspirina, un tipo de AINE se ha documentado como reductor de riesgo de desarrollar ciertos tipos de cánceres, notablemente el cáncer colorrectal, y algunos cánceres del esófago, estómago, seno, ovario y pulmón.66 También se ha demostrado que la aspirina puede reducir el riesgo de desarrollar un esófago de Barrett, un precursor del cáncer de esófago.67 Sin embargo, se ha propuesto que el uso de la aspirina puede incrementar el riesgo de desarrollar cáncer de riñón.68
En algunos estudios se ha visto que algunos individuos que tienen un alto riesgo de desarrollar el cáncer de colon pueden reducir la recurrencias de adenomas o adenomas avanzados del colon mediante el uso de la aspirina.69 Sin embargo, su efectividad en la prevención puede depender de la duración del uso y la dosis que se ingiere 70, 71. Se ha documentado que el uso a largo plazo de la aspirina puede reducir la incidencia del cáncer de colon. En contraste, aquellos estudios que administraron dosis de aspirina por menos tiempo no obtuvieron dichos resultados 72, 73. La Comisión de Servicios Preventivos de los Estados Unidos ha concluido que por lo general, el consumo de la aspirina con fines preventivos puede provocar mayor daño que beneficio en aquellos individuos que no tienen un riesgo elevado de desarrollar el cáncer de colon.74 Tome en cuenta que se necesitan más investigaciones para definir si los beneficios superan los posibles riesgos para las personas que tienen un mayor riesgo de desarrollar cáncer colorrectal. En resumen, se ha demostrado que la aspirina puede reducir el riesgo de desarrollar el cáncer colorrectal y los adenomas, y la recurrencia de las mismas. Sin embargo, la eficacia del consumo de la aspirina para la prevención del cáncer colorrectal depende del riesgo de que una persona desarrolle cáncer, pues los posibles efectos negativos de la aspirina deben compararse con sus beneficios de quimioprevención.
Asimismo, los resultados de algunos estudios enfocados en el consumo de la aspirina y la reducción del riesgo de desarrollar el cáncer de próstata han sido inconsistentes.75 Varias investigaciones indican que la aspirina puede reducir los niveles de un antígeno prostático específico en individuos que tienen cánceres latentes, y por lo tanto afecta la detección de cáncer de próstata.76 Otras investigaciones indican que con el cáncer colorrectal, la dosis y la duración del consumo de la aspirina desempeña un papel importante en el efecto protector del fármaco.77 Por ejemplo, un grupo de expertos concluyó que la exposición a una dosis de al menos 80mg de aspirina por 8 años ocasionaba a una decadencia del 18% en el riesgo del desarrollo del cáncer de próstata. Sin embargo, al realizar una evaluación un año después de que los participantes hayan tomado aspirina de manera regular por 7 años, no se encontró ningún efecto preventivo.
Aún se desconoce si la aspirina también puede reducir el riesgo de desarrollar el cáncer de mama. Mientras algunos estudios han demostrado que el uso de la aspirina está asociado con la reducción del desarrollo del cáncer de mama78, otros indican que no se logra reducir el riesgo del desarrollo del cáncer como resultado del uso de la aspirina como método preventivo.77 Una posible explicación es que los efectos de la medicina se manifiestan de manera según el tipo de cáncer de mama. Por ejemplo, el consumo diario de la aspirina está asociado con la reducción del riesgo de desarrollar el cáncer de mama ER-positivo.77 Algunas investigaciones recientes señalan que la aspirina también puede prevenir la metástasis en el cáncer de mama 79.
Aprobación de la Administración de alimentos y fármacos de los Estados Unidos (FDA)
El Celecoxib (Celebrex®) es el único AINE cuyo uso ha sido aprobado para tratar al cáncer. Este medicamento se puede administrar para la reducción de pólipos en aquellos que sufren de desordenes genéticos raros (poliposis adenomatosa). 80. En el año 2007 la Comisión de Servicios Preventivos de los Estados Unidos hizo recomendó evitar el uso de la aspirina para la prevención del cáncer colorrectal.81
Antagonistas Hormonales

Medicamentos:
Tamoxifeno- Nolvadex®
Raloxifeno- Evista®, Keoxifeno, Raloxifeno hidroclorado
Clasificados como:
Antagonistas hormonales

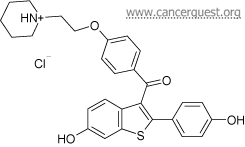
Estructura del tamoxifeno Estructura del raloxifeno
Introducción y Antecedentes
El tamoxifeno y el raloxifeno son dos medicamentos distintos cuya estructura se asemeja a la del estrógeno. Originalmente el tamoxifeno se desarrolló en la década de los 60 como un posible anticonceptivo, sin embargo después de que se descubrió que era ineficaz para este uso, los médicos comenzaron a investigarlo por su posible uso en contra de los cánceres estimulados por estrógenos. 82, 83 Diez años después se ejecutó una serie de estudios con el cáncer de mama en etapa avanzada y se descubrió que este fármaco podría ser un tratamiento potente. En el año 1998 se aprobó el uso del tamoxifeno como el primer agente quimiopreventivo para mujeres que tienen alto riesgo de cáncer de mama. 83, 84
El tamoxifeno y raloxifeno están clasificados como moduladores selectivos de los receptores de estrógenos (MSRE) por su capacidad de bloquear la reacción celular hacia los estrógenos. Se ha descubierto que el tamoxifeno puede inducir el desarrollo del cáncer de útero y el crecimiento de coágulos sanguíneos que podrían bloquear las arterias (tromboembolia). A causa de este efecto secundario negativo, los doctores recomiendan que únicamente las mujeres con riesgos altos de desarrollar el cáncer de mama deberían tomar este medicamento como una medida preventiva 84, 85 .
Investigación científica
Algunos estudios recientes demuestran que el desarrollo de tumores en el cáncer de mama se puede inhibir según los resultados de varios experimentos con ratas que fueron tratadas con tamoxifeno.86 A pesar de los efectos positivos del tamoxifeno, se ha descubierto que esta medicina puede aumentar las posibilidades de desarrollar el cáncer de útero y de endometrio; esto podría ser por su habilidad de dañar al ADN en las células sanas.87 Por otro lado, se ha visto que el tamoxifeno y el raloxifeno tienen la capacidad de reducir la incidencia de invasión del cáncer de mama por un 50% en las mujeres que tienen un alto riesgo de desarrollarlo 88, 89, 90, 91 .
Aprobación de la Administración de Alimentos y Fármacos de los Estados Unidos (FDA)
El uso del tamoxifeno fue aprobado por la FDA en el 1977 para el tratamiento del cáncer de mama. Subsecuentemente, el tamoxifeno fue aprobado como método preventivo de la recurrencia de tejidos cancerígenos que se extrajeron quirúrgicamente y del desarrollo del cáncer de mama en mujeres que tienen un alto riesgo.83 Asimismo, el uso del raloxifeno fue aprobado por la FDA para la prevenir y combatir el cáncer y la pérdida ósea (osteoporosis)92, 89 .
Vacunas
La prevención del cáncer es el objetivo principal de los investigadores y de los médicos del cáncer; esto se puede lograr mediante la prevención de aquellas infecciones con agentes (virus, bacterias y parásitos) que pueden causar el cáncer. Varias vacunas se han desarrollado y se han aprobado para su uso en la prevención de la infección con el virus de la hepatitis B (una causa de cáncer de hígado) y del papiloma humano (la principal causa de cáncer de cuello uterino y una causa de cáncer de cabeza/cuello y del tracto urogenital de hombres y mujeres). Obtenga más información sobre las vacunas aprobadas:
Vacuna contra el cáncer cervical
El desarrollo de la vacuna contra el VPH es un paso muy grande en la batalla contra el cáncer cérvico-uterino.
Hasta la fecha, existen dos vacunas que están aprobadas para prevenir el VPH: Gardasil® y Cervarix®.
La vacuna Gardasil® fue aprobado por la FDA para prevenir el VPH, particularmente sus subtipos 6, 11, 16 y 18, en mujeres entre los 9 y 26 años de edad. En el 16 de octubre del 2009 la FDA también aprobó Gardasil® para prevenir el crecimiento de quistes genitales ocacionado por el VPH 6 y 11 en hombres entre 9 y 26 años de edad.93, 94
La vacuna Cervarix® también previene las infecciones con el VPH 16 y 18. El uso del Cervarix® en los Estados Unicos fue aprobado en el mes de octubre del 2009.95
Tome en cuenta que las vacunas son profilácticas y no son efectivas en contra de la progresión de una infección por VPH preexistente o de una displasia cervical, y no quitan la necesidad de realizarse los exámenes anuales de detección, pues no todas las formas de VPH que causan cáncer (oncogénicas) están incluidas en vacunas. 95, 96
Vea el video si desea aprender más acerca de las vacunas contra el VPH. De clic aquí para ver la entrevista completa con el Dr. Ira Horowitz
Este tema ha sido cubierto con más detalle debido a los desarrollos recientes en este campo.
Se presume que la mayor parte de los casos de cáncer de cuello uterino son producto de una infección con el virus del papiloma humano (VPH). El VPH tiene más de 100 variantes (subtipos), sin embargo solamente una fracción de ellas está asociada con el cáncer humano. Por ejemplo, los subtipos 16 y 18 del VPH son las variantes que tienen más vínculos con el cáncer de cuello uterino humano. Varias características del VPH lo convierten en un buen enfoque en el desarrollo de vacunas, pues el virus es simple, pequeño y tiene un genoma estable. El desarrollo de la vacuna contra el VPH y los ensayos clínicos siguen en curso.
Gardasil®
La estrategia
Para reiterar, el propósito de las vacunas es aumentar la respuesta del sistema inmunológico a cualquier antígeno extraño que se detecte en el cuerpo. La idea es que si nuestro sistema inmunológico entra en contacto con un antígeno que ha detectado y eliminado en el pasado, reaccionará con mucha más fuerza. En el caso de los virus, el sistema inmunológico suele interactuar con las proteínas que se encuentran en el exterior de la partícula del virus.
Existe la posibilidad de elaborar agentes no contagiosos dentro del laboratorio que se parecen a los virus infecciosos pero que no se pueden replicar por su falta de ADN. Estos agentes contienen proteínas virales y son capaces de generar la misma respuesta inmunológica humoral al ser inyectados dentro del cuerpo. Actualmente, algunas vacunas contra el virus del papiloma humano que se basan en esta tecnología ya se están empleando, o se encuentran en las etapas avanzadas de desarrollo.
Los agentes:
Gardasil®
La primera vacuna preventiva contra el cáncer que obtuvo la aprobación de la FDA fue la Gardasil®. La Gardasil® se diseñó para prevenir la infección de cuatro subtipos del VPH (6, 11, 16, y 18). Los subtipos 6 y 11 representan 90% de las causas de los quistes genitales, mientras que los subtipos 16 y 18 son responsables del 70% de los casos de cáncer cérvicouterino. La vacuna Gardasil® contiene agentes parecidos al virus al poseer la proteína del cápside de cada uno de los cuatro subtipos del VPH.
La Gardasil® es producto de la farmacéutica Merck Pharmaceuticals. El uso de esta vacuna fue aprobado por la FDA el 8 de junio del 2006 para la prevención del cáncer cérvicouterino y de quistes genitales en mujeres entre 9 y 26 años de edad. Actualmente se investiga la eficacia de la Gardasil® dentro de otros rangos de edades y al combinarla con otras vacunas. El 16 de octubre del 2009 se aprobó el uso de la vacuna en hombres ente 9 y 26 años de edad.
Los datos
Después de haber rendido resultados positivos en las fases I y II de los ensayos clínicos, un total de 12167 mujeres entre 16 y 26 años de edad se inscribieron a la fase III del estudio en en 90 centros investigativos en Brasil, Colombia, Dinamarca, Finlandia, Islandia, México, Noruega, Perú, Polonia, Singapur, Suecia, el Reino Unido y en los Estados Unidos. De los más de 12.000 participantes, 6082 mujeres recibieron un régimen de tres dosis de Gardasil, mientras que las 6075 restantes recibieron un placebo. El estudio evaluó la aparición de cánceres no invasivos y pre-cancerígenos del cuello uterino asociados al VPH 16/18.
Específicamente, las participantes fueron examinadas para detectar la neoplasia intraepitelial cervical (NIC) de grado moderado (2) y alto (3). La NIC de grado 3 también se conoce como un carcinoma in situ (CIS). Un CIS es un precursor inmediato al cáncer cérvicouterino invasor de células escamosas. Las participantes también se sometieron a exámenes para determinar la presencia o ausencia del adenocarcinoma in situ (AIS), un precursor al cáncer cérvicouterino glandular. Los resultados de la prueba clínica demostraron que la vacuna Gardasil® previene el 100% de los pre-cánceres de grado alto y de los los cánceres no-invasivos asociados con el VPH 16/18. La Gardasil® también reduce el riesgo de desarrollar pre-cánceres de grado alto y de cánceres no-invasivos en mujeres que pudieron haber no seguido el protocolo o haber sido infectadas con el virus durante el período de las pruebas. El tratamiento recibió la aprobación por la FDA en el verano del 2006. 97, 98, 99, 95

En la mayoría de los casos, el sistema inmunológico elimina las infecciones con el VPH en su totalidad. Por ende, el cáncer no se desarrolla.

Si las infecciones duran mucho tiempo (varios años) el cáncer se puede desarrollar.

Las vacunas le dan una oportunidad al sistema inmunológico de prepararse, de tal modo de que si el virus logra entrar al cuerpo, se lo puede eliminar rápidamente. Esto previene la infección y la posibilidad de desarrollar el cáncer.
Gardasil 9®
Partiendo del éxito de la Gardasil® se creó una vacuna nueva para proteger al cuerpo humano de subtipos adicionales del virus del papiloma humano.
La Gardasil 9® cubre a 9 tipos del VPH, de los cuales 4 ya estaban incluidos dentro del enfoque de la Gardasil®, y 5 que no; estos subtipos adicionales del VPH son el 31, 33, 45, 52 y el 58, y son los patógenos responsables de un 20% de los casos de cáncer cervical. La Gardasil®9 se administra mediante tres inyecciones: dos meses después de la primera dosis se administra la segunda, y seis meses después de la primera dosis se administra la tercera.
Como parte de un estudio clínico realizado en los Estados Unidos y en otros países, casi 14000 participantes (mujeres entre las edades de 16 a 26) recibieron una dosis completa de Gardasil® o Gardasil®9. La investigación halló que la Gardasil®9 tenía una eficacia de un 97% en la prevención de las enfermedades que provienen del VPH 31, 33, 45, 52 y 58. También se reveló que esta nueva vacuna es igual de eficaz a la Gardasil® en la prevención de las enfermedades ocasionadas por el VPH 6, 11, 16 y 18. Algunos efectos secundarios de la vacuna incluyen al dolor en el lugar de inyección, hinchazón, enrojecimiento y dolor de cabeza.
La Gardasil®9 también es un producto de la farmacéutica Merck Pharmaceuticals. El 10 de diciembre del 2014 fue el día en el cual el uso de la Gardasil®9 en mujeres de 9 a 26 años de edad y en hombres de 9 a 15 años de edad se aprobó. En el 2016, un regímen de dos dosis en personas de 9 a 14 años de edad se aprobó100
Más acerca de la Gardasil® de parte de Merck
Busque ensayos clínicos con la Gardasil® en la página web del Instituto nacional de cáncer
Cervarix®
La farmacéutica Glaxo Smith Kline desarrolló una segunda vacuna contra el Virus del Papiloma Humano (VPH), cuya aprobación de parte de la FDA se otorgó en el mes de octubre del 2009 para su uso en mujeres entre 10 y 25 años de edad. 92 La Cervarix® está diseñada para proteger al cuerpo en contra de la infección del VPH 16 y 18. Estos dos subtipos representan la causa de 70% de los casos de cáncer cérvicouterino. Además de tener dos partículas que se asemejan a las que tiene el virus, la vacuna también contiene ciertos químicos (hidróxido de aluminio y lípido A monofosforilado (AS04)) que realzan la respuesta inmunológica a las proteínas virales.
La fase III del estudio doble ciego de con la Cervarix® (controlado con un placebo) se llevo a cabo con más de 1,100 mujeres entre las edades de 15 y 25 en Norteamérica y en Brasil. Las que recibieron Cervarix®, recibieron tres dosis de la vacuna durante un periodo de seis meses, semejante a cómo se administra la Gardasil®. Los resultados tras 27 meses de seguimiento demostraron una tasa de eficiencia de 92% contra infecciones nuevas y un 100% de protección en contra una infección persistente con el VPH. Los resultados también demostraron que el AS04 ayudaba a la vacuna a maximizar la respuesta inmunológica que ocurriría con una infección natural.101
En el 2016 se descontinuó la producción de la Cervarix®.
Busque estudios (ensayos) clínicos que están utilizando Cervarix® en el Instituto nacional del cáncer (NCI).
Cáncer de hígado (virus del hepatitis)
La infección crónica con el virus de la hepatitis es uno de los mayores factores de riesgo para el desarrollo de cáncer de hígado. Tanto el virus de la hepatitis B (HBV) como el virus de la hepatitis C (HCV) están asociados con el cáncer de hígado.102, 103 Globalmente, la infección con el virus de la hepatitis B es extremadamente común, con aproximadamente 240 millones de personas infectadas alrededor del mundo en el 2005.104
Una vacuna contra la hepatitis B se aprobó en 1981, convirtiéndola en la primera vacuna de prevención del cáncer.105 Hoy en día, los bebés estadounidenses reciben una vacuna de rutina contra la hepatitis B poco tiempo después de nacer. También se recomienda que los adultos se vacunen contra la hepatitis B.106, 107 Desafortunadamente, no existe una vacuna para prevenir la infección con el virus de la hepatitis C.
Tablas de prevención de cáncer
| Clasificación |
Químicos |
| Fármacos | AINEs, Tamoxifen, Raloxifen |
| Fitoquímicos | Antocianina, Curcumina, EGCG, Licopeno, Fitoestrógenos, Picnogenol, Resveratrol, Selenio, Vitamin E |
| Procesos biológicos afectados |
Químicos |
| Angiogénesis | Curcumina, EGCG, Resveratrol |
| Apoptosis | Antocianina, Curcumina, EGCG, Licopeno, Resveratrol, Selenio |
| Inflamación | Antocianina, Picnogenol, AINEs |
| Metástasis | Curcumina, AINEs, Vitamin E, Resveratrol |
| Oxidación (Antioxidantes) | Antocianina, Cúrcuma, EGCG, Licopeno, Fitoestrógenos, Picnogenol |
| Proliferación | Antocianina, Cúrcuma, AINEs, EGCG, Selenio, |
| Actividad enzimática | NSAIDs |
| Actividad hormonal | Tamoxifen, Raloxifene |
- 1 Littman AJ, Beresford SA, White E: The association of dietary fat and plant foods with endometrial cancer (United States). Cancer Causes Control 12 (8): 691-702, 2001 [PUBMED]
- 2 McCann SE, Freudenheim JL, Marshall JR, et al.: Diet in the epidemiology of endometrial cancer in western New York (United States). Cancer Causes Control 11 (10): 965-74, 2000. [PUBMED]
- 3 Howe GR, Benito E, Castelleto R, et al.: Dietary intake of fiber and decreased risk of cancers of the colon and rectum: evidence from the combined analysis of 13 case-control studies. J Natl Cancer Inst 84 (24): 1887-96, 1992. [PUBMED]
- 4 Morse DE, Pendrys DG, Katz RV, et al.: Food group intake and the risk of oral epithelial dysplasia in a United States population. Cancer Causes Control 11 (8): 713-20, 2000. [PUBMED]
- 5 Buiatti E, Palli D, Decarli A, et al.: A case-control study of gastric cancer and diet in Italy: II. Association with nutrients. Int J Cancer 45 (5): 896-901, 1990. [PUBMED]
- 6 Neuhouser ML, Patterson RE, Thornquist MD, et al.: Fruits and vegetables are associated with lower lung cancer risk only in the placebo arm of the beta-carotene and retinol efficacy trial (CARET). Cancer Epidemiol Biomarkers Prev 12 (4): 350-8, 2003. [PUBMED]
- 7 Fuchs CS, Giovannucci EL, Colditz GA, et al.: Dietary fiber and the risk of colorectal cancer and adenoma in women. N Engl J Med 340 (3): 169-76, 1999 [PUBMED]
- 8 Michels KB, Edward Giovannucci, Joshipura KJ, et al.: Prospective study of fruit and vegetable consumption and incidence of colon and rectal cancers. J Natl Cancer Inst (2000) 92(21): 1740-52. [PUBMED]
- 9 Jain MG, Rohan TE, Howe GR, et al.: A cohort study of nutritional factors and endometrial cancer. Eur J Epidemiol (2000) 16 (10): 899-905. [PUBMED]
- 10 Friedenreich CM: Physical activity and cancer prevention: from observational to intervention research. Cancer Epidemiol Biomarkers Prev 10 (4): 287-301, 2001. [PUBMED]
- 11 Schouten LJ, Goldbohm RA, van den Brandt PA: Anthropometry, physical activity, and endometrial cancer risk: results from the Netherlands Cohort Study. J Natl Cancer Inst 96 (21): 1635-8, 2004. [PUBMED]
- 12 Vainio H, Weiderpass E. Fruit and Vegetables in Cancer Prevention. Nutrition and Cancer. (2006) 54(1):111-42 [PUBMED]
- 13 Greenwald P, Anderson D, Nelson SA, Taylor PR. Clinical trials of vitamin and mineral supplements for cancer prevention. Am J Clin Nutr. (2007) 85(1):314S-317S. [PUBMED]
- 14 Boffetta P, Pershagen G, Jöckel KH, et al.: Cigar and pipe smoking and lung cancer risk: a multicenter study from Europe. J Natl Cancer Inst 91 (8): 697-701, 1999 [PUBMED]
- 15 Anthonisen NR, Skeans MA, Wise RA, et al.: The effects of a smoking cessation intervention on 14.5-year mortality: a randomized clinical trial. Ann Intern Med 142 (4): 233-9, 2005. [PUBMED]
- 16 Koh HK: The end of the "tobacco and cancer" century. J Natl Cancer Inst 91 (8): 660-1, 1999. [PUBMED]
- 17ab Morimoto LM, White E, Chen Z, et al.: Obesity, body size, and risk of postmenopausal breast cancer: the Women's Health Initiative (United States). Cancer Causes Control 13 (8): 741-51, 2002. [PUBMED]
- 18 Bagnardi V, Blangiardo M, La Vecchia C, et al.: Alcohol consumption and the risk of cancer: a meta-analysis. Alcohol Res Health 25 (4): 263-70, 2001 [PUBMED]
- 19 Purdie DM, Green AC: Epidemiology of endometrial cancer. Best Pract Res Clin Obstet Gynaecol 15 (3): 341-54, 2001 [PUBMED]
- 20 Bergström A, Pisani P, Tenet V, et al.: Overweight as an avoidable cause of cancer in Europe. Int J Cancer 91 (3): 421-30, 2001. [PUBMED]
- 21 Preston DS, Stern RS: Nonmelanoma cancers of the skin. N Engl J Med 327 (23): 1649-62, 1992 [PUBMED]
- 22 English DR, Armstrong BK, Kricker A, et al.: Case-control study of sun exposure and squamous cell carcinoma of the skin. Int J Cancer 77 (3): 347-53, 1998. [PUBMED]
- 23 Czene K, Lichtenstein P, Hemminki K. Environmental and heritable causes of cancer among 9.6 million individuals in the Swedish Family-Cancer Database. Int J Cancer 2002;99:260266 [PUBMED]
- 24 Lawrence H. Kushi, Tim Byers, Colleen Doyle, Elisa V. Bandera, Marji McCullough, Ted Gansler, Kimberly S. Andrews, Michael J. Thun and The American Cancer Society 2006 Nutrition and Physical Activity Guidelines Advisory Committee. CA Cancer J Clin (2006) 56; 254-281 [PUBMED]
- 25 World Health Organization. Cancer Fact Sheet No. 297. February 2006. Accessed 2 June 2010. [http://www.who.int/mediacentre/factsheets/fs297/en/index.html]
- 26 Calle EE, Rodriguez C, Walker-Thurmond K, Thun MJ. Overweight, obesity, and mortaily from cancer in a prospectively studied cohort of U.S. adults. N Engl J Med. (2003) 348: 1625-38 [PUBMED]
- 27 World Health Organization "Physical Activity" https://www.who.int/health-topics/physical-activity#tab=tab_1
- 28 Piercy, K., Troiano, R., Ballard, R., Carlson, S., Fulton, J., Galuska, D., … Olson, R. (2018). The Physical Activity Guidelines for Americans. JAMA, 320(19), 2020–2028. http://doi.org/10.1001/jama.2018.14854 (Original work published diciembre de 2018) [PUBMED]
- 29ab Idorn, M., & Straten, P. (2017). Exercise and cancer: from "healthy" to "therapeutic"? Cancer immunology, immunotherapy : CII, 66(5), 667–671. http://doi.org/10.1007/s00262-017-1985-z (Original work published mayo de 2017) [PUBMED]
- 30 de Rezende, L., de Sá, T., Markozannes, G., Rey-López, J., Lee, I.-M., Tsilidis, K., … Eluf-Neto, J. (2018). Physical activity and cancer: an umbrella review of the literature including 22 major anatomical sites and 770 000 cancer cases. British journal of sports medicine, 52(13), 826–833. http://doi.org/10.1136/bjsports-2017-098391 (Original work published julio de 2018) [PUBMED]
- 31 Keimling, M., Behrens, G., Schmid, D., Jochem, C., & Leitzmann, M. (2014). The association between physical activity and bladder cancer: systematic review and meta-analysis. British journal of cancer, 110(7), 1862–70. http://doi.org/10.1038/bjc.2014.77 (Original work published abril de 2014) [PUBMED]
- 32 Niehoff, N., Nichols, H., Zhao, S., White, A., & Sandler, D. (2019). Adult Physical Activity and Breast Cancer Risk in Women with a Family History of Breast Cancer. Cancer epidemiology, biomarkers & prevention : a publication of the American Association for Cancer Research, cosponsored by the American Society of Preventive Oncology, 28(1), 51–58. http://doi.org/10.1158/1055-9965.EPI-18-0674 (Original work published diciembre de 2019) [PUBMED]
- 33 Shaw, E., Farris, M., Stone, C., Derksen, J., Johnson, R., Hilsden, R., … Brenner, D. (2018). Effects of physical activity on colorectal cancer risk among family history and body mass index subgroups: a systematic review and meta-analysis. BMC cancer, 18(1), 71. http://doi.org/10.1186/s12885-017-3970-5 (Original work published diciembre de 2018) [PUBMED]
- 34 Voskuil, D., Monninkhof, E., Elias, S., Vlems, F., van Leeuwen, F., & Cancer, T. (2007). Physical activity and endometrial cancer risk, a systematic review of current evidence. Cancer epidemiology, biomarkers & prevention : a publication of the American Association for Cancer Research, cosponsored by the American Society of Preventive Oncology, 16(4), 639–48. (Original work published abril de 2007) [PUBMED]
- 35 Chen, Y., Yu, C., & Li, Y. (2014). Physical activity and risks of esophageal and gastric cancers: a meta-analysis. PloS one, 9(2), e88082. http://doi.org/10.1371/journal.pone.0088082 (Original work published diciembre de 2014) [PUBMED]
- 36 Behrens, G., & Leitzmann, M. (2013). The association between physical activity and renal cancer: systematic review and meta-analysis. British journal of cancer, 108(4), 798–811. http://doi.org/10.1038/bjc.2013.37 (Original work published marzo de 2013) [PUBMED]
- 37abc Campbell, K., & McTiernan, A. (2007). Exercise and biomarkers for cancer prevention studies. The Journal of nutrition, 137(1 Suppl), 161S-169S. http://doi.org/10.1093/jn/137.1.161S (Original work published diciembre de 2007) [PUBMED]
- 38ab Lee, D., de Rezende, L., Eluf-Neto, J., Wu, K., Tabung, F., & Giovannucci, E. (2019). Association of type and intensity of physical activity with plasma biomarkers of inflammation and insulin response. International journal of cancer, 145(2), 360–369. http://doi.org/10.1002/ijc.32111 (Original work published diciembre de 2019) [PUBMED]
- 39abc Betof, A., Dewhirst, M., & Jones, L. (2013). Effects and potential mechanisms of exercise training on cancer progression: a translational perspective. Brain, behavior, and immunity, 30 Suppl, S75–87. http://doi.org/10.1016/j.bbi.2012.05.001 (Original work published marzo de 2013) [PUBMED]
- 40 Pulliero, A., You, M., Chaluvally-Raghavan, P., Marengo, B., Domenicotti, C., Banelli, B., … Izzotti, A. (2020). Anticancer effect of physical activity is mediated by modulation of extracellular microRNA in blood. Oncotarget, 11(22), 2106–2119. http://doi.org/10.18632/oncotarget.27609 (Original work published junio de 2020) [PUBMED]
- 41 Assi, M., Dufresne, S., & Rébillard, A. (2020). Exercise shapes redox signaling in cancer. Redox biology, 35, 101439. http://doi.org/10.1016/j.redox.2020.101439 (Original work published diciembre de 2020) [PUBMED]
- 42 Saffer, H., Dave, D., Grossman, M., & Leung, L. (2013). Racial, Ethnic, and Gender Differences in Physical Activity. Journal of human capital, 7(4), 378–410. (Original work published diciembre de 2013) [PUBMED]
- 43 Hair, B., Hayes, S., Tse, C.-K., Bell, M., & Olshan, A. (2014). Racial differences in physical activity among breast cancer survivors: implications for breast cancer care. Cancer, 120(14), 2174–82. http://doi.org/10.1002/cncr.28630 (Original work published julio de 2014) [PUBMED]
- 44 Valcheva-Kuzmanova S.V., Belcheva A. Colon-available raspberry polyphenols exhibit anti-cancer effects on in vitro models of colon cancer. Journal of Carcinogenesis (2007) Apr 18; 6: 4 [PUBMED]
- 45 Lin Y.G., Kunnumakkara A., et al. Curcumin Inhibits Tumor Growth and Angiogenesis in Ovarian Carcinoma by targeting the Nuclear Factor-ºB Pathway. Clin Cancer Res 2007 13: 3423-3430 [PUBMED]
- 46 Yanase S, Yasuda K, Ishii N: Adaptive responses to oxidative damage in three mutants of Caenorhabditis elegans (age-1, mev-1 and daf-16) that affect life span. Mech Ageing Dev. (2002) 123:1579-1587 [PUBMED]
- 47 Missirlis F, Phillips JP, Jackle H: Cooperative action of antioxidant defense systems in Drosophila. Curr Biol. (2001) 11:1272-1277 [PUBMED]
- 48abc Halliwell, Barry. (May 3, 2005) Free radicals and other reactive species in disease. In: Encyclopedia of Life Sciences. John Wiley & Sons, Ltd: Chichester http://www.els.net/ [doi:10.1038/npg.els.0006101] [http://www.els.net/ [doi:10.1038/npg.els.0006101]]
- 49 Ramsey MR, Sharpless NE: ROS as a tumour suppressor? Nat Cell Biol. (2006) 8: 1213-1215 [PUBMED]
- 50 Irminger-Finger I. Science of cancer and aging. J Clin Oncol. 2007 May 10;25(14):1844-51 [PUBMED]
- 51ab Villarreal G, Zagorski J, Wahl Sm (January 29, 2003). Inflammation: Acute. In: ENCYCLOPEDIA OF LIFE SCIENCES. John Wiley & Sons, Ltd: Chichester [http://www.els.net/ [doi:10.1038/npg.els.0006101]]
- 52 Fox JG, Wang TC. Inflammation, atrophy and gastric cancer. J Clin Invest. (2007) 117: 60-9 [PUBMED]
- 53 Dobrovolskaia MA, Kozlov SV. Inflammation and cancer: when NF-ºB amalgamates the perilous partnership. Current Cancer Drug Targets. (2005) 5:325-44 [PUBMED]
- 54 de Visser KE, Eichten A, Coussens LM. Paradoxical roles of the immune system during cancer development. Nature Reviews. Cancer. (2006) 6: 24-37. [PUBMED]
- 55 MacDonald N. Cancer cachexia and targeting chronic inflammation: a unified approach to cancer treatment and palliative/supportive care. J Support Oncol. (2007) 5(4): 157-62 [PUBMED]
- 56ab Baron JA, Cole BF, Sandler RS, et al. A randomized trial of aspirin to prevent colorectal adenomas. N Engl J Med (2003) 348: 891-9. [PUBMED]
- 57ab Campbell CL, Smyth S, Nontalescot G, Steinhubl SR. Aspirin dose for the prevention of cardiovascular disease: a systematic review. JAMA. (2007) 297(18): 2018-24 [PUBMED]
- 58 Chan AT. Aspirin, non-steroidal anti-inflammatory drugs, and colorectal neoplasia: future challenges in chemoprevention. Cancer Causes Control (2003) 14: 413-8 [PUBMED]
- 59 Bertagnolli MM. Chemoprevention of colorectal cancer with cyclooxygenase-2 inhibitors: two steps forward, one step back. Lancet Oncol. (2007) May;8(5):439-43. [PUBMED]
- 60 Sandler RS, Halabi S, Baron JA, et al. A randomized trial of aspirin to prevent colorectal adenomas in patients with previous colorectal cancer. N Engl J Med (2003) 348: 883-90. [PUBMED]
- 61 Bertagnolli MM, Eagle CJ, Zauber AG, et al. Celecoxib for the prevention of sporadic colorectal adenomas. N Engl J Med (2006) 355: 873-84 [PUBMED]
- 62 Arber N, Eagle CJ, Spicak J, et al. Celecoxib for the prevention of colorectal adenomatous polyps. N Engl J Med (2006) 355: 885-95 [PUBMED]
- 63 Chan AT, Ogino S, Fuchs CS. Aspirin and the risk of colorectal cancer in relation to the expression of COX-2. N Engl J Med. (2007) 356(21): 2131-42. [PUBMED]
- 64 Couzin J. Drug Safety. FDA panel urges caution on many anti-inflammatory drugs. Science. (2005) 307(5713): 1183-5 [PUBMED]
- 65 Markowitz SD. Aspirin and colon cancer--targeting prevention? N Engl J Med. (2007) 356(21): 2195-8. [PUBMED]
- 66 Baron JA. Aspirin and cancer: trials and observational studies. J Natl Cancer Inst. 2012 Aug 22;104(16):1199-200. [PUBMED]
- 67 Omer ZB, Ananthakrishnan AN, Nattinger KJ, Cole EB, Lin JJ, Kong CY, Hur C. Aspirin Protects Against Barrett's Esophagus in a Multivariate Logistic Regression Analysis. Clin Gastroenterol Hepatol. 2012 Jul;10(7):722-7. Epub 2012 Mar 15. [PUBMED]
- 68 Bosetti C, Gallus S, La Vecchia C. Aspirin and cancer risk: a summary review to 2007. Recent Results Cancer Res. 2009;181:231-51. [PUBMED]
- 69 Cooper K, Squires H, Carroll C, Papaioannou D, Booth A, Logan RF, Maguire C, Hind D, Tappenden P. Chemoprevention of colorectal cancer: systematic review and economic evaluation. Health Technol Assess. 2010 Jun;14(32):1-206. [PUBMED]
- 70 Chan AT, Giovannucci EL, Meyerhardt JA, et al. Aspirin dose and duration of use and risk of colorectal cancer in men. Gastroenterology 2008;134:21¿28.
- 71 Chan AT, Giovannucci EL, Meyerhardt JA, et al. Long-term use of aspirin and nonsteroidal anti-inflammatory drugs and risk of colorectal cancer. JAMA 2005;294:914¿923.
- 72 Cook NR, Lee IM, Gaziano JM, et al. Low-dose aspirin in the primary prevention of cancer: the Women¿s Health Study: a randomized controlled trial. JAMA 2005;294:47¿55.
- 73 Gann PH, Manson JE, Glynn RJ, et al. Low-dose aspirin and incidence of colorectal tumors in a randomized trial. J Natl Cancer Inst 1993;85:1220¿1224.
- 74 Chan AT, Giovannucci EL. Primary prevention of colorectal cancer. Gastroenterology. 2010 Jun;138(6):2029-2043.e10. [PUBMED]
- 75 Brasky TM, Velicer CM, Kristal AR, Peters U, Potter JD, White E. Non-Steroidal Anti-Inflammatory Drugs and Prostate Cancer Risk in the VITamins And Lifestyle (VITAL) Cohort. Cancer Epidemiol Biomarkers Prev. 2010 Oct 8. [PUBMED]
- 76 Fowke JH, Motley SS, Smith JA Jr, Cookson MS, Concepcion R, Chang SS, Byerly S. Association of nonsteroidal anti-inflammatory drugs, prostate specific antigen and prostate volume. J Urol. 2009 May;181(5):2064-70 [PUBMED]
- 77abc Takkouche B, Regueira-Méndez C, Etminan M.Breast cancer and use of nonsteroidal anti-inflammatory drugs: a meta-analysis. J Natl Cancer Inst. 2008 Oct 15;100(20):1439-47. [PUBMED]
- 78 Zhao YS, Zhu S, Li XW, Wang F, Hu FL, Li DD, Zhang WC, Li X. Association between NSAIDs use and breast cancer risk: a systematic review and meta-analysis. Breast Cancer Res Treat. 2009 Sep;117(1):141-50. [PUBMED]
- 79 Bhattacharyya M, Girish GV, Ghosh R, Chakraborty S, Sinha AK. Acetyl salicyclic acid (aspirin) improves synthesis of maspin and lowers incidence of metastasis in breast cancer patients. Cancer Sci. 2010 Oct;101(10):2105-9. [PUBMED]
- 80 US Food and Drug Adminstration website. Accessed 6/20/2016. [http://www.fda.gov/]
- 81 Routine Aspirin or Nonsteroidal Anti-inflammatory Drugs for the Primary Prevention of Colorectal Cancer: U.S. Preventive Services Task Force Recommendation Statement. Annals of Internal Medicine. 2007 Mar;146(5):361-364. [http://www.uspreventiveservicestaskforce.org/uspstf/uspsasco.htm]
- 82 Jordan VC . Tamoxifen: a most unlikely pioneering medicine. Nat Rev Drug Discov. (2003) 2: 205-13 [PUBMED]
- 83abc Wozniak K, Kolacinska A, Blasinska-Morawiec M, Morawiec-Bajda A, Morawiec Z, Zadrozny M, Blasiak J. The DNA-damaging potential of tamoxifen in breast cancer and normal cells. Arch Toxicol. (2007) 81(7): 519-27 [PUBMED]
- 84ab Jordan VC. SERMs: meeting the promise of multifunctional medicines. J Natl Cancer Inst. (2007) 99(5): 350-6. [PUBMED]
- 85 Hu H, Jiang C, Ip C, Rustum YM, Lu J. Methylseleninic acid potentiates apoptosis induced by chemotherapeutic drugs in androgen-independent prostate cancer cells. Clinical Cancer Research (2005). 11: 2379-2388. [PUBMED]
- 86 Jordan, V. C., Allen, K. E. & Dix, C. J. Pharmacology of tamoxifen in laboratory animals. Cancer Treat. Rep. (1980) 64: 745-759. [PUBMED]
- 87 Poirier MC, Schild LJ. The genotoxicity of tamoxifen: extent and consequences. Mutagenesis. (2003) 18: 395399 [PUBMED]
- 88 Cuzick J, Forbes J, Edwards R, et al. First results from the International Breast Cancer Intervention Study (IBIS-I): a randomized prevention trial. Lancet. (2002) 360:81724. [PUBMED]
- 89ab Richardson H, Johnston D, Pater J, Goss P. The National Cancer Institute of Canada Clinical Trials Group MAP.3 trial: an international breast cancer prevention trial. Curr Oncol. (2007) 14(3): 89-96 [PUBMED]
- 90 Fisher B, Costantino JP, Wickerham DL, et al. Tamoxifen for prevention of breast cancer: report of the National Surgical Adjuvant Breast and Bowel Project P-1 Study. J Natl CancerInst (1998) 90: 1371-88 [PUBMED]
- 91 Vogel VG, Costantino JP, Wickerham DL, et al. Effects of tamoxifen vs raloxifene on the risk of developing invasive breast cancer and other disease outcomesthe NSABP study of tamoxifen and raloxifene (STAR) P-2 trial. JAMA. (2006) 295: 272741. [PUBMED]
- 92ab US Food and Drug Administration. FDA Approves raloxifene to prevent osteoporosis. U.S. Department of Health and Human Services. Dec 10, 1997. [http://www.fda.gov/bbs/topics/ANSWERS/ANS00838.html]
- 93 Markowitz LE, Dunne EF, Saraiya M, Lawson HW, Chesson H, Unger ER; Centers for Disease Control and Prevention (CDC); Advisory Committee on Immunization Practices (ACIP).Quadrivalent Human Papillomavirus Vaccine: Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2007 Mar 23;56(RR-2):1-24. [PUBMED]
- 94 U.S. Food and Drug Administration. News Release: FDA Approves New Indication for Gardasil to Prevent Genital Warts in Men and Boys. October 16, 2009. [http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm187003.htm]
- 95abc Food and Drug and Administration Vaccines, Blood, & Biologics Accessed October 21st, 2009 [http://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/ucm186991.htm]
- 96 Gardasil® Website Registered by Merck & Co., Inc. Site accessed 12/04/07 [http://www.gardasil.com/index.html]
- 97 Lowndes CM. "Vaccines for cervical cancer." Epidemiology and Infection. (2006) 134: 1-12. [PUBMED]
- 98 "Merck's investigational vaccine GARDASIL" prevented 100 percent of cervical pre-cancers and non-invasive cervical cancers associated with HPV types 16 and 18 in new clinical study." Merck website. Accessed 3 August 2006. [http://www.merck.com/newsroom/press_releases/research_and_development/2005_1006.html]
- 99 Schmiedeskamp, MR and DR Kockler. "Human Papillomavirus vaccines." 2006, The Annals of Pharmacotherapy 40(7):1344-52 [PUBMED]
- 100 FDA website https://www.fda.gov/biologicsbloodvaccines/vaccines/approvedproducts/ucm426445.htm Accessed 10-7-2017
- 101 Harper DM, et al. "Efficacy of a bivalent L1 virus-like particle vaccine in prevention of infection with human papillomavirus types 16 and 18 in young women: a randomized controlled trial." The Lancet (2004) Nov 13; 364:1757-65. [PUBMED]
- 102 El-Serag HB. Epidemiology of viral hepatitis and hepatocellular carcinoma. Gastroenterology. 2012 May;142(6):1264-1273.e1. [PUBMED]
- 103 Perz JF, Armstrong GL, Farrington LA, Hutin YJ, Bell BP. The contributions of hepatitis B virus and hepatitis C virus infections to cirrhosis and primary liver cancer worldwide. J Hepatol. 2006 Oct;45(4):529-38. Epub 2006 Jun 23. [PUBMED]
- 104 Vaccine. 2012 Mar 9;30(12):2212-9. Epub 2012 Jan 24. Global epidemiology of hepatitis B virus infection: new estimates of age-specific HBsAg seroprevalence and endemicity. Vaccine. 2012 Mar 9;30(12):2212-9. Epub 2012 Jan 24. [PUBMED]
- 105 Centers for Disease Control and Prevention. Epidemiology and Prevention of Vaccine-Preventable Diseases. Atkinson W, Wolfe S, Hamborsky J, eds. 12th ed. Washington DC: Public Health Foundation, 2011. http://www.cdc.gov/vaccines/pubs/pinkbook/downloads/hepb.pdf Accessed July 20, 2011. [http://www.cdc.gov/vaccines/pubs/pinkbook/downloads/hepb.pdf]
- 106 Mast EE, Margolis HS, Fiore AE, Brink EW, Goldstein ST, Wang SA, Moyer LA, Bell BP, Alter MJ; Advisory Committee on Immunization Practices (ACIP). A comprehensive immunization strategy to eliminate transmission of hepatitis B virus infection in the United States: recommendations of the Advisory Committee on Immunization Practices (ACIP) part 1: immunization of infants, children, and adolescents. MMWR Recomm Rep. 2005 Dec 23;54(RR-16):1-31. [PUBMED]
- 107 Mast EE, Weinbaum CM, Fiore AE, Alter MJ, Bell BP, Finelli L, Rodewald LE, Douglas JM Jr, Janssen RS, Ward JW; Advisory Committee on Immunization Practices (ACIP) Centers for Disease Control and Prevention (CDC). A comprehensive immunization strategy to eliminate transmission of hepatitis B virus infection in the United States: recommendations of the Advisory Committee on Immunization Practices (ACIP) Part II: immunization of adults. MMWR Recomm Rep. 2006 Dec 8;55(RR-16):1-33; quiz CE1-4. [PUBMED]