Como se describió (más brevemente) en la sección de Distintivos del Cáncer, la metástasis es responsable de la gran mayoría de las muertes en los pacientes de cáncer. Esta sección detalla los pasos por los cuales las células cancerosas se esparcen al rededor del cuerpo para formar nuevos tumores. Más información sobre los temas discutidos en esta página puede ser encontrada en mayoría de los textos introductorios de biología; nosotros recomendamos Campbell Biology, 11ma edición.1
- Generalidades de la metástasis
- Formación de la metástasis
- Rutas de la metástasis
- Cómo la metástasis forma nuevos tumores
- Barreras para la metástasis
- Drogas cuyo blanco es la metástasis
- Resumen de sección: MetástasisSection Summary: Metastasis
- Juego educacional: Conoce el Flujo: Metástasis
Generalidades de la metástasis
La mayoría de la mortalidad relacionada con el cáncer es a causa de la metástasis de las células tumorosas originales hacia sitios distantes del tumor inicial or primario. La metástasis es un proceso por el cual las células cancerosas migran a través del cuerpo.
Para que las células puedan moverse a través del cuerpo, éstas deben treparse sobre o alrededor de las células adyacentes. Hacen esto reestructurando su citoesqueleto y atándose a otras células y a la matriz extracelular por medio de proteínas en la superficie exterior de su membrana plasmática. Al extender una parte de la célula hacia adelante y soltando su extremidad posterior, las células pueden migrar hacia adelante. Las células pueden arrastrarse hasta que encuentren un bloqueo que no pueden pasar. Frecuentemente este bloqueo es una capa gruesa de proteínas y glicoproteínas llamada la lámina basal o la membrana basal que envuelve los tejidos. Para poder cruzar esta barrera, las células cancerosas secretan un grupo de enzimas digestivas que degradan la lámina basal y permite que las células continúen su migración.
Las proteinas secretadas por las células cancerosas contienen enzimas conocidos como metaloproteasa de la matriz (matrix metalloproteases o MMP por sus siglas en inglés). Estas enzimas actúan como tijeras moleculares para cortar a través de las proteínas que inhiben el movimiento de las células cancerosas migratorias. Una vez que han pasado a través de la lámina basal, pueden esparcirse a través del cuerpo de varias maneras. Pueden entran al torrente sanguíneo comprimiéndose entre las células que componen los vasos sanguíneos.
Una vez en el torrente sanguíneo, las células flotan a través del sistema circulatorio hasta que encuentran un lugar adecuado para posarse y entrar de nuevo a los tejidos. Entonces, las células pueden empezar a crecer en este lugar nuevo, formando un tumor.
El proceso de metástasis es muy ineficiente pero es la causa de la mayoría de las muertes asociadas con el cáncer. Esto es porque millones células se pueden separar de un tumor diariamente. Aunque solo una pequeña fracción de las células que se desprenden de un tumor tienen la habilidad sobrevivir y formar un nuevo tumor, el gran numero de intentos significa que un crecimiento a distancia es probable en algún momento.
Células cancerosas migratorias pueden morir por varias razones, incluyendo:
- Normalmente las células viven altamente conectadas a sus vecinos y la red de proteinas que las envuelven. El desprenderse de la superficie de otras células puede resultar en la muerte celular (conocida como anoikis).
- Frecuentemente las células cancerosas son muy grande comparadas con las células que normalmente viven en el sistema linfático o circulatorio. Cuando estas viajan a través de los vasos sanguíneos pueden lesionarse o atascarse, resultado así en la muerte celular.
- Las células del sistema inmunológico pueden reconocer y destruir las células.
Es importante notar que aunque una célula cancerosa no muera, esto no significa que definitivamente va a formar un tumor. Las células pueden existir lejos del tumor original sin multiplicarse lo suficiente como para causar algún problema.
Este video demuestra el proceso de metástasis.
Mira cómo el investigador Adam Marcus del Emory Winship Cancer Institute describe su investigación sobre la metástasis del cáncer. Contiene un video del movimiento celular en tiempo real.
Formación de la metástasis
Formación de Colonias
Para que una célula tumoral metastática se exitosa, necesita establecer nuevas colonias para crear un tumor secundario. Para formar una colonia viable, necesita crear un lugar dentro de un ambiente hostil y extraño. La formación de colonias aparece ser el paso clave en el proceso de metástasis. En un modelo experimental de melanoma metastático, más de un 80% de las células cancerosas inyectadas sobrevivieron en la circulación y salieron a través del hígado. De estas, solo 1 célula en 40 formó micrometástasis en un período de 3 días, y de estas sólo 1 célula de cada 100 formó macrometástasis. Crear un ambiente adecuado parece ser un proceso difícil que limita la habilidad de una célula metastásica para formar un tumor secundario.2
Obstáculos para la Fromación de Colonias
¿Qué hace de la formación de nuevas colonias un paso tan ineficiente? El estroma (tejido adyacente) del órgano nuevo va a ser muy diferente al del lugar original, y en la mayoría de los casos, va a ser inhóspito a la supervivencia celular tumoral. Si la célula metastática no puede convertir al nuevo estroma a un ambiente más hospitalario, no va a poder colonizar exitosamente al nuevo lugar (por ejemplo, promover suficiente angiogénesis), y no podrá formarse un tumor secundario.3 En estos casos las células tumorales se dicen estar latentes: no se mueren, pero son incapaces de crecer. El adquirir mutaciones adicionales frecuentemente permite que estas micrometástasis latentes superar las dificultades que enfrentan en nuevos tejidos y entonces pueden colonizarlos exitosamente, formando así un verdadero tumor metastático. 4
Rutas de la metástasis
Rutas de Metástasis
Existen tres rutas de diseminación tumoral a órganos distantes:
- Hematógena (circulación sanguínea)
- Sistema linfático
- Transcelómica (a través de la pared corporal a las cavidades abdominales y en el pecho).
El sistema circulatorio es la ruta primaria de diseminación a órganos lejanos. Los vasos linfáticos proveen una ruta a los ganglios linfáticos locales, y frecuentemente después las metástasis se diseminan a través de la sangre.3 Mientras que la diseminación a través de la sangre parece ser la más común, la extensión de diseminación linfática versus hematógena aparece depender del origen y la ubicación del tumor primario.5 Por ejemplo, tumores de hueso y tejidos blandos (sarcomas) se diseminan primariamente a través de la sangre, mientras que los tumores de melanoma, mama, pulmón, y gastrointestinales se riegan principalmente a través del sistema linfático.6 La diseminación transcelómica es poco común y aparece estar limitada a los mesoteliomas y a los carcinomas ováricos.7
Para que las células tumorales puedan adquirir acceso a los vasos linfáticos o sanguíneos, los tumores necesitan promover el crecimiento de estos vasos dentro de y alrededor del tumor. Al crecimiento de vasos sanguíneos se le conoce como angiogénesis, y al crecimiento de los vasos linfáticos se le conoce como linfangiongénesis.
Aprenda más sobre la angiogénesis
El Sistema Linfático
El sistema linfático juega un papel importante en el control del movimiento de fluidos a través del cuerpo. Específicamente el sistema linfático controla el flujo de la linfa, un fluido incoloro que contiene oxígeno, proteínas, azúcar (glucosa) y linfocitos (cito=célula). Hay algunas similaridades entre el sistema circulatorio y el sistema linfático.
Los pequeños vasos linfáticos se unen en vasos más grandes y estos a su vez se terminan eventualmente en nódulos linfáticos. Los nódulos linfáticos son tejidos con forma de riñon-frijol y se encuentran en agrupaciones similares a un racimo de uvas ubicados por todo el cuerpo. Los nódulos linfáticos son donde se realiza la activación del sistema inmune y la proliferación celular. El fluido en esta extensa red fluye a través del cuerpo, muy simila al torrente sanguíneo. Es el movimiento de las células cancerosas al sistema linfático, específicamente a los nódulos linfáticos, lo que se usa para detectar la metástasis. Las etapas del cáncer se comentan con más detalle en la sección de Diagnóstico y Detección.
Esparcimiento del Cáncer a través del Sistema Linfático
Cuando una célula cancerosa se han movido a través del sistema circulatorio sanguíneo o linfático o a través de contacto directo a otra ubicación, esta puede dividirse y formar un tumor en el nuevo lugar. Los tumores metastásicos a veces infertieren con las funciones de los órganos que invaden y llevan a la morbilidad y mortandad vista en el cáncer.
El sistema linfático tiene un papel crucial en la metástasis de ciertos cánceres. Los vasos linfáticos están diseñados para la entrada y salida de células inmunológicas, y por lo tanto es facil que las células tumorales entren. Adicionalmente, el flujo del sistema linfático es lento, por lo que existe menos estrés que dañe las células.6 Los investigadores creían originalmente que las células tumorales invadían el sistema linfático a través de la erosion los vasos linfáticos conforme el tumor avanzaba y que la metástasis ocurriría por drenado pasivo. Sin embargo, la evidencia actual sugiere que las interacciones entre las células metastásicas y los vasos linfáticos es mucho más activa y compleja, y se ha sugerido que interacciones específicas entre ambas son requeridas.
La presencia de metastasis en los nódulos linfáticos cerca del tumor primario a menudo indica metástasis a organos distantes, y es un indicador significativo para el pronóstico en muchos cánceres. Para determinar la presencia de metástasis a nódulos linfáticos circundantes, los médicos realiaban una biopsia al nódulo linfático. En este procedimiento, los nódulos se remueven con cirujía y son revisados para buscar la presencia de células cancerosas. Los nódulos pueden ser determinados como positivos o negativos para cáncer.
Debido a que las rutas de drenado de un tumor varian mucho de un paciente a otro, incluso en la misma área, hasta el 30% de los tumores no se les puede predecir una migración a un nódulo linfático específico. Mejoras en la imagenología y mapeo del sistema linfático son requeridos para asegurar que cánceres en metastásis no sean pasados por alto.8
Aprenda más sobre el sistema linfático
Aprenda más sobre la biopsia de nódulos linfáticos
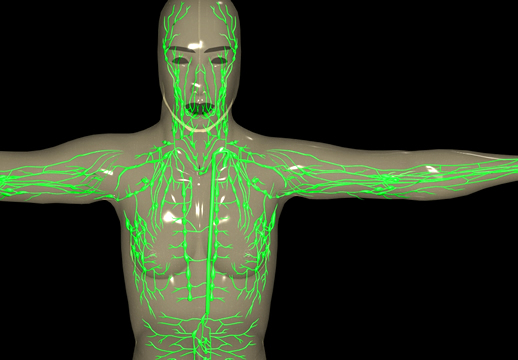
El diagrama debajo muestra el sistema linfático.
En el modelo anatómico de metástasis, los tumores secundarios ocurren en órganos que encuentran primero durante su diseminación del tumor primario. Esto ocurre en el caso de metástasis regionales donde las células tumorales consiguen acceso a tejidos cercanos o a ganglios linfáticos a través del torrente sanguíneo o la circulación linfática.9 Por ejemplo, las metástasis al hígado son algo común en los pacientes con cáncer colorectal. En este caso, la cama de capilares del hígado es lo primero que encuentran las células tumorales al salir del colon, y el hígado parece proveer un medio ambiente apropiado para el crecimiento de estos tumores secundarios.2 Sin embargo, la metástasis a órganos lejanos ocurre a través de otro mecanismo (vea la próxima sección).
La Hipótesis de la Semilla y la Tierra Fértil
Los primeros investigadores del cáncer notaron la propensión de ciertos tipos de cánceres a metastizar al mismo órgano. En el 1889, Stephen Paget observó que pacientes con cáncer de mama frecuentemente desarrollaban tumores secundarios en el hígado. El consideraba poco probable que esto se debía principalmente a la accesibilidad al hígado a través del torrente sanguíneo, como otros órganos que recibían un suministro de sangre equivalente rara vez desarrollaban metástasis. En vez, desarrolló la hipótesis de Semilla y Tierra Fértil, en la cual ciertas células tumorales (las semillas) solo pueden colonizar ciertos órganos específicos que tienen el medio ambiente apropiado para su crecimiento (la tierra fértil).10
La opinión actual de la Hipótesis de la Semilla y la Tierra Fértil consiste de tres conceptos importantes.
- Los tumores primarios y sus metástasis consisten de células tumorales y huéspedes genéticamente diversas (para más sobre el papel de las células huésped en el cáncer, refiérase a la sección sobre El Microambiente Tumoral).
- La metástasis elige células que pueden triunfar en todas las fases del proceso de metástasis. Esencialmente, una célula metastática triunfante debe de ser como un decatleta: bueno en todos los eventos, no solo en uno o dos.
- Generalmente las metástasis se desarrollan de cierta manera específica. Como el microambiente de cada órgano es distinto (la tierra fértil), puede que células cancerosas individuales puedan colonizar un órgano en específico.9
En el centro de la hipóesis de la Semilla y la Tierra Fértil está la idea de que la metástasis exitosa depende de la interacción de las células tumorales de metástasis con las células del órgano blanco (el estroma, o el microambiente tumoral). Las células tumorales tienen que producir factores que alteran las células del estroma de tal manera que le sirvan a la supervivencia y al crecimiento tumoral, y además, el medio ambiente en el cual se encuentra la célula cancerosa debe de ser capaz de responder a esas señales. Si la célula cancerosa se encuentra en in medioambiente inhóspito, (por ejemplo, no puede cambiar al estroma a que sirva sus necesidades), será imposible el efectuar una metástasis exitosa.3
Estudios recientes, examinando el perfil genético expresado en tumores que logran metastizar a ciertos órganos en específico, han logrado identificar ciertas firmas genéticas de estos tumores. Por ejemplo, los genes que median la metástasis del cáncer de mama al hueso son distintos a los que median la metástasis al pulmón. Esencialmente, diferentes grupos de genes permiten que las células tumorales interactúen con las células del estroma del órgano blanco. Esto podría llevar al desarrollo de estrategias terapéuticas dirigidas a las propiedades metastáticas de los tumores.11
Cómo la metástasis forma nuevos tumores
Formación de Colonias
Para que una célula tumoral metastática se exitosa, necesita establecer nuevas colonias para crear un tumor secundario. Para formar una colonia viable, necesita crear un lugar dentro de un ambiente hostil y extraño. La formación de colonias aparece ser el paso clave en el proceso de metástasis. En un modelo experimental de melanoma metastático, más de un 80% de las células cancerosas inyectadas sobrevivieron en la circulación y salieron a través del hígado. De estas, solo 1 célula en 40 formó micrometástasis en un período de 3 días, y de estas sólo 1 célula de cada 100 formó macrometástasis. Crear un ambiente adecuado parece ser un proceso difícil que limita la habilidad de una célula metastásica para formar un tumor secundario.2
Obstáculos para la Fromación de Colonias
¿Qué hace de la formación de nuevas colonias un paso tan ineficiente? El estroma (tejido adyacente) del órgano nuevo va a ser muy diferente al del lugar original, y en la mayoría de los casos, va a ser inhóspito a la supervivencia celular tumoral. Si la célula metastática no puede convertir al nuevo estroma a un ambiente más hospitalario, no va a poder colonizar exitosamente al nuevo lugar (por ejemplo, promover suficiente angiogénesis), y no podrá formarse un tumor secundario.3 En estos casos las células tumorales se dicen estar latentes: no se mueren, pero son incapaces de crecer. El adquirir mutaciones adicionales frecuentemente permite que estas micrometástasis latentes superar las dificultades que enfrentan en nuevos tejidos y entonces pueden colonizarlos exitosamente, formando así un verdadero tumor metastático. 4
Barreras para la metástasis
En algunos casos las células provenientes de un tumor invaden un tejido "foráneo", pero no lo logran colonizar. ¿Qué causa la incapacidad de estas células de poder hacer tumores secundarios? Estas pueden no ser capaces de promover suficiente angiogénesis, o puede ser que no se reproducen, en cualquier caso puede ser la falta de las interacciones apropiadas entre el tumor y su nuevo ambiente. Mutaciones adicionales parecen ser necesarias cuando se requiere que estas células sobrepasen este tipo de dificultades en tejidos nuevos.4
La disección de las interacciones del tumor y su entorno es muy desafiante. El gran número de factores de crecimiento, citoquinas y factores presentes, así como las muchas vías de señalización implicadas en la intercomunicación entre estas dos entidades hace a los mecanismos difíciles de desentrañar, y casi cualquier resultado es aparentemente posible. Sin embargo, la importancia del microambiente del tumor es ya muy evidente, y cuanto más se aprende de ello, un mayor número de estrategias terapéuticas dirigidas al medio ambiente solo o en combinación con el tumor en sí estarán disponibles.
Aprenda más sobre las interacciones tumor-huésped.
Drogas cuyo blanco es la metástasis
Los Supresores de Metástasis
Recientes investigaciones han encontrado un grupo de moléculas que actúan para inducir o suprimir la metástasis sin afectar el crecimiento del tumor primario.Ttales moléculas, llamadas Supresores de Metástasis, han sido identificadas. Estas moléculas son críticas para las diferentes etapas de metástasis, y pueden funcionar para inhibir la muerte celular al perder la adhesión celular, o aumentar la habilidad de las células a migrar a través del estroma. Los investigadores tienen la esperanza de que estas moléculas prueben ser valiosas como blancos contra el cáncer o contra las metástasis.12
Es importante el darse cuenta de que la mayoría de los actuales estudios de fármacos contra el cáncer están hechos usando células de tumor primario. La eficacia de cada fármaco se mide a través de su habilidad de reducir el tamaño del tumor primario. Sin embargo, como los supresores de metástasis no afectan el crecimiento del tumor primario, es probable que muchos fármacos contra metástasis han sido pasados por alto. Nuevos métodos de analizar la habilidad de un fármaco de inhibir metástasis están siendo desarrolladas y podrían resultar en una nueva clase de compuestos terapéuticos.2
Terapia antiangiogénica
Como la metástasis depende de: el crecimiento de nuevos vasos sanguíneos en ambos, el tumor primario y secundario, los fármacos que inhiban la angiogénesis pueden inhibir la metástasis. Actualmente, la combinación de fármacos contra la angiogénesis con la quimioterapia/radiación es el tratamiento más efectivo. Desafortunadamente, muchos tumores se vuelven resistentes al tratamiento antiangiogénico, así que generalmente, esto no es una solución a largo plazo. 4
Investigaciones actuales sobre la inhibición de metástasis están enfocadas en entender cual paso en el proceso de metástasis es más susceptible a la terapia. La identificación de genes supresores de metástasis ha abierto muchos nuevos potenciales blancos para prevenir e inhibir este mortal evento.
Retos para el Desarrollo de Fármacos Anti-Metastásicos
Encontrar fármacos potenciales que bloqueen el proceso de metástasis es complicado, pero testear dichos fármacos en humanos es aun más difícil. La mayoría de ensayos clínicos son diseñados para descubrir si los fármacos destruyen a las células cancerosas o previenen el crecimiento tumoral. Un fármaco que previene la metástasis podría no mostrar una o ninguna de estas dos actividades. Algunos investigadores sienten que es importante idealizar nuevos métodos de ensayos clínicos que podrían enfocarse específicamente en la habilidad de los fármacos para prevenir la propagación del tumor.13
Resumen de sección: MetástasisSection Summary: Metastasis
Metástasis
- La metástasis es el proceso por el cual el cáncer se propaga a diferentes lugares del cuerpo humano.
- La mayor parte de las muertes asociadas con el cáncer se debe a la metástasis del tumor original.
- La células con cáncer tienen que secretar una mezcla de enzimas digestivas para poder degradar ciertas barreras.
- Las células cancerígenas pueden usar el sistema circulatorio para moverse a una mejor ubicación para desarrollarse.
- La metástasis es un proceso bastante ineficiente. La mayor parte de las células mueren cuando estas salen del tumor original.
Metástasis Linfática
- El cáncer puede usar el sistema linfático así como el sistema circulatorio para hacer metástasis
- El movimiento de las células cancerígenas vía el sistema linfático en los nódulos linfáticos se utiliza para la detección de una metástasis.
Algunos cánceres se pueden propagar a través del contacto directo con otros órganos. Los tumores metastásicos suelen interferir con las funciones de los órganos afectados.
Prueba tu conocimiento de cómo el cáncer se esparce con este juego educacional:
Conoce el Flujo: Metástasis
Conoce el Flujo es un juego interactivo para poner a prueba su conocimiento del tema. Para jugar:
- Mueva las respuestas adecuadas de la columna a la derecha y póngalas en orden en las cajas que están a la izquierda. Fíjese que solo usara cinco de las seis opciones para completar el juego.
- Cuando termine, haga click en "Check" para ver cuantas de sus respuestas son correctas.
- Para ver las respuestas incorrectas, haga clic a la "Description2 para repasar la información sobre los procesos.
- Para intentar de nuevo, seleccione "Reset"y empieze de nuevo.
Please visit us on a larger screen to play this game.
- 1 Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11th ed.). Pearson.
- 2abcd Steeg, P.S. 2006. Tumor metastasis: mechanistic insights and clinical challenges. Nat Med. 12:895-904. [PUBMED]
- 3abcd Bacac, M., and I. Stamenkovic. 2008. Metastatic cancer cell. Annu Rev Pathol. 3:221-47. [PUBMED]
- 4abcd Gupta, G.P., and J. Massague. 2006. Cancer metastasis: building a framework. Cell. 127:679-95. [PUBMED]
- 5 Gerhardt, H., and H. Semb. 2008. Pericytes: gatekeepers in tumour cell metastasis? J Mol Med. 86:135-44. [PUBMED]
- 6ab Kopfstein, L., and G. Christofori. 2006. Metastasis: cell-autonomous mechanisms versus contributions by the tumor microenvironment. Cell Mol Life Sci. 63:449-68. [PUBMED]
- 7 Tan DS, Agarwal R, Kaye SB. Mechanisms of transcoelomic metastasis in ovarian cancer. Lancet Oncol. 2006 Nov;7(11):925-34. [PUBMED]
- 8 Shayan, R., M.G. Achen, and S.A. Stacker. 2006. Lymphatic vessels in cancer metastasis: bridging the gaps. Carcinogenesis. 27:1729-38. [PUBMED]
- 9ab Fidler, I.J. 2003. The pathogenesis of cancer metastasis: the 'seed and soil' hypothesis revisited. Nat Rev Cancer. 3:453-8. [PUBMED]
- 10 Paget, S. 1889. The distribution of secondary growths in cancer of the breast. The Lancet. 1:571-573. [PUBMED]
- 11 Minn, A.J., G.P. Gupta, P.M. Siegel, P.D. Bos, W. Shu, D.D. Giri, A. Viale, A.B. Olshen, W.L. Gerald, and J. Massague. 2005. Genes that mediate breast cancer metastasis to lung. Nature. 436:518-24. [PUBMED]
- 12 Stafford, L.J., K.S. Vaidya, and D.R. Welch. 2008. Metastasis suppressors genes in cancer. Int J Biochem Cell Biol. 40:874-91. [PUBMED]
- 13 ACS 2014 Kidney Cancer Detailed Guide [http://www.cancerquest.org/sites/default/files/assets/pdf/Kidney/kidney-cancer-detailed-guide-acs.pdf]
