Introducción: Metabolismo de una Célula Normal
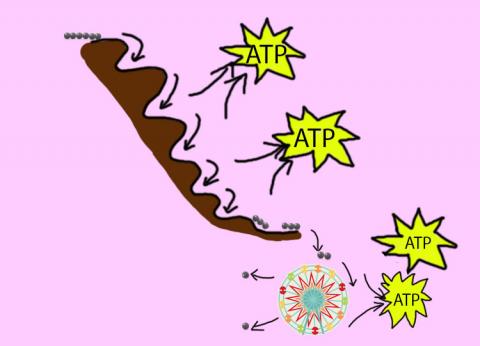
Respiración celular describe la serie de pasos que las células usan para descomponer azúcares y químicos para extraer la energía que necesitamos para funcionar. La energía se almacena en los enlaces de glucosa (como una banda elástica), y cuando descomponemos glucosa, esa energía se suelta. Parte de esta energía se captura de forma que las células puedan usarla - una molécula llamada trifosfato de adenosina (ATP). La energía que no es capturada en ATP se gasta en calor.
El proceso de respiración celular es similar a un carro que usa gasolina. Al igual que la gasolina es combustible para el carro, glucosa es combustible para la célula. Un carro quema gasolina y usa la energía para moverse. Similarmente, las células 'queman' glucosa para capturar la energía y crear ATP. ATP es la forma de energía primaria que las células usan para funcionar.
El primer paso de respiración celular es glucólisis. En una serie de pasos, glucólisis descompone glucosa en dos moléculas pequeñas - llamadas piruvato. Un poco de ATP se forma en este proceso.
La mayoría de las células saludables continúan la descomposición en un segundo proceso, llamado el ciclo de Kreb. El ciclo de Kreb permite que las células 'quemen' los piruvatos hechos en glucólisis para sacar más ATP.
La última etapa en la descomposición de glucosa se llama fosforilación oxidativa. Esto ocurre en unas estructuras celulares especializadas llamadas mitocóndrias. Este proceso produce cantidades enormes de ATP. Es importante notar que las células necesitan oxígeno para completar la fosforilación oxidativa. Si una célula solo completa glucólisis, solo genera 2 moléculas de ATP por cada glucosa. Sin embargo, si la célula completa el proceso entero (glucólisis, Kreb, fosforilación oxidativa), se generan alrededor de 36 moléculas de ATP. Más información en estos temas se puede encontrar en la mayoría de los textos introductorios de biología, nosotros recomendamos Campbell Biology, 11th edition.1
Temas a ser Discutidos en esta Página:
- Lo que las Células Cancerosas Hacen Diferente
- Hipoxia y el Ambiente Tumoral
- Cambios Genéticos y Metabolismo de una Células Cancerosa
- Metabolismo en Detección Tumoral y Tratamiento
¿Qué Hacen Diferente Las Células Cancerosas?
Diferente a las células saludables que "queman" la molécula entera de azúcar para capturar cantidades grandes de energía, las células cancerosas desperdician mucho. Las células cancerosas solo rompen la molécula parcialmente. Repiten mucho la primera etapa de respiración celular: glucólisis. Muy frecuentemente no completan el segundo paso, fosforilación oxidativa. Esto resulta en solo dos moléculas de ATP por glucosa en vez de las ~36 que se producen en una célula normal. Como resultado, las células cancerosas necesitan usar muchas más moléculas de azúcar para obtener la energía necesaria para sobrevivir.2
Otto Warbug, un científico alemán, fue el primero en describir este comportamiento inusual de las células cancerosas. Ganó el premio Nobel en 1931 por su trabajo. Se dio cuenta que las células cancerosas solo completan glucólisis (no fosforilación oxidativa), aún cuando hay oxígeno presente. La presencia de oxígeno debe permitirlas a completar el proceso entero de respiración celular. La dependencia anormal de glucólisis como fuente única de ATP, aún en la presencia de oxígeno, se le conoce como el "efecto Warburg".3
Puede que algunas células cancerosas no puedan completar el proceso entero de respiración celular a causa de cambios de su ADN (mutaciones), pero eso no es el cuento completo. Usar solo glucólisis le provee una ventaja a las células cancerosas. Los productos de glucólisis (ácido bicarbónico y ácido láctico) pueden ser usados para construir productos que ayudan a las células cancerosas a sobrevivir.
Investigaciones también han sugerido que usar solo glucólisis puede ayudar a las células cancerosas a no ser reconocidas por el sistema inmune.2 Cambios en el ambiente metabólico pueden detener a las células inmunes de encontrar el cáncer y hasta pueden atraer a más células que ayuden al tumor a crecer. Los cambios metabólicos inusuales vistos en células cancerosas también pueden activar oncogenes que ayudan a las células cancerosas evitar la muerte.
Hipoxia y el Ambiente Tumoral
El ambiente dentro de un tumor está lleno de tensión para las células normales que viven ahí. Los vasos sanguíneos en un tumor no están desarrollados propiamente y a veces están virados y torcidos. Las estructuras defectivas resultan en una habilidad reducida de entregar el oxígeno y resulta en el desarrollo de condiciones acídicas. Otro resultado de la distribución de los vasos sanguíneos distorcionados es que algunas partes del tumor están lejos de los vasos y no reciben suficientes nutrientes y oxígeno.4 Eventualmente, los tumores crecen tanto que su provisión de sangre no es suficiente. Esto resulta en que el área dentro del tumor se convierte hipóxico (le falta oxígeno). Las células que solo usan glucólisis no son dependientes de oxígeno para sobrevivir. Por esta razón las células cancerosas pueden sobrevivir en áreas de poco oxígeno.
En respuesta a las condiciones hipóxicas (hipoxia), una proteína llamada subunidad alfa del factor 1 inducible por hipoxia (HIF1-α) es activada. La proteína HIF1-α incrementa el ritmo de glucólisis y reduce la conversión de glucosa a los productos vistos en células normales.5 Hipoxia y la activación de HIF1-α causan problemas. Poco oxígeno ayuda a promover movimiento celular y el esparsimiento de cáncer (metástasis) al causar la producción de TWIST, una proteína que juega un rol esencial en metástasis. Activación de TWIST resulta en que las células cancerosas se suelten de su ambiente, permitiendo que se muevan e invadan a los tejidos cercanos. El proceso por el cual las células epiteliales se cambian a un tipo de células que se pueda mover más fácil se conoce como transición epitelio-mesenquimal (EMT). Además de la habilidad de moverse, EMT le da a las células capacidades primitivas adicionales que ayuda a proteger a las células cancerosas.6
Cambios Genéticos y Metabolismo de las Células Cancerosas
Muchos cambios de ADN (mutaciones) ocurren en células cancerosas, pero no están presentes en células normales. Algunos de estos cambios pueden resultar en glucólisis incrementado. AKT, un oncogén envuelto en el metabolismo y supervivencia de las células cancerosas, puede ser activado en respuesta a hipoxia y HIF1-α. Esto puede llevar a mayor supervivencia de las células cancerosas.5 Otros oncogenes, RAS y MYC, son activados frecuentemente en células cancerosas. Sus proteínas ambas contribuyen a glucólisis aerobico visto en células cancerosas.7
En células cancerosas, los supresores de tumores que detienen el crecimiento celular canceroso frecuentemente son desactivados. La pérdida del supresor de tumores p53 puede provocar el efecto Warburg y las células se convierten "adictas" a glucólisis.4
Glucólisis aerobico también está atado a la producción/actividad de otra proteína, el factor de crecimiento derivado del endotelio vascular (VEGF). VEGF causa la formación de vasos sanguíneos (angiogénesis). Los tumores necesitan crear nuevos vasos sanguíneos para mantener un suministro de nutrientes mientras crecen. El metabolismo anormal visto en células cancerosas puede causar la creación de estos vasos sanguíneos.8
Metabolismo en Detección y Tratamiento de Tumores
Como mencionado anteriormente, las células cancerosas frecuentemente utilizan el glucólisis aeróbico, una manera muy ineficiente de obtener ATP. Entonces, las células cancerosas tienen que usar mucha más glucosa para generar suficiente ATP para sobrevivir. La tomografía de emisión de positrones (PET) es un método de detección que aprovecha esta situación para detectar cáncer. En los escaneos PET, a los pacientes se le inyecta con un químico, fluorodeoxiglucosa (FDG) que es muy similar a la glucosa. La presencia de FDG en tejidos puede ser detectado por máquinas PET. Los tumores demuestran un consumo aumentado de glucosa y FDG en comparación a tejidos normales. Los escaneos PET pueden ser usados para etapificar los tumores, asesar las respuestas a los tratamientos, predicar la agresividad del tumor y ayudar a formular un prognosis. 9
Metabolismo de las células de cáncer también puede proveer pistas para objetivos posibles de tratamiento. Dicloroacetato (DCA) es un químico que está siendo investigado por su habilidad a reactivar fosforilación oxidativaen células tumorales y reprimir su crecimiento.10 Ensayos clínicos también están examinando el uso de medicamentos que detengan glucólisis.

- 1 Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11th ed.). Pearson.
- 2ab Kroemer G, Pouyssegur J. Tumor cell metabolism: cancer's Achilles' heel. Cancer Cell. 2008 Jun;13(6):472-82. [PUBMED]
- 3 Warburg, O. On the origin of cancer cells. Science. 1956 Feb 24;123(3191):309-14. [PUBMED]
- 4ab Denko NC. Hypoxia, HIF1 and glucose metabolism in the solid tumour. Nat Rev Cancer. 2008 Sep;8(9):705-13. [PUBMED]
- 5ab Kaelin WG Jr, Thompson CB. Q&A: Cancer: clues from cell metabolism. Nature. 2010 Jun 3;465(7298):562-4. [PUBMED]
- 6 Wu KJ, Yang MH. Epithelial-mesenchymal transition and cancer stemness: the Twist1-Bmi1 connection. Biosci Rep. 2011 Dec;31(6):449-55. [PUBMED]
- 7 Singleterry J, Sreedhar A, Zhao Y. Components of cancer metabolism and therapeutic interventions. Mitochondrion. 2014 Jul;17:50-5. [PUBMED]
- 8 Hsu PP, Sabatini DM. Cancer cell metabolism: Warburg and beyond. Cell. 2008 Sep 5;134(5):703-7. [PUBMED]
- 9 Mankoff DA, Bellon JR. Positron-emission tomographic imaging of cancer: glucose metabolism and beyond. Semin Radiat Oncol. 2001 Jan;11(1):16-27. [PUBMED]
- 10 Pan JG, Mak TW. Metabolic targeting as an anticancer strategy: dawn of a new era? Sci STKE. 2007 Apr 10;2007(381):pe14. [PUBMED]