El sistema inmunológico cuenta con un gran número de varios tipos de células y proteínas que pueden reconocer qué componentes celulares son normales o anormales, y qué sustancias son 'propias' o 'extrañas.' Por ejemplo, cuando una espina se atasca en el cuerpo, las células inmunológicas reconocen a la espina como un objeto extraño y la atacan. Lo mismo ocurre en el caso de bacterias, virus u otros organismos que pueden invadir nuestros cuerpos. Una distinción más sutil entre lo "propio" y lo "extraño" ocurre cuando el sistema inmune reconoce a las células cancerígenas. El cuerpo las logra reconocer y atacar por sus diferencias que las distingue de las células normales.
Las células y las proteínas del sistema inmunológico participan en dos tipos de inmunidad: No específica y específica1Si desea más información acerca de los temas de esta sección, la puede encontrar en la mayoría de los textos introductorios de biología; nosotros recomendamos el libro Campbell Biology, 11ma edición.2
Las siguientes secciones describen algunos de los componentes y las actividades principales del sistema inmune:
- El sistema inmunológico innato
- La respuesta inmunológica adquirida
- El sistema linfático
- El sistema inmunológico y el cáncer
- Inflamación y el cáncer
- Resumen de sección: el sistema Inmunológico
Puede que también le interese nuestra sección sobre las vacunas contra el cáncer
El sistema inmunológico innato
El sistema inmunológico innato recibe su nombre por el hecho de que nacimos con él y que cambia muy poco durante nuestras vidas. Esta división del sistema inmunológico le brinda protección al cuerpo al reconocer las características generales de los posibles patógenos. Por ejemplo, la piel bloquea la entrada de muchos tipos de organismos. Similarmente, las células del sistema inmunológico innato reconocen las características generales de los patógenos, como la pared celular de las bacterias. Sin embargo, estos tipos de células no tienen la habilidad de distinguir las clases de patógenos con las que entran en contacto. Por ejemplo, con una analogía militar, se podría equiparar a esta reacción inmune con el uso de un mismo tipo de misil para varios tipos de blancos, en vez de tener a un misil para cada tipo de blanco. Por ejemplo, los macrófagos son células que participan en la respuesta inmunológica innata al ubicar, consumir y matar a múltiples tipos de bacterias. Las células asesinas naturales son otro tipo de célula inmunológica que elimina a las células que se han infectado con un virus y a células cancerígenas.1
Existen varios componentes del sistema inmunológico innato. Aunque también se lo conoce como la inmunidad "no específica", el uso de esta terminología es algo incorrecto. Es más, los mecanismos de la inmunidad innata sí pueden atacar a "invasores" vivos y muertos con especificidad. Cuando un organismo o partícula trata de entrar al cuerpo, deben pasar por algunas barreras físicas y químicas. Por ejemplo, nuestra piel es un escudo duro pero flexible que bloquea a muchos tipos de invasores. Asimismo, los puntos de entrada a nuestro cuerpo están protegidos por mucosas pegajosas (ejemplos: boca, nariz, ano, vagina) o cera (orejas) que atrapan a las bacterias, al polvo y a otras partículas. Las secreciones corporales como el ácido en nuestro estómago y las proteínas en la saliva y las lágrimas también sirven para prevenir la entrada de patógenos. Nuestro cabello mantiene a organismos más grandes lejos de nuestra piel. Si un organismo invasor o partícula (ejemplo: una espina) alcanza a pasar a través de estas defensas, ciertas células (producidas en la médula ósea), como los macrófagos y neutrófilos atacan al objeto extraño.
El siguiente gráfico ilustra a algunos de los componentes del sistema inmune innato en los seres humanos:
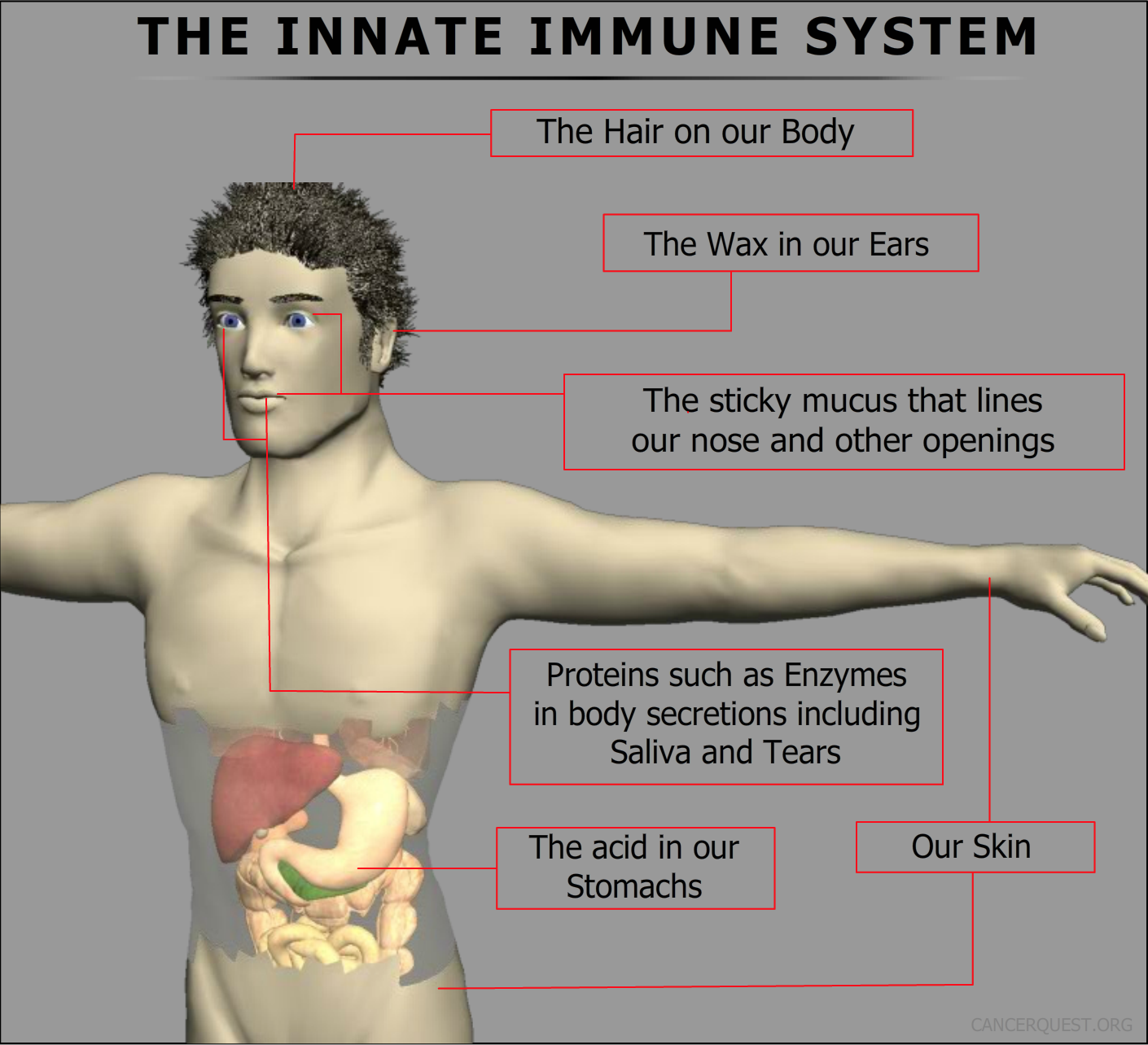
La respuesta inmunológica adquirida
La inmunidad específica o adaptativa es la segunda línea de defensa, pues solamente se activa si la repuesta inmunológica innata no logra eliminar al patógeno invasor. Sin embargo, los dos sistemas se superponen y trabajan en conjunto. Por ejemplo, las proteínas que producen las células del sistema inmunológico adaptativo se encuentran en secreciones como las lágrimas que también contienen proteínas del sistema inmunológico innato.
Ya que la respuesta inmunológica adaptativa se desarrolla y cambia durante el transcurso de nuestra vida, también se conoce como inmunidad adquirida. Las células y las proteínas de la respuesta inmunológica adaptativa son sumamente específicas hacia los patógenos invasores o las células anormales dentro del cuerpo. Esto contrasta con el amplio espectro de actividades de los componentes del sistema inmunológico innato.
Al igual que nuestro sistema inmunológico innato, la inmunidad adquirida cuenta con distintos tipos de células y las proteínas que éstas producen. Gran parte de estas células se producen en nuestra medula ósea y maduran en varias partes del cuerpo. Las células pueden flotar dentro del torrente sanguíneo, del sistema linfático o pueden permanecer dentro de algún órgano o tejido. Los dos tipos de células inmunológicas más importantes que pasan bastante tiempo dentro del sistema linfático son los linfocitos T y B. Un componente proteico importante del sistema inmunológico adquirido son los anticuerpos que producen los linfocitos B. 1.
La respuesta inmunológica específica es un sistema activo con cuatro características que lo definen:
- Especificidad antigénica- Las células y proteínas de este sistema sólo reconocen a ciertos fragmentos proteicos que se encuentran en las superficies celulares o en los fluidos corporales.
- Diversidad en el número de péptidos que pueden ser reconocidos. El sistema inmunológico adquirido es capaz de responder a un número increíble de diferentes proteínas foráneas. ¡La cantidad de proteínas y organismos con los que nos encontramos durante nuestras vidas es enorme y el sistema inmunológico adquirido es capaz de generar una respuesta especifica contra cada uno!
- Memoria-Una característica típica de la respuesta inmunológica adquirida es que si el cuerpo se encuentra nuevamente con el mismo objeto extraño, la reacción es más rápida e intensa que la primera, pues el sistema inmune guarda memoria de las sustancias con las que ha entrado en contacto. Esta habilidad proviene de un tipo de linfocito conocido como el linfocito de "memoria" que vive durante mucho tiempo mientras espera la oportunidad de re-activarse y dirigir la lucha contra el objeto extraño.
- Tolerancia-El sistema inmunológico adquirido tiene la capacidad de reaccionar cuando las células dentro del cuerpo presentan anormalidades o modificaciones. Por ejemplo, el cuerpo suele rechazar a los trasplantes de órgano e intentar destruirlo ya que las células de éste no son propias del individuo. Por esta razón, a los pacientes que reciben trasplantes se les administra medicamentos para disminuir su respuesta inmunológica. 1.
De importancia para nosotros: Los cambios genéticos que transforman a las células normales en cancerígenas también pueden alterarlas de tal manera que el sistema inmunológico logra detectarlas.
Células del sistema inmunológico adquirido
Las células principales de la respuesta inmunológica específica son los linfocitos B y T. Todos los precursores celulares de los linfocitos se originan en la medula ósea. Las células pre-B permanecen en la medula ósea en donde se someten a más crecimiento, mientras que los precursores de las células T viajan para continuar su desarrollo dentro de un órgano inmunológico que se encuentra en el cuello (el timo). De hecho, las células T obtienen su nombre del timo. Para los fanáticos de las trivias: las células B obtienen su nombre de un órgano de gallinas (la Bolsa de Fabricio) donde se estudiaron a estas células por la primera vez; los humanos no tienen un órgano equivalente.
En una fase temprana del desarrollo de las células T y las células B, todas las células en desarrollo que reaccionan fuertemente con las proteínas de células normales se eliminan del sistema. De esta manera, el sistema inmunológico se asegura de que estos linfocitos no maten a las células corporales normales. Si las células T y las células B autoreactivas no se eliminan de la población de linfocitos, se pueden desarrollar enfermedades autoinmunes como el lupus o la artritis reumatoide.
Existen dos clases de linfocitos T:
- Linfocitos T cooperadores- Estas células ayudan a otras células inmunológicas, incluyendo a los linfocitos T citotóxicos, a los macrófagos y a los linfocitos B, a ejercer sus funciones de una manera más eficiente.
- Linfocitos T Citotóxicos (CTL)-(cito=célula y tóxicos porque pueden matar) Éstas son células que tienen la capacidad de matar a otras células; son asesinas celulares. Estas células pueden matar a cualquier célula que reconocen como anormal, tal como las células infectadas con un virus o las células cancerígenas.
Los linfocitos T prematuros que residen en los nódulos linfáticos y en el bazo no pasan a ser células completas hasta que una célula presentadora de antígeno viene a ellas y les acerca a un antígeno proteico. Una vez que el linfocito T reconoce la presencia de células que contienen estas proteínas anormales, salen de los nódulos linfáticos y del bazo para circular por el cuerpo a ubicar a las células anormales. Cuando las células T encuentran a las células anormales tienen la capacidad de matarlas. En el caso de una infección viral, el matar a la célula es una manera drástica pero efectiva de prevenir la reproducción del virus. Las células citotóxicas del sistema inmunológico también pueden reconocer y eliminar a las células cancerígenas.
Los linfocitos B son otro componente crítico de la respuesta inmunológica adquirida. Al igual que los linfocitos T, los linfocitos B se producen en la médula ósea. Las células se mueven hacia el cuerpo para madurar. Las células B se encargan de producir anticuerpos, proteínas que reconocen objetos foráneos que entran al cuerpo (virus, bacterias, otras proteínas, etc.). Cada linfocito B puede reconocer solamente a un blanco molecular. Por ende, el cuerpo tiene millones de tipos distintos de células B para poder responder a una gran cantidad de agentes patológicos.
El sistema inmunológico funciona como un sistema de vigilancia efectivo para eliminar a las células anormales y a los organismos invasores de nuestros cuerpos.
Cómo el sistema inmunológico visualiza al mundo
Nuestro sistema inmunológico está en actividad constante examinado nuestro cuerpo en busca de invasores, como las bacterias y los virus. El sistema inmunológico también es capaz de reconocer cuando las células normales han pasado por alteraciones (como las células cancerígenas). El reconocimiento de invasores o de sustancias "propias" modificadas, requiere la cooperación entre diferentes células y es un proceso altamente regulado.
Los pasos exactos de una repuesta inmunológica varían según el tipo de amenaza (virus, bacteria, etc.) pero por lo general, lo que ocurre es lo siguiente: primeramente, nuestras células reconocen a ciertas partes del patógeno, como los fragmentos proteicos que resultan de la digestión de una proteína más grande. Por ejemplo, una bacteria que invade la piel a través de una lesión puede reconocerse por las proteínas en su superficie.
Cualquier proteína o producto (azúcar, lípido, etc.) que el sistema inmunológico puede reconocer y que lleva a la producción de una respuesta inmunológica se considera un antígeno.
Algunas células inmunológicas, incluyendo a los macrófagos y las células dendríticas, pueden cargar estas proteínas en su superficie y "presentarlos" a los linfocitos B y T para activarlos. Las células que tienen la capacidad de presentar antígenos se denominan células presentadoras de antígeno.
Cada linfocito B y T cuenta con múltiples copias de un solo tipo de receptor en su membrana celular. Los receptores de los linfocitos B y T tienen la habilidad de adherirse a un solo tipo de antígeno. La expresión de un solo tipo de receptor asegura que cada linfocito tenga la especificidad para un solo antígeno. A diferencia de las células de la repuesta inmunológica innata, los linfocitos pueden identificar a sus blancos moleculares aún en la presencia de sustancias semejantes. ¡Hay suficientes linfocitos diferentes en el cuerpo para reconocer a más de un billón de péptidos distintos! Esta increíble diversidad asegura que el cuerpo tenga células capaces de reconocer casi cualquier sustancia.
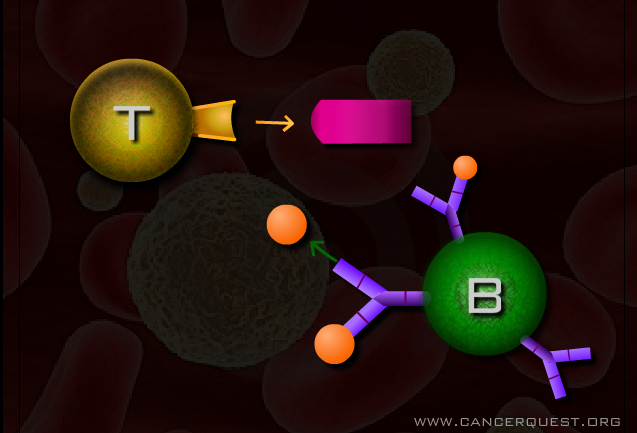
La respuesta inmunológica específica se divide en dos partes: la inmunidad humoral y celular. La inmunidad humoral consiste en la producción de anticuerpos en los linfocitos B. Estos pequeños interceptores proteicos en forma de Y circulan por la sangre y otros fluidos corporales. Cuando un anticuerpo choca con su blanco molecular (antígeno), se une a él fijamente para destruir o desactivarlo. Los anticuerpos pueden:
- Neutralizar toxinas
- Adherirse a los virus para prevenir su entrada a las células
- Unirse a moléculas en el torrente sanguíneo para eliminarlas
- Marcar al patógeno para que el sistema inmunológico innato lo elimine
- Trabajar en conjunto con otras proteínas corporales para matar a las bacterias y parásitos directamente
El sistema linfático
Una vez desarrollados, los linfocitos circulan por el cuerpo y permanecen en el tejido linfático, incluyendo los ganglios linfáticos y el bazo, en donde buscan y esperan entrar en contacto con sus proteínas blanco. El sistema linfático es un sistema de vasos (tubos) que se extiende por todo el cuerpo. Al igual que el sistema circulatorio, el sistema linfático transporta líquidos, proteínas y células del sistema inmunológico, sin embargo no contiene glóbulos rojos. Estos dos sistemas (linfático y circulatorio) están conectados. El sistema linfático recoge el liquido y las células del cuerpo y los regresa al sistema circulatorio a través de ductos en el área del cuello/hombros. El líquido dentro de los vasos linfáticos se llama linfa.
Como los riachuelos que se unen para formar ríos que finalmente fluyen al océano, los vasos linfáticos más pequeños vacían su contenido en otros más grandes. Este flujo viaja hacia y se acumula en los ganglios linfáticos. Muchas de las células del sistema inmunológico residen en el sistema linfático por gran parte de su vida.
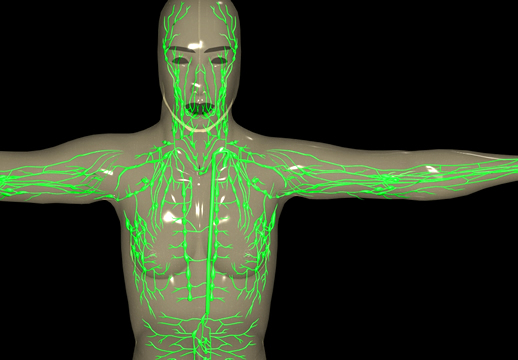
El sistema linfático es de gran importancia en el cáncer por varias razones:
- Las células cancerígenas se pueden esparcir (metástasis) al entrar al sistema linfático.
- Muchos tipos de cánceres son se clasifican según la ubicación de las células cancerígenas. Por ejemplo, si las células cancerígenas de un tumor se detectan dentro del sistema linfático, es probable que se han esparcido hacia otras áreas del cuerpo.
Aprenda más acerca del sistema linfático y la metástasis.
El sistema inmunológico y el cáncer
Los científicos no siempre tuvieron una idea definida de cómo que el sistema inmunológico desempeñaba un rol en la prevención y en la lucha contra el cáncer. Esta idea fue propuesta en el 1957, sin embargo, la evidencia científica en esos momentos sólo parecía indicar que el sistema inmunológico protegía contra ciertos patógenos como virus y bacterias, pero no contra las células corporales anormales como las células cancerígenas. A finales del siglo XX, varios investigadores y médicos se dieron cuenta de que personas con sistemas inmunológicos muy débiles o no existentes, tenían un riesgo más alto de desarrollar cáncer que una persona promedio. Además, desde entonces los investigadores se han dado cuenta de que pacientes con células inmunológicas presentes en sus tumores tienen un mejor pronóstico que los pacientes sin ellas.3
La inmunovigilancia que describe la actividad de las células inmunológicas, como por ejemplo la circulación corporal de los linfocitos T en busca de cualquier anormalidad. Cuando las células corporales pasan por mutaciones, las células inmunes las pueden detectar y marcar como anormales. Entonces, el cuerpo las reconoce como no propias o extrañas. Al eliminar las células anormales, el sistema inmunológico realza la protección en contra del cáncer. Sin embargo, las mutaciones pueden llegar a ser tan drásticas que logran evadir el mecanismo de vigilancia del sistema inmunológico, y como resultado, continúan su división como células cancerígenas. El proceso es una versión compleja de "jugar al escondite" con consecuencias importantes.
Para reiterar, los linfocitos T reconocen a los péptidos antígenos se que presentan cerca sobre su superficie celular. Si las células pre-cancerígenas presentan proteínas anormales, las células T las reconocerán como anormales. Recíprocamente, las células pre-cancerígenas que el sistema inmunológico no reconoce como anormales, o no puede eliminar, sobrevivirán y podrían proliferarse para formar un tumor.
Hay varios mecanismos que las células tumorales pueden usar para evadir a las defensas inmunológicas del cuerpo. Muchos cánceres producen mensajeros químicos que inhiben las acciones de las células inmunológicas. Otros cánceres tienen defectos en la manera en que los antígenos son presentados sobre su superficie celular. Sin embargo, otras células inmunológicas, llamadas células destructoras naturales (Natural Killer cells - NK), juegan un papel especial en este caso porque se dan cuenta cuando las células corporales ya no tienen proteínas "propias" sobre su superficie y matan a las células anormales. Adicionalmente, algunos tumores crecen en lugares como los ojos o el cerebro, los cuales no están regularmente patrullados por las células inmunológicas.4
La meta principal de la inmunoterapia y de las vacunas contra el cáncer consta de facilitar la comunicación de las señales celulares necesarias que necesita el sistema inmune para reconocer a las células cancerígenas como anormales. Si tienen éxito, estas estrategias podrían permitir que el cuerpo reconozca y destruya a las células cancerígenas, incluyendo aquéllas que han logrado formar un tumor.
Aprenda más sobre las vacunas contra el cáncer
El sistema inmunológico y el desarrollo del cáncer
Aparte de luchar en contra el cáncer, el sistema inmune también parece estar involucrado en el desarrollo de gran parte de, si no todos, los casos de cáncer. La inflamación crónica parece ser un punto de partida importante. La inflamación ocurre cuando las células inmunes producen químicos y proteínas como reacción a una 'amenaza'. Esta amenaza puede ser un microbio (bacteria o virus) o una sustancia más sutil. Hoy en día, ya se sabe que la obesidad y el estrés pueden estimular una reacción inflamatoria del sistema inmune. La inflamación puede durar por mucho tiempo, incluso por varios años. La actividad alargada de esta reacción puede causar problemas en las células normales y puede provocar el desarrollo del cáncer.
Aunque la inflamación es una reacción corporal normal, es muy dañina cuando ocurre en el contexto del cáncer. Algunos tipos de células inmunológicas que participan en las reacciones inflamatorias se describen en esta sección. La inflamación que se observa en el cáncer se encuentra bajo investigación activa como un enfoque de la prevención del cáncer y de su tratamiento.
Macrófagos y reorganización de tejidos
Los macrófagos son una clase de leucocito cuya función consta de destruir a microbios y a sustancias extrañas. Cuando los macrófagos invaden el área alrededor del tumor, se introducen dentro del micro-ambiente complejo del tumor. Los macrófagos que rodean al tumor se conocen como los macrófagos asociados con tumores, y suelen participar en el crecimiento del tumor y no en su destrucción. La presencia de los macrófagos provoca la inflamación y promueve la proliferación de células cancerígenas, el crecimiento de vasos sanguíneos, la invasión de células cancerígenas, su propagación a ubicaciones distantes (metástasis) y la resistencia a los tratamientos de cáncer como la quimioterapia.
Los monocitos que circulan por el cuerpo (precursores de los macrófagos) también desempeñan un rol en el microambiente del tumor. Los monocitos inflamatorios normalmente atacan a microbios, pero pueden presentar un peligro ya que promueven la inflamación y producen proteínas que la estimulan, como el factor de necrosis tumoral alfa y la interleucina 1 beta. Los monocitos residentes normalmente responden a los virus y participan en la reorganización de tejidos, la angiogénesis y la producción de colágeno. Los monocitos inflamatorios están asociados con una gran cantidad de cáncer.
La manera de la cual un macrófago actúa en el microambiente del tumor puede variar. Los macrófagos que NO participan en el crecimiento del tumor pertenecen al la categoría M1, y los macrófagos que producen sustancias que sí estan involucradas en este proceso representan la categoría M2. La causa detrás de la transformación de un macrófago M1 a un macrófago M2. Típicamente, los macrófagos que rodean un tumor son M1 y atacan al tumor. Sin embargo, medida que el tumor va creciendo, la cantidad de macrófagos M2 domina y promueve los procesos pro-tumor como la angiogénesis y la metástasis. Los macrófagos asociados a tumores también pueden estimular la inmuno-supresión local, y por lo tanto, prevenir que otras células inmunes ataquen al tumor.5, 6
Células supresoras derivadas de la médula ósea (células mieloides supresoras)
Las células supresoras son células inmunes que pueden bloquear al sistema inmunológico. Normalmente, nuestros cuerpos necesitan a estas células para disminuir o detener la actividad del sistema inmune una vez que se logra eliminar a una amenaza. Estas células reducen la actividad de los linfocitos T y regulan la producción de proteínas de señalización celular (citoquinas) en los macrófagos. En el cáncer y en otras enfermedades, la actividad estas células no procede como debe, y las respuestas inmunológicas en contra de las células cancerígenas pueden llegar a bloquearse.7, 8
La inflamación y el cáncer
La inflamación es una reacción corporal a eventos potencialmente dañinos. Es un proceso protector y necesario que involucra el reclutamiento de células y moléculas del sistema inmune del cuerpo para llevarlas al lugar de las lesión. Las células y moléculas reclutadas, en conjunto con las células locales, remueven las células muertas y lastimadas. Además, se encargan de eliminar la causa de cualquier irritación, sea a causa de un químico, objeto foráneo o un organismo invasivo. Después, las células inmunes empiezan el proceso de reparación en las células y los tejidos del área. La inflamación es una respuesta inmune compleja que envuelve un gran número de células y señales distintas. Es esencial para nuestra supervivencia.9
Síntomas de la inflamación
La inflamación aguda, se mencionó por primera vez en el siglo I, y es una reacción física que está compuesta por cuatro indicios, descritos por el romano Aulus Cornelius Celsus:
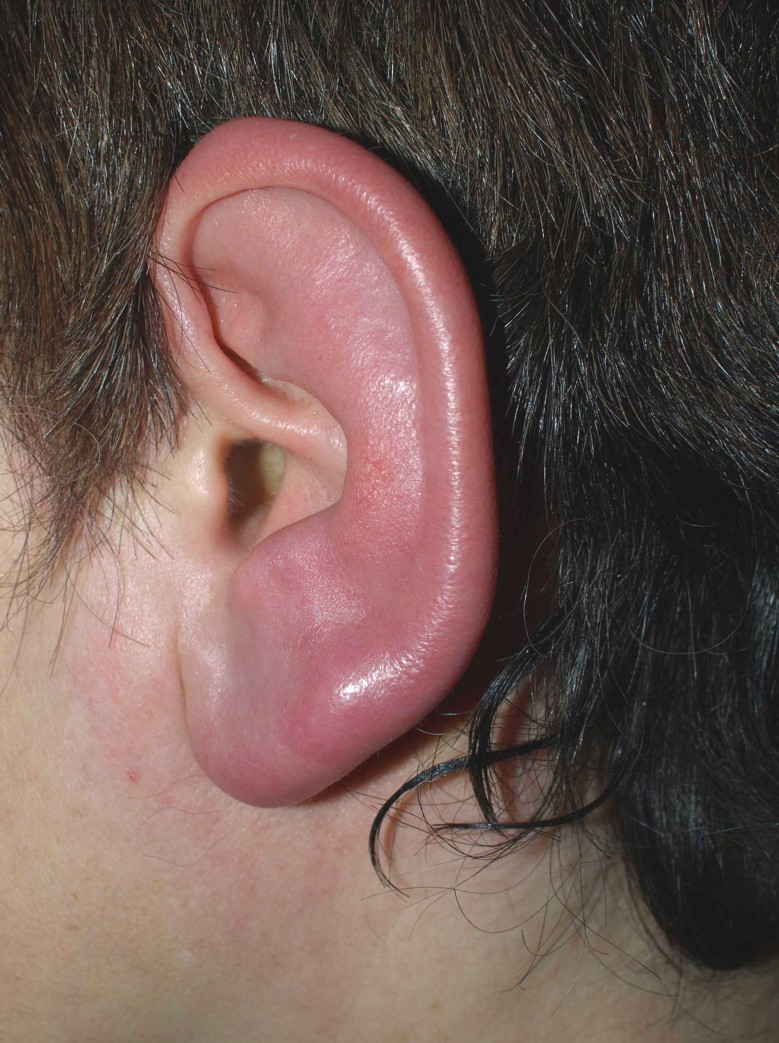
1. rubor (enrojecimiento)
2. calor
3. tumor (hinchazón)
4. dolor 10
Siglos después, ahora sabemos que la inflamación se puede manifestar de una manera distinta: una que en la que estos síntomas físicos no se demuestran y que probablemente contribuye a muchas enfermedades en las personas afectadas. Esta forma de inflamación es se conoce como la inflamación crónica. La inflamación crónica desempeña un rol importante en la formación de cáncer, contribuyendo a por lo menos 15% de todos los tumores sólidos.11
Imagen: Klaus D. Peter, Gummersbach, Germany (Own work) [CC BY 3.0 de (http://creativecommons.org/licenses/by/3.0/de/deed.en)], via Wikimedia Commons
¿Cómo puede ser dañina la inflamación?
Nuestro sistema inmune ataca y elimina a invasores foráneos, pero este mecanismo de defensa puede ser dañino si se sale de control. Por lo general, la inflamación puede ser dañina cuando la reacción se prolonga.12 Durante la curación normal de las heridas, la inflamación y la reproducción celular que se amplifican para aliviar la lesión, se disipan luego de que se sana la lesión. Sin embargo, si se sustenta por varios años, el riesgo de desarrollar el cáncer se eleva, según varios estudios epidemiológicos.12 Como con muchos aspectos de cáncer, el rol de la inflamación en cáncer viene de un proceso biológico normal que se sale de control. Un proceso que debía haber sido corto se extiende por mucho u ocurre cuando no debe. La inflamación suele causar el cáncer mediante la producción de químicos que dañinos para las células. Esta reacción se puede comparar con un daño colateral del uso de un arma. Estos químicos, llamados especies reactivas de oxígeno (ROS) y especies reactivas de nitrógeno (NOS), son usadas por las células del sistema inmune (leucocitos y fagocitos) como defensa contra infecciones.13 ROS y NOS causan daño al ADN que puede matar organismos invasores. Si atacan nuestras propias células, pueden causar daño celular permanente (mutaciones).12 Las células inmunes también pueden producir moléculas de señal (citoquinas), enzimas destructivas (peptidasa) y otros medios para matar células (como TNF-α y interleucinas).12
Inflamación crónica vs aguda
Inflamación crónica vs. inflamación aguda
Inflamación aguda (a corto plazo) es diferente a inflamación crónica (a largo plazo) en varias maneras. Las diferencias incluyen:
Aguda
- Progreso rápido (minutos u horas)
- Mayoría de las células que se reclutan son neutrófilos
- Causa lesiones leves al tejido afectado.
- Síntomas físicos y notables a nivel local y sistémico.9

Crónica
- Progreso lento (días)
- Suele involucrar el reclutamiento de macrófagos (derivados de monocitos) y linfocitos
- Causa daño leve a severo en el tejido afectado
- Síntomas físicos leves o no-existentes9
La inflamación crónica tiene bastante relevancia en las conversaciones acerca del cáncer ya que está asociada con un aumento del riesgo de desarrollar la enfermedad, sin embargo, la inflamación aguda no parece tener estos efectos.

Inflamación aguda
La inflamación aguda es la reacción normal del sistema inmunológico a una infección y no se considera como un factor de riesgo del cáncer.12 La inflamación aguda es una reacción universal e inmediata que se desencadena a partir de una lesión local. La lesión puede ser una infección (bacterial, viral, parasítica o con hongos), un traumatismo cerrado o penetrante, una necrosis de un tejido, la presencia de cuerpos foráneos (ej. una astilla), o cualquier irritación hipersensible (como aquella causada por la hiedra venenosa).9
La inflamación aguda está compuesta por dos elementos principales: las reacciones al nivel de los vasos sanguíneos (cambios vasculares) y al nivel celular. Cuando se presenta alguna lesión, el cuerpo responder en cuestión de segundos al enviar mediadores químicos hacia el tejido lesionado, provocando una serie de reacciones. Por ejemplo, la cantidad de sangre que fluye por los vasos sanguíneos aumenta, así como la permeabilidad vascular y la activación de las células que los rodean (células del endotelio). Esto facilita la adhesión de las células inmunes (leucocitos) y su migración al área que las necesita. El componente celular de la inflamación aguda cuenta con el traslado de los leucocitos al lugar de la lesión y su activación con el fin de eliminar a cualquier organismo invasor.9 Gran parte de la inflamación aguda también consiste de la actividad de los leucocitos polimorfonucleares. Esta reacción es un mecanismo inmunológico no-específico, ya que varios tipos de lesiones la pueden desencadenar.14
Inflamación crónica
La inflamación crónica es una reacción inmune prolongada que puede lesionar a tejidos secundarios, y puede durar por muchos años. A pesar de la diferencias claras entre la inflamación crónica y aguda, la inflamación aguda puede convertirse en crónica si la infección/lesión es muy duradera o si algo previene el proceso normal de la cicatrización. La inflamación crónica puede ser el resultado de infecciones persistentes, enfermedades de hipersensibilidad o de la exposición a agentes tóxicos.9 A diferencia de la inflamación aguda, la inflamación crónica es una reacción altamente específica e involucra a otros tipos de células inmunes (linfocitos y macrófagos). Los macrófagos son células multi-funcionales que provienen de los monocitos; su rol en la respuesta inflamatoria consiste de eliminar a los microbios y al tejido muerto, de estimular la reparación, secretar citoquinas (incluyendo quimiocinas, interleucinas, factores de necrosis tumoral y eicosanoides) y de trabajar en conjunto con los linfocitos T.
Inflamación crónica y el cáncer
La siguiente tabla (en inglés) resume la relación que existe entre la inflamación crónica y varios tipos de cáncer.

El uso de esta imagen fue autorizado por sus respectivos creadores. Referencia: Kamp DW, Shacter E, Weitzman SA. Chronic inflammation and cancer: the role of the mitochondria. Oncology (Williston Park). 2011;25(5):400-13) http://www.cancernetwork.com/oncology-journal/chronic-inflammation-and-cancer-role-mitochondria
La relación más obvia entre estos tipos de condiciones médicas se observa con el síndrome del colon irritable y el cáncer colorectal. Aquellos que padecen de este trastorno digestivo tienen una probabilidad de sufrir del cáncer colorrectal 5 a 7 veces mayor a lo normal. Cerca de 4 de 10 pacientes con colitis ulcerosa--un tipo de IBD--desarrollan CRC 25-35 años luego.15

Las evidencias más nuevas que corroboran la conexión entre el cáncer y la inflamación indican que los medicamentos que reducen la inflamación también disminuyen el riesgo de desarrollar algunos cánceres. Por ejemplo, las investigaciones que estudian el efecto continuo de los medicamentos anti-inflamatorios no-esteroideos (AINE) demuestran que la probabilidad de desarrollar ciertos tipos de cáncer se puede reducir. Los AINE son una clase común de medicamentos para el dolor, tal como el ibuprofeno, la aspirina y el naproxeno. El riesgo de que se desarrolle el cáncer de colon se puede reducir hasta un por 50% con el uso continuo (por lo menos 6 meses) de los AINE que no tengan aspirina, y por un un 40% con el uso a largo plazo de la aspirina.16 Los AINE actúan por medio del bloqueo de la actividad de ciertas proteínas (llamadas ciclooxigenasas o COX) que pueden causar la inflamación.17 También se ha demostrado que la aspirina puede prevenir el cáncer mediante al reducir la cantidad de un oncometabolito (Ácido alfa-hidroxi-glutárico o 2HG) en la sangre.18 El exceso del 2HG está asociado con la activación del oncogén MYC.19 Por lo tanto, la prevención de esta acumulación es otra manera en la cual la aspirina impide el desarrollo del cáncer. Adicionalmente, la aspirina disminuye el riesgo de muerte a causa del cáncer prostático.20 Las Fuerzas especiales de servicios preventivos de los Estados Unidos recomienda "iniciar el uso de la aspirina en dosis pequeñas para la prevención primaria de enfermedades cardiovasculares y el cáncer colorrectal en adultos entre los 50 y 59 años de edad con un riesgo mayor o igual a un 10% de padecer de enfermedades cardiovasculares dentro de diez años, que no tienen riesgo aumentado de desangramiento, y con una esperanza de vida mayor de 10 años y están dispuestos a tomarla aspirina diariamente por lo menos por 10 años."21
Se debe tomar en cuenta que una asociación entre hechos (correlación) no siempre significa que una acción causa la otra (causalidad). Por lo general, los estudios que se han mencionado demuestran una correlación entre la inflamación y el cáncer, sin embargo no indican explícitamente que la inflamación causa cáncer. A continuación se describen algunas las investigaciones que buscan identificar los mecanismos por los cuales la inflamación puede causar el cáncer.
¿Causa el cáncer la inflamación?
La idea de que existe una relación entre la inflamación y el cáncer comenzó en 1836, cuando Rudolf Virchow hipotetizó que los lugares de inflamación a largo plazo (crónica) eran el origen de los cánceres.17 Hoy en día, esta relación ahora es una convención científica que cuyos mecanismos celulares y moleculares están bajo investigación. La inflamación a largo plazo incrementa el riesgo de que se desarrolle el cáncer mediante:
- Proliferación celular sustentada
- Aumento de factores de crecimiento
- Cambios en las células locales y proteínas que crean estromas activos
- La invasión y activación de las células inmunes inflamatorias
- Un aumento en la cantidad de agentes que causan daños al ADN en el área.17
Ya que el cáncer es una enfermedad que proviene de una serie de cambios genéticos, la presencia de químicos peligrosos para el ADN puede ser crítica para el desarrollo del cáncer. Por ejemplo, las especies reactivas de oxígeno (ROS por sus siglas en inglés) o de nitrógeno (NOS por sus siglas en inglés) contienen ciertas estructuras químicas, los radicales libres, que pueden causarle daño directo al ADN. Si esta daño se presenta en los oncogenes o en los genes de supresión de tumores, la célula afectada puede empezar a dividirse de manera descontrolada, algo característico del cáncer.
Algunos de los mecanismos son más difíciles de definir. La enzima COX-2 se produce en células inmunes, y estimula la producción de prostaglandinas, un grupo de moléculas de señalización celular que provocan la inflamación. Varios estudios han demostrado que la proteína COX-2:
- Provoca la inestabilidad genómica
- Induce la expresión genética de la resistencia a la doxorubicina, un medicamento quimioterapéutico, mediante el gen BCL2 (un oncogén que previene apoptosis).22
Otro hallazgo que corrobora esta relación causante es la deficiencia de la citoquina anti-inflamatoria IL-10 que se ha manifestado mediante mutaciones de el ADN ratones de modelo de la enfermedad del colon irritable.23
Imagen: "Virchow1" por Hanns Fechner - http://www.kunsttexte.de/download/bwt/werner.pdf Gabriele Werner, Das Bild vom Wissenschaftler - Wissenschaft im Bild, in: kunsttexte.de Seite 2. Licensed under Public Domain via Wikimedia Commons - https://commons.wikimedia.org/wiki/File:Virchow1.JPG#/media/File:Virchow1.JPG
Aprenda más sobre los oncogenes
Aprenda más sobre los represores de tumores
Prevención de la inflamación
La inflamación es influenciada por la dieta y estilo de vida. Por el lado de las dietas, muchas comidas han sido asociadas con aumentos o reducciones de inflamación. En la siguiente lista podemos ver algunos ejemplos, con breves descripciones acerca de la manera en que se piensan que funcionan. Note que esta lista no es una recomendación de ninguna comida o dieta específica.
Comidas que han sido estudiadas por su efectos anti-inflamatorios:

- Suppresión de las secuencias NF-kB and STAT3
- Exhibe propiedades similares a bloqueadores de factores de necrosis tumoral, factores de crecimiento celular vascular, factor de crecimiento epidérmico y HER2.25
Granada
- El jugo y la corteza poseen propiedades antioxidantes
- El jugo, la corteza y el aceite pueden interferir con proliferación de células tumorales, el ciclo celular, invasión y angiogénesis
Aceite de oliva extra virgen26, 27
- Contiene un compuesto fenólico en el aceite llamado oleocantal actúa como un inhibidor de COX (ciclooxigenasas)
- El oleocantal también puede inducir la apoptosis en las células cancerígenas via al alterar la permeabilidad de la membrana lisosomal

Soya
- Contiene un compuesto conocido como la genisteína puede tener propiedades anti-inflamatorias al afectar monocitos, granulocitos y linfocitos
- En ensayos con ratones, las proteínas de la soya lograron inhibir las secuencias de señalamiento NF-kB y AKT
- Los ácidos grasos omega-3 que se encuentran en la comida tienen factores modulatorios anti-inflamatorio y del sistema inmune
- El alto consumo del ácido omega-3 a omega-6 puede reducir el estrés oxidativo.
- El consumo de ajo lleva a la inhibición de NF-kB en estudios in vitrio.
- Alicina, un compuesto encontrado en ajo, alivia la inflamación en ratas.
Jengibre 33
- Tiene efectos anti-inflamatorios en los ratones
Fitoquímicos (estos están presentes en muchas plantas distintas):
Flavenoides34
- La casticina y el crisosplenol D inhiben la inflamación en vitrio y en vivo en ratones
Carotenoides35
- Varios studios han demostrado que los carotenoides tienen propiedades anti-oxidantes y anti-inflamatorias.
Comidas que han sido asociadas con un AUMENTO en inflamación incluyen:
Ácidos grasos trans36
- Posible rol en inflamación intestinal

Carne Roja 37
- Contiene una molécula de azúcar que puede causar la inflamación.
La reducción de la inflamación también ha sido asociada con terapias de cuerpo y mente.
Actividades asosciadas con una reducción en inflamación:
Tai chi38
- Sobrevivientes de cáncer de mama* con insomnia que practicaron Tai Chi por tres meses demostraron una reducción en los marcadores de inflamación IL-6 y TNF
Yoga39
- Sobrevivientes de cáncer de mama* que practicaron yoga demostraron una reducción en IL-6 y TNF.
*Para más información sobre la vida post-cáncer, visite nuestra página dedicada a la supervivencia.
Resumen:
Introducción al sistema inmunológico
- El sistema inmunológico es capaz de distinguir entre lo que es "propio" y "no propio" y también entre células normales y anormales.
- El sistema inmunológico actúa a través de dos mecanismos amplios y un poco sobrepuestos: Respuesta Inmunológica Específica e Inmunidad No Específica (Innata).
El sistema inmunológico innato
- El sistema inmunológico innato lleva a cabo las funciones no específicas.
- El sistema inmunológico innato consiste de tres componentes:
- Barreras físicas y químicas como la piel, mucosas y cera del oído.
- Células como los macrófagos y los neutrófilos.
- Proteínas que incluyen enzimas encontradas en la saliva y las lágrimas.
- El sistema inmunológico innato reconoce rasgos generales de patógenos potenciales.
La respuesta inmunológica adquirida
- La respuesta inmunológica adquirida lleva a cabo la inmunidad específica o adaptativa.
- La respuesta adaptativa se desarrolla y cambia a lo largo del transcurso de nuestra vida.
- La respuesta inmunológica adaptativa tiene especificidad hacia a los patógenos invasores.
- Las células B y células T son los tipos principales de células del sistema inmunológico adquirido.
- La respuesta inmunológica específica se caracteriza por lo siguiente: 1) especificidad antigénica, 2) diversidad, 3) memoria, y 4) discriminación entre lo propio y lo extraño
- La respuesta inmunológica adaptativa puede detectar a las células cancerígenas.
Células de la respuesta inmunológica adquirida
- Los linfocitos B y T se producen en la médula ósea.
- Los linfocitos residen en los tejidos linfáticos, como por ejemplo, en los ganglios linfáticos o en el bazo.
- Cualquier proteína o producto que pueda ser reconocido por el sistema inmunológico e inducir una respuesta inmunológica se denomina antígeno.
- Los linfocitos B producen anticuerpos que se adhieren firmemente a un patógeno, para desactivar o destruirlo.
- Al madurarse, los linfocitos T se convierten en linfocitos T auxiliares o linfocitos T citotóxicos.
El sistema inmunológico y el cáncer
- El sistema inmunológico puede logra etiquetar a las células mutantes o anormales como extrañas.
- Las células cancerígenas pueden mutarse lo suficiente para escapar de los mecanismos de vigilancia del sistema inmunológico.
- Varios tipos de cáncer producen señales químicas que inhiben las acciones de las células inmunológicas.
- Algunos tumores crecen en lugares como los ojos o el cerebro, donde las células inmunológicas no suelen estar activas.
- La inmunoterapia y las vacunas para el cáncer se diseñan con el fin de realzar las señales celulares que requiere el sistema inmunológico para reconocer y destruir a las células cancerígenas.
Si le parece que nuestro material es útil, por favor considere referenciar nuestro sitio web.
- 1abcd Charles Janeway, Paul Travers, Mark Walport and Mark Schlomchik. Immunobiology. (2004) 6th Edition. Garland Publishing, NY, NY
- 2 Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11th ed.). Pearson.
- 3 Gavin P. Dunn, Allen T. Bruce, Hiroaki Ikeda, Lloyd Old and Robert D. Schreiber. Cancer immunoediting: from immunosurveillance to tumor escape. Nature Immunology. (2002) 3 (11): 991-998. [PUBMED]
- 4 Biagi E, Rousseau RF, Yvon E, Vigouroux S, Dotti G and Brenner MK. "Cancer vaccines: dream, reality or nightmare?" Clinical Experimental Medicine. (2002) 2:109-118 [PUBMED]
- 5 Lahmar Q, Keirsse J, Laoui D, Movahedi K, Van Overmeire E, Van Ginderachter JA. Tissue-resident versus monocyte-derived macrophages in the tumor microenvironment. Biochim Biophys Acta. 2015 Jul 2. pii: S0304-419X(15)00052-9. [Epub ahead of print] [PUBMED]
- 6 Ostuni R, Kratochvill F, Murray PJ, Natoli G. Macrophages and cancer: from mechanisms to therapeutic implications. Trends Immunol. 2015 Apr;36(4):229-39. Epub 2015 Mar 11. [PUBMED]
- 7 Gabrilovich DI, Nagaraj S. Myeloid-derived suppressor cells as regulators of the immune system. Nat Rev Immunol. 2009 Mar;9(3):162-74. [PUBMED]
- 8 Katoh H, Watanabe M. Myeloid-Derived Suppressor Cells and Therapeutic Strategies in Cancer. Mediators Inflamm. 2015;2015:159269 Epub 2015 May 19 [PUBMED]
- 9abcdef Kumar, Vinay, Abul K. Abbas, Jon C. Aster, and Stanley L. Robbins. "Chapter 2 Inflammation and Repair." <i>Robbins Basic Pathology</i>. 9th ed. Philadelphia, PA: Elsevier/Saunders, 2013. 29-74. Print.
- 10 Punchard NA, Whelan CJ, Adcock I. The Journal of Inflammation. J Inflamm (Lond) 2004 Sep 27;1(1):1. [PUBMED]
- 11 Ahmad A, Banerjee S, Wang Z, Kong D, Majumdar AP, Sarkar FH. Aging and inflammation: etiological culprits of cancer. Curr Aging Sci. 2009 Dec; 2(3):174-86. [PUBMED]
- 12abcde Emily Shacter and Sigmund A. Weitzman, Chronic Inflammation and Cancer, Colorectal Cancer, Oncology Journal, January 31, 2002
- 13 Lisa M. Coussens and Zena Werb, Inflammation and Cancer, Nature 420, 860-867, December 19, 2002
- 14 Ryan GB, Majno G., Acute inflammation. A review., Am J Pathol. 1977 Jan;86(1):183-276. [PUBMED]
- 15 Kamp DW, Shacter E, Weitzman SA; Chronic inflammation and cancer: the role of the mitochondria; Oncology (Williston Park). 2011 Apr 30;25(5):400-10, 413. [PUBMED]
- 16 García-Rodríguez LA, Huerta-Alvarez C; Epidemiology. 2001 Jan;12(1):88-93; Reduced risk of colorectal cancer among long-term users of aspirin and nonaspirin nonsteroidal antiinflammatory drugs. [PUBMED]
- 17abc Lisa M. Coussens & Zena Werb. Inflammation and cancer. Nature (420). December 2002. [http://osteosarcomasupport.org/immunology/inflammation-cancer-nature-2002.pdf]
- 18 Liesenfeld DB, Botma A, Habermann N, Toth R, Weigel C, Popanda O, Klika KD, Potter JD, Lampe JW, Ulrich CM; Aspirin Reduces Plasma Concentrations of the Oncometabolite 2-Hydroxyglutarate: Results of a Randomized, Double-Blind, Crossover Trial; Cancer Epidemiol Biomarkers Prev. 2016 Jan;25(1):180-7. [PUBMED]
- 19 Terunuma A, Putluri N, Mishra P, Mathé EA, Dorsey TH, Yi M, Wallace TA, Issaq HJ, Zhou M, Killian JK, Stevenson HS, Karoly ED, Chan K, Samanta S, Prieto D, Hsu TY, Kurley SJ, Putluri V, Sonavane R, Edelman DC, Wulff J, Starks AM, Yang Y, Kittles RA, Yfantis HG, Lee DH, Ioffe OB, Schiff R, Stephens RM, Meltzer PS, Veenstra TD, Westbrook TF, Sreekumar A, Ambs S; J Clin Invest. 2014 Jan;124(1):398-412; MYC-driven accumulation of 2-hydroxyglutarate is associated with breast cancer prognosis. [PUBMED]
- 20 Assayag J, Pollak MN, Azoulay L.J Urol; 2015 Apr;193(4):1220-5; The use of aspirin and the risk of mortality in patients with prostate cancer. [PUBMED]
- 21 Bibbins-Domingo K, on behalf of the U.S. Preventive Services Task Force. Aspirin Use for the Primary Prevention of Cardiovascular Disease and Colorectal Cancer: U.S. Preventive Services Task Force Recommendation Statement. Ann Intern Med 12 April 2016
- 22 Singh B, Cook KR, Vincent L, Hall CS, Berry JA, Multani AS, Lucci A; J Surg Res. 2008 Jun 15;147(2):240-6; Cyclooxygenase-2 induces genomic instability, BCL2 expression, doxorubicin resistance, and altered cancer-initiating cell phenotype in MCF7 breast cancer cells. [PUBMED]
- 23 T SCHEININ, D M BUTLER, F SALWAY, B SCALLON, and M FELDMANN; Clin Exp Immunol. 2003 Jul; 133(1): 38¿43; Validation of the interleukin-10 knockout mouse model of colitis: antitumour necrosis factor-antibodies suppress the progression of colitis [PUBMED]
- 24 Kim JH, Gupta SC, Park B, Yadav VR, Aggarwal BB, Turmeric (Curcuma longa) inhibits inflammatory nuclear factor (NF)-¿B and NF-¿B-regulated gene products and induces death receptors leading to suppressed proliferation, induced chemosensitization, and suppressed osteoclastogenesis, Mol Nutr Food Res. 2012 Mar;56(3):454-65 [PUBMED]
- 25ab Aggarwal BB, Sundaram C, Malani N, Ichikawa H.; Curcumin: the Indian solid gold.; Adv Exp Med Biol. 2007;595:1-75. [PUBMED]
- 26 Onica LeGendreab, Paul AS Breslincd & David A Fosterae; (-)-Oleocanthal rapidly and selectively induces cancer cell death via lysosomal membrane permeabilization; Molecular & Cellular Oncology, Volume 2, Issue 4, 2015
- 27 Lucas L, Russell A, Keast R.; Molecular mechanisms of inflammation. Anti-inflammatory benefits of virgin olive oil and the phenolic compound oleocanthal.; Curr Pharm Des. 2011;17(8):754-68. [PUBMED]
- 28 Kiecolt-Glaser JK, Epel ES, Belury MA, Andridge R, Lin J, Glaser R, Malarkey WB, Hwang BS, Blackburn E.Omega-3 fatty acids, oxidative stress, and leukocyte telomere length: A randomized controlled trial. Brain Behav Immun. 2013 Feb;28:16-24 [PUBMED]
- 29 Mori TA, Beilin LJ. Curr Atheroscler Rep. 2004 Nov;6(6):461-7. Omega-3 fatty acids and inflammation. [PUBMED]
- 30 Georgia Schäfer and Catherine H. Kaschula; The Immunomodulation and Anti-Inflammatory Effects of Garlic Organosulfur Compounds in Cancer Chemoprevention; Anticancer Agents Med Chem. 2014 Feb; 14(2): 233¿240. [PUBMED]
- 31 Li C, Lun W, Zhao X, Lei S, Guo Y, Ma J, Zhi F. Allicin alleviates inflammation of trinitrobenzenesulfonic acid-induced rats and suppresses P38 and JNK pathways in Caco-2 cells. Mediators Inflamm. 2015;2015:434692. [PUBMED]
- 32 Kiecolt-Glaser JK, Belury MA, Andridge R, Malarkey WB, Hwang BS, Glaser R; Omega-3 supplementation lowers inflammation in healthy middle-aged and older adults: a randomized controlled trial; Brain Behav Immun. 2012 Aug;26(6):988-95. [PUBMED]
- 33 Hsiang CY, Cheng HM, Lo HY, Li CC, Chou PC, Lee YC, Ho TY; J Agric Food Chem. 2015 Jul 8;63(26):6051-8; Ginger and Zingerone Ameliorate Lipopolysaccharide-Induced Acute Systemic Inflammation in Mice, Assessed by Nuclear Factor-¿B Bioluminescent Imaging. [PUBMED]
- 34 Li YJ, Guo Y, Yang Q, Weng XG, Yang Y, Wang YJ, Chen Y, Zhang D, Li Q, Liu XC, Kan XX, Chen X, Zhu XX, Kmoníèková E, Zídek Z; Toxicol Appl Pharmacol. 2015 Aug 1;286(3):151-8; Flavonoids casticin and chrysosplenol D from Artemisia annua L. inhibit inflammation in vitro and in vivo. [PUBMED]
- 35 Kaulmann A, Bohn T; Nutr Res. 2014 Nov;34(11):907-29; Carotenoids, inflammation, and oxidative stress--implications of cellular signaling pathways and relation to chronic disease prevention. [PUBMED]
- 36 Ann M. Bode and Zigang Dong; Chapter 7 The Amazing and Mighty Ginger Herbal Medicine: Biomolecular and Clinical Aspects. 2nd edition. Benzie IFF, Wachtel-Galor S, editors. Boca Raton (FL): CRC Press/Taylor & Francis; 2011.
- 37 Samraj AN, Pearce OM, Läubli H, Crittenden AN, Bergfeld AK, Banda K1 Gregg CJ, Bingman AE, Secrest P, Diaz SL, Varki NM, Varki A. A red meat-derived glycan promotes inflammation and cancer progression. Proc Natl Acad Sci U S A. 2015 Jan 13;112(2):542-7. Epub 2014 Dec 29. [PUBMED]
- 38 Michael R. Irwin,corresponding author Richard Olmstead, Elizabeth C. Breen, Tuff Witarama, Carmen Carrillo, Nina Sadeghi, Jesusa M. G. Arevalo, Jeffrey Ma, Perry Nicassio, Patricia A. Ganz, Julienne E. Bower, and Steve Cole. Tai Chi, Cellular Inflammation, and Transcriptome Dynamics in Breast Cancer Survivors With Insomnia: A Randomized Controlled Trial. J Natl Cancer Inst Monogr. 2014 Nov; 2014(50): 295-301.
- 39 Kiecolt-Glaser JK, Bennett JM, Andridge R, Peng J, Shapiro CL, Malarkey WB, Emery CF, Layman R, Mrozek EE, Glaser R. Yoga's impact on inflammation, mood, and fatigue in breast cancer survivors: a randomized controlled trial. J Clin Oncol. 2014 Apr 1;32(10):1040-9. [PUBMED]
