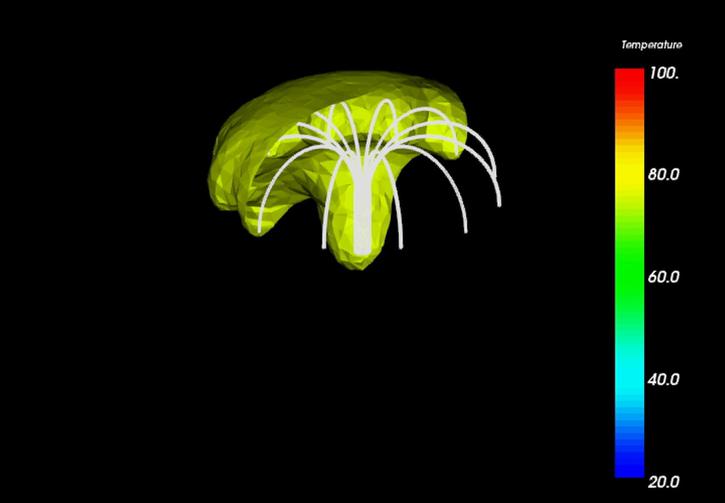
Se ha sabido por largo tiempo que las funciones celulares normales se detienen si la temperatura es elevada hasta los 42°C/108°F y que la muerte celular (necrosis) ocurre a gran escala cuando se superan los 46°C/115°F. La eliminación de células mediante calor presenta un posible método para tratar el cáncer; sin embargo es obvio que se deben tomar las medidas necesarias para minimizar el calentamiento de células sanas adyacentes.
La ablación por radiofrecuencia (RFA) es un procedimiento invasivo que utiliza pulsos eléctricos para calentar una sonda que es colocada en el tumor. La sonda puede tener la forma de una varilla recta o ser una varilla hueca que contiene varios cables pequeños. Una vez dentro del tumor, los cables pueden ser extendidos hacia el exterior para tener un mayor alcance del tumor. 1, 2
La ablación por radiofrecuencia puede ser realizada durante un procedimiento quirúrgico abierto con anestesia general o insertando la sonda a través de la piel. La colocación de la sonda puede ser guiada mediante un ultrasonido, imágnes por resonancia magnética (RM) y/o tomografía axial computarizada (CAT o CT). Después del tratamiento, las células del tumor morirán dejando sólo una cicatriz.
Los tipos de cáncer tratados con RFA incluyen: cáncer de hígado 3, 4, cáncer metastásico colorrectal 5, cáncer de pulmón 6, 7, 8 y cáncer de riñón.9
La ablación por radiofrecuencia puede ser utilizada más de una vez en caso de que surjan tumores adicionales. La efectividad del procedimiento en comparación con la de la remoción quirúrgica del tumor aún debe ser determinada.3, 5
Más información al respecto puede ser encontrada en el Capítulo 16 de La Biología del Cáncer de Robert A. Weinberg.
Vista Cercana a: Matar Células Cancersas con Calor
En un estudio hecho en ratones ingenieridas a contener células cancerosas de seno humano, los investigadores examinaron tumores con el uso de nanosondas como un método para dirigir calor a un tumor. Anticuerpos antitumorales fueron asociados a esferas muy pequeñas conteniendas gránulos de óxido de hierro. Inyección con estos 'biovectores' llevó a la unión de los partículos en el superficie de las células tumorales.
La natura química del hierro en los complejos les causan girar rápidamente cuando una frequecia magnética que alterna es aplicada cerca del tumor. El movimiento girante genera calor que rápidamente aumenta la temperatura de las células tumorales sobre 46°C/115°F, causando muerte en las células tumorales. Para esta técnica ser útil, es crítico que la frequencia aplicada no dañe tejido alrededor.
En los experimentos de ratones el tratamiento aplicado bajó signíficamente el crecimiento de tumor. Crucialmente, el efecto fue proporcional a la cantidad de calor dirigido via frequecia magnética que alterna. El tratamiento no tóxico más efectivo correpondió a una amplitud baja de la frequencia magnética con un tiempo prolongado de entrega. Desde este estudio, nanopartículas nuevas han sido desarrolladas para responder mejor a las frequencias magnéticas potencialmente reduciendo la cantidad de frequencia necesaria para tratar los tumores. 10
- 1 Widmann G, Bodner G, Bale R. Tumour ablation: technical aspects. Cancer Imaging. 2009 Oct 2;9 Spec No A:S63-7. [PUBMED]
- 2 Gillams A. Tumour ablation: current role in the kidney, lung and bone. Cancer Imaging. 2009 Oct 2;9 Spec No A:S68-70. [PUBMED]
- 3ab Jarnagin WR. Management of small hepatocellular carcinoma: a review of transplantation, resection, and ablation. Ann Surg Oncol. 2010 May;17(5):1226-33. Epub 2010 Apr 20. [PUBMED]
- 4 Laeseke PF, Frey TM, Brace CL, Sampson LA, Winter TC 3rd, Ketzler JR, Lee FT Jr. "Multiple-electrode radiofrequency ablation of hepatic malignancies: initial clinical experience." AJR Am J Roentgenol. 2007 Jun;188(6):1485-94. [PUBMED]
- 5ab Wong SL, Mangu PB, Choti MA, Crocenzi TS, Dodd GD 3rd, Dorfman GS, Eng C, Fong Y, Giusti AF, Lu D, Marsland TA, Michelson R, Poston GJ, Schrag D, Seidenfeld J, Benson AB 3rd. American Society of Clinical Oncology 2009 clinical evidence review on radiofrequency ablation of hepatic metastases from colorectal cancer. J Clin Oncol. 2010 Jan 20;28(3):493-508. Epub 2009 Oct 19. [PUBMED]
- 6 Casal RF, Tam AL, Eapen GA. Radiofrequency ablation of lung tumors. Clin Chest Med. 2010 Mar;31(1):151-63, Table of Contents. [PUBMED]
- 7 Simon CJ, Dupuy DE, DiPetrillo TA, Safran HP, Grieco CA, Ng T, Mayo-Smith WW. "Pulmonary radiofrequency ablation: long-term safety and efficacy in 153 patients." Radiology. 2007 Apr;243(1):268-75. [PUBMED]
- 8 Gadaleta C, Mattioli V, Colucci G, Cramarossa A, Lorusso V, Canniello E, Timurian A, Ranieri G, Fiorentini G, De Lena M, Catino A. "Radiofrequency ablation of 40 lung neoplasms: preliminary results." AJR Am J Roentgenol. 2004 Aug;183(2):361-8. [PUBMED]
- 9 Joniau S, Tailly T, Goeman L, Blyweert W, Gontero P, Joyce A. Joniau S, Tailly T, Goeman L, Blyweert W, Gontero P, Joyce A. J Endourol. 2010 May;24(5):721-8. [PUBMED]
- 10 Sally J. DeNardo, Gerald L. DeNardo, Arutselvan Natarajan, Laird A. Miers, Allan R. Foreman, Cordula Gruettner, Grete N. Adamson, and Robert Ivkov. "Thermal Dosimetry Predictive of Efficacy of 111In-ChL6 Nanoparticle AMF Induced Thermoablative Therapy for Human Breast Cancer in Mice." Journal Nuclear Medicine 2007 48: 437-444. [PUBMED]
