Antes de leer sobre tratamientos complementarios de plantas, por favor vea las siguientes páginas:
- Introducción a Oncología Integrativa
- Nota de Tratamientos Complementarios
- Introducción a Investigación Científica (inglés)
Muchos productos de plantas distintos han sido estudiados por su habilidad de prevenir o tratar el cáncer. La lista abajo no está completa, pero incluye algunos de los productos de plantas que han sido estudiado por estos efectos.
Como algunos de los químicos activos en las plantas que parecen prevenir el cáncer son los mismos que ayudan combatir el cáncer una vez se ha desarrollado, hemos combinado estas dos actividades en las siguientes descripciones.
Los siguientes tratamientos de plantas han demostrado actividad de tratamiento contra el cáncer en animales modelos (in vivo) o en células humanas en un laboratorio (in vitrio). Lea las entradas inviduales para más información en su actividad de prevención.
- Antocianina (Bayas)
- Bromelina (Piña)
- Curcumina (Cúrcuma)
- EGCG (Té verde)
- Licopeno (Tomates)
- Fitoestrógenos (Soya)
- Tanino (Árboles de pino)
- Resveratrol (Uvas)
- Selenio (Nueces)
Los siguientes tratamientos de plantas NO TIENEN apoyo científico sustancial en ningún modelo como un tratamiento contra el cáncer.
- Cannabis y Aceite de Cáñamo
- Essiac®, Flor-Essence® (Mezcla)
- Terapia Gerson (Mezcla)
- Guanabaná (Graviola)
Anthocyanin

Clasificado como:
Fitoquímico, Polifenol, Flavonoide, Antocianidina
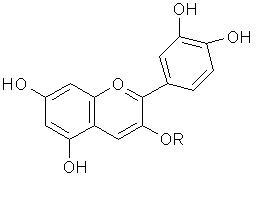
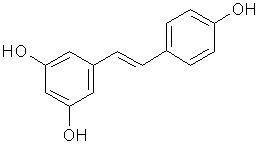
Estructura de la Antocianina
Introducción y Antecedentes
El término antocianina se refiere a un grupo de compuestos encontrados en vegetales, frutas cítricas, vino rojo, y especialmente en bayas comestibles. Las antocianinas también son responsables de los colores rojo, azul y púrpura de varias plantas.1;Pueden ayudar a prevenir desórdenes cardiovasculares, complicaciones de la edad, obesidad , respuestas inflamatorias, cáncer, y otras enfermedades degenerativas. 2, 1 Estos compuestos tambíen exhiben un comportamiento antioxidante que puede ayudar en la protección del ADN y su estructura. 2 Las antocianinas dejan el cuerpo rápido después de ser ingeridas y actualmente se desconoce su rapidez de absorción.1Este tipo de compuestos podrían atacar al cáncer induciendo la apoptosis e inhibiendo la proliferación de células cancerígenas. Aprenda más sobre la apoptosis y proliferación.3
, respuestas inflamatorias, cáncer, y otras enfermedades degenerativas. 2, 1 Estos compuestos tambíen exhiben un comportamiento antioxidante que puede ayudar en la protección del ADN y su estructura. 2 Las antocianinas dejan el cuerpo rápido después de ser ingeridas y actualmente se desconoce su rapidez de absorción.1Este tipo de compuestos podrían atacar al cáncer induciendo la apoptosis e inhibiendo la proliferación de células cancerígenas. Aprenda más sobre la apoptosis y proliferación.3
Investigación Científica
Estudios han demostrado que las antocianinas pueden retrasar el crecimiento de células tumorales in vitro.4, 5, 6 ;Ya que no se encuentra claro cómo las antocianinas actuarían en experimentos con animales,7 , no se han hecho pruebas clínicas para investigar la habilidad de las antocianinas para tratar el cáncer en humanos. La mayoría de las investigaciones recientes se concentran en la habilidad de las antocianinas para prevenir el cáncer en vez de tratarlo. Las antocianinas no han demostrado tener efectos secundarios en los estudios hechos en células in vitro 8
Actualmente, no se conocen estudios clínicos que se estén llevando a cabo sobre la investigación de los beneficios médicos de la antocianina. 9 Para información sobre pruebas clínicas que se están llevando a cabo que involucran antocianinas, por favor visite nuestra sección sobre Encontrando Ensayos Clínicos.
sobre pruebas clínicas que se están llevando a cabo que involucran antocianinas, por favor visite nuestra sección sobre Encontrando Ensayos Clínicos.
Aprobación por parte de la Administración de Fármacos y Alimentos de Estados Unidos (FDA).
No existe evidencia suficiente para respaldar la efectividad de las antocianinas en la lucha contra el cáncer y no han sido aprobadas por la FDA para tratar el cáncer.10
evidencia suficiente para respaldar la efectividad de las antocianinas en la lucha contra el cáncer y no han sido aprobadas por la FDA para tratar el cáncer.10
Es importante mantener en mente que muchos tratamientos de cáncer, incluyendo la quimioterapia y radiación, trabajan generando radicales libres para destruir a las células cancerígenas. Si un paciente con cáncer toma antioxidantes mientras se encuentra en un tratamiento de radiación o quimioterapia, es posible que estos compuestos protejan a las células tumorales de los radicales libres. Los médicos pueden recomendar a los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea los más efectivo posible.11
Bromelina

Clasificación
Como un fitoquímico, el término "bromelina" describe una enzima, o un polímero catalítico de aminoácidos, encontrado en la familia de las Bromeliaceae, de las cuales el miembro más reconocido es la piña. Técnicamente, la bromelina del tallo de la piña no es la misma enzima bromelina de la fruta de la piña, aunque en la práctica ambas son referidas como bromelina.
Introducción y Antecedentes
La piña ha sido usada terapéuticamente en Sudamerica y en el Sudeste de Asia y fue llamado en 1558 como el "fruto del cual los indígenas de América hacen el mayor uso medicinal." Aunque la bromelina fue aislada como la enzima activa de la piña en 1891, no fue producida comercialmente porque la piña era relativamente cara.
Sin embargo, en 1957 Heinecke descubrió que los tallos descartados contienen más bromelina que la fruta, abriendo el camino para la producción de bromelina como un compuesto medicinal. Actualmente, se vende en tiendas de nutrición en todo América como un suplemento que ayuda a la digestión, aunque tiene muchos usos biológicos.
Investigación científica
La bromelina ha sido estudiada por décadas. No solo ayuda a combatir la inflamación, un gran contribuyente al cáncer, pero también presenta actividad contra el cáncer en cultivos de células (in vitro) y en ratones modelo (in vivo), bloqueando el crecimiento y causando la muerte de las células cancerígenas. Por lo que la forma en que la bromelina combate el cáncer es conocida. Las enzimas en la bromelina son proteolíticas; pueden romper las proteínas en la superficie de las células, influyendo en la señalización celular y comportamiento. Sin embargo, no toda la actividad biológica de la bromelina puede ser atribuida a la proteólisis.
Grandes cantidades de bromelina deben acercarse al sitio del tumor para tener resultados significantes. A pesar de que los seres humanos pueden tolerar altas dosis de bromelina sin tener efectos secundarios, las altas dosis disminuyen la eficiencia, una característica ya antes vista en medicamentos. Como resultado de ello, estudios están actualmente en marcha para investigar nanopartículas que liberen bromelina.
Ensayos clínicos
Se ha iniciado un estudio clínico para explorar la eficacia de la bromelina como un tratamiento anticancerígeno. Otro estudio investigo el uso de la bromelina, en conjunto con otros compuestos, para reducir los efectos secundarios asociados con la quimioterapia, pero los resultados no están disponibles.
Aprobación de EUA Food and Drug Administration
No hay suficiente evidencia de que la bromelina trata el cáncer, y la bromelina no ha sido aprobada por la FDA para el tratamiento del cáncer.
*Para más información, ver la sección de Inflamación.
Curcumina

Clasificado como:
Fitoquímico, Polifenol
Tambien llamado:
Diferuloilmetano
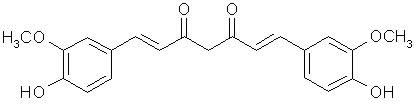
Estructura de la Curcumina
Introducción y antecedentes
La curcumina viene de la planta Curcuma longa. Es vista comúnmente como el colorante amarillo en el curry--una especia tradicional usada en el Sudeste de Asia en las comidas y medicinas.12
Este agente ha sido usado durante siglos por diferentes culturas en Asia. Por ejemplo, prácticas medicinales de la India han usado la curcumina para tratar anorexia, tos, reumatismo, y otras enfermedades.13 En la medicina hindú, los hombres todavía utilizan la curcumina para tratar esguinces e inflamación.13 La medicina tradicional china usa el mismo compuesto para tratar enfermedades que van acompañadas de dolor abdominal.13 La medicina occidental ha reconocido recientemente la capacidad anti-inflamatoria, antioxidante, antibacterial, anti-veneno, anti-VIH, así como la habilidad de combatir a la enefermedad de Alzheimer de la curcumina.13, 14
En términos de lucha contra el cáncer la curcumina podría actuar induciendo apoptosis reduciendo la angiogénesis, apoptosis, metástasis, proliferación y transformación.15
Investigación científica
Se ha encontrado que la curcumina reduce el desarrollo de las células tumorales16 y procesos angiogénicos17in vitro y en experimentos con roedores. También parece que la curcumina induce la apoptosis en células cancerígenas in vitro sin lastimar a las células saludables.18 Sin embargo, la curcumina ha encontrado varias difucultades durante las pruebas clínicas ya que parece tener una pobre biodisponibilidad (es decir, tiene problemas trabajando y manteniéndose dentro del cuerpo humano).19, 20 Los investigadores trabajan actualmente en hacer al compuesto más estable en términos de acercamiento nanotecnológico y químico.19, 21, 20 Algunas de las investigaciones más recientes del 2007 muestran que la curcumina puede incrementar el crecimiento de tumores en ratas que fueron alimentadas con curcumina. Debido a estos reportes contradictorios, es necesaria más información
que fueron alimentadas con curcumina. Debido a estos reportes contradictorios, es necesaria más información para determinar si la curcumina es un agente de lucha contra el cáncer.
para determinar si la curcumina es un agente de lucha contra el cáncer.
Actualmente, existen varias pruebas clínicas llevándose a cabo que investigan a la curcumina como un agente de lucha contra el cáncer (NCI, Campus Rambam Health Care , Centro médico Tel-Aviv Sourasky, Centro de cáncer M.D. Anderson , Universidad Johns Hopkins , Universidad de Pennsylvania, Organización médica Hadassah). Para más información sobre pruebas clínicas que se estén llevando a cabo que involucran curcumina, por favor visite nuestra sección sobre Ensayos Clínicos.
, Centro médico Tel-Aviv Sourasky, Centro de cáncer M.D. Anderson , Universidad Johns Hopkins , Universidad de Pennsylvania, Organización médica Hadassah). Para más información sobre pruebas clínicas que se estén llevando a cabo que involucran curcumina, por favor visite nuestra sección sobre Ensayos Clínicos.
Aprobación de la Administración de alimentos y fármacos de los Estados Unidos
No existe evidencia suficiente para respaldar la efectividad de la curcumina contra el cáncer y no ha sido aprobada por la FDA como tramiento contra el cáncer.22 De hecho, un gran número de productos de curcumina están en la lista de la FDA de Curas Falsas de Cáncer.
evidencia suficiente para respaldar la efectividad de la curcumina contra el cáncer y no ha sido aprobada por la FDA como tramiento contra el cáncer.22 De hecho, un gran número de productos de curcumina están en la lista de la FDA de Curas Falsas de Cáncer.
*Es importante tener en mente que muchos tratamientos de cáncer, incluyendo a la quimioterapia y radiación, trabajan generando radicales libres para destruir a las células cancerígenas. Si un paciente con cáncer toma antioxidantes mientras se encuentra en un tratamiento de radiación o quimioterapia, es posible que estos compuestos protejan a las células tumorales de los radicales libres. Los doctores pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea los más efectivo posible.23
pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea los más efectivo posible.23
EGCG



Clasificado como:
Fitoquímico, Polifenol
Otros nombres:
epigalocatequina-3-galato
Estructura de EGCG.
Introducción y antecedentes
El té es una de las bebidas de mayor consumo en el planeta, segundo después del agua.24 El té verde viene de la planta Canellia sinesis, un arbusto de hoja perenne de la familia Theaceae. Los tés verde, negro y de oolong provienen de la misma planta, se diferencian en la forma en que son preparados.25 El té verde no se fermenta, por lo tanto mantiene muchas de las propiedades benéficas de la planta de té. En general, muchas plantas producen químicos llamados polifenoles que las protegen del daño ambiental. El polifenol EGCG (epigalocatequina-3-galato) se encuentra presente en grandes cantidades en el té verde.24 El EGCG tiene propiedades antioxidantes y ha demostrado tener algunos efectos preventivos en los cánceres de piel, esófago, pulmón, estómago, hígado, intestino delgado, páncreas, colon, vejiga y de seno.26, 27 Alrededor del mundo, se cree que el té tiene varios efectos benéficos que varían desde mejorar el flujo sanguíneo, eliminación de toxinas, incrementar la resistencia a enfermedades, incremento de la salud cardiovascular, bajar el colesterol y prevenir/combatir el cáncer. Se ha encontrado que el té verde tiene antioxidantes y beneficios promotores de la salud debido a su alto contenido de epigalocatequina-3-galato (EGCG).24
Investigación científica
Estudios que han involucrado poblaciones grandes indican que tomar té verde puede estar asociado con menor riesgo de padecer ciertos tipos de cáncer.28
Lea nuestro aviso sobre MCA y métodos de quimioprevención
Estos hallazgos han sido una base para investigación sobre las habilidades para luchar contra el cáncer del té verde. Se ha encontrado que el EGCG previene que las células cancerígenas obtengan nutrientes (angiogénesis)29 e inhibe la proliferación de células cancerígenas gástricas en ratones.30 Una forma ligeramente modificada del EGCG (Pro-EGCG) recientemente ha demostrado inducir apoptosis en células cancerígenas in vitro e inhibir el crecimiento del cáncer de seno en ratones.30 Han habido pruebas clínicas numerosas para determinar la habilidad del EGCG para prevenir el cáncer con resultados mixtos. Varias pruebas clínicas han demostrado qué compuesto previene el cáncer de próstata.31, 30 En estos estudios se observaron molestias abdominales y fatiga, probablemente debido a la presencia de cafeína en el té verde.30
Aprenda más sobre angiogénesis, apoptosis y proliferación
Para información sobre pruebas clínicas que involucren EGCG que se estén realizando, por favor visite nuestra sección de Encontrando pruebas clínicas.
sobre pruebas clínicas que involucren EGCG que se estén realizando, por favor visite nuestra sección de Encontrando pruebas clínicas.
Aprobación de la Administación de alimentos y fármacos de los Estados Unidos
No existe suficiente evidencia para apoyar la efectividad del EGCG contra el cáncer y no ha sido aprobado por la FDA como tratamiento para el cáncer.32
suficiente evidencia para apoyar la efectividad del EGCG contra el cáncer y no ha sido aprobado por la FDA como tratamiento para el cáncer.32
*Es importante tener en mente que muchos tratamientos para el cáncer, incluyendo la quimioterapia y radiación, trabajan generando radicales libres para poder destruir células cancerígenas. Si un paciente de cáncer toma antioxidantes cuando se encuentra bajo tratamiento de radiación o quimioterapia, es posible que estos compuestos protejan a las células cancerígenas de los radicales libres deseados. Los doctores pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea lo más efectivo posible.11
pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea lo más efectivo posible.11
Licopeno

Clasificado como:
Fitoquímico, Carotenoide
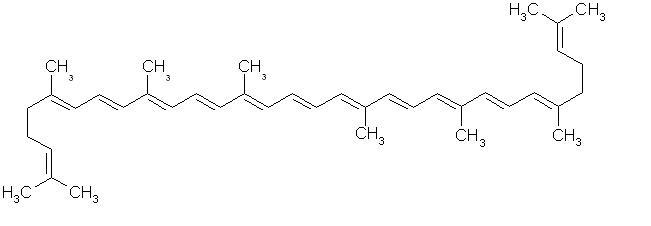
Estructura del licopeno.
Introducción y Antecedentes
El licopeno es el compuesto que le da a los tomates su colo rojo (Solanum lycopersicum).33 Las sandías, toronjas, guayabas, y papayas también contienen licopeno pero en cantidades menores. El consumo de este antioxidante ha sido asociado con un descenso en el riesgo de padecer de cáncer de próstata.34 La mayoria de las investigaciones concernientes a licopeno y cáncer involucran la prevención de cáncer de próstata. Estudios también han demostrado que el licopeno puede ser más efectivo al ser ingerido de un tomate (en vez de un suplemento).35
Investigación Científica
Cuando se administró licopeno a células cancerígenas in vitro, se indujo apoptosis en un número significativo de células.36 En un estudio realizado en ratones, el polvo obtenido de los tomates mostró inhibir la creación de células cancerosas, además prolongó la vida de los animales y redujo su tasa de muerte.37 Estudios clínicos con respecto al tomate y el licopeno muestran que no existe evidencia suficiente para decidir si el licopeno es o no un tratamiento efectivo contra el cáncer.38, 39, 35
evidencia suficiente para decidir si el licopeno es o no un tratamiento efectivo contra el cáncer.38, 39, 35
Existen varios estudios llevándose a cabo con respecto al licopeno. Dos se encuentran investigando la prevención del cáncer de próstata mientras que otro se concentra en la efectividad del licopeno como tratamiento contra el cáncer de próstata. 40 Para informarse sobre pruebas clínicas llevándose a cabo que involucran al licopeno, por favor visite nuestra sección de Ensayos Clínicos.
sobre pruebas clínicas llevándose a cabo que involucran al licopeno, por favor visite nuestra sección de Ensayos Clínicos.
Aprobación de la Administración de alimentos y fármacos de Estados Unidos
No existe evidencia suficiente para respaldar la efectividad del licopeno en la lucha contra el cáncer y no ha sido aprobado por la FDA como tratamiento para el cáncer. 22
*Es importante tener en mente que muchos tratamientos de cáncer, incluyendo a la quimioterapia y radiación, trabajan generando radicales libres para destruir a las células cancerígenas. Si un paciente con cáncer toma antioxidantes mientras se encuentra en un tratamiento de radiación o quimioterapia, es posible que estos compuestos protejan a las células tumorales de los radicales libres. Los doctores pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea los más efectivo posible.23
pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea los más efectivo posible.23
Fitoestrógenos



Clasificado como:
Fitoquímicos, Fitoestrógenos, Isoflavona
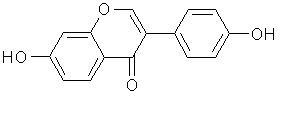
Tipos de Fitoestrógenos
Isoflavonas (por ejemplo, la genisteína, daidzeína, gliciteína, formononetina) 41

Estructura de la Genisteína Estructura de la Daidzeína
Lignanos (por ejemplo, secoisolariciresinol, matairesinol, lariciresinol pinoresinol)42
Estructura de un Lignano
Coumestan (ejemplo: coumestrol)43
Estructura del Coumestan
Isoflavonoides
Estructura de los Isoflavonoides
Flavonoides (flavanonas, flavonas, flavonoles43

Estructura del Flavonol Estructura de la Flavona
Introdución y antecedentes:
El término fitoestrógeno clasifica un gran grupo de compuestos derivados de plantas y que son encontrados naturalmente en muchos alimentos. Algunos de los grupos más grandes de fitoestrógenos son las isoflavonas, lignanos y coumestanos. Las isoflavonas son comúnmente encontradas en la soya (muy rica en isoflavones), legumbres, carne, cereales, nueces, frutas, y vegetales. Los lignasnos son comúnmente encontrados en plantas con la linaza registrando las concentraciones más altas.41 Los coumestanos pueden ser encontrados en los frijoles pintos, brotes de alfalfa, y en vegetales.44
Se ha encontrado que los fitoestrógenos tienen propiedades antioxidantes.45 Ya que la actividad antioxidante se encuentra relacionada con la salud y supervivencia de las células, este descubrimiento ha llevado a algunas personas a creer que pueden prevenir y combatir el cáncer en seres humanos.46 Otra de las razones por las cuales se cree que los fitoestrógenos son agentes anticáncer es la baja incidencia de cánceres de próstata y de seno en las naciones asiáticas. En estos países, se consumen más fitoestrógenos de la soya y vegetales que en los países occidentales. Este cosumo, presumiblemente, contribuye a las bajas tasas de padecimiento de estos tipos de cáncer.47
Lea nuestro aviso sobre CAM y métodos de quimioprevención
También se asume que estos compuestos inhiben el cáncer porque tienen una similaridad estructural a las hormonas esteroides como el estrógeno y la testosterona. El estrógeno es un instigador conocido de tipos de cáncer de respuesta hormonal (por ejemplo: seno, útero, endometrio). El parecido de los fitoestrógenos a los estrógenos les permite unirse a receptores moleculares que son para la hormona mencionada, lo que podría resultar en menos cáncer causando señales en las células.48 Los investigadores creen que esta clase de compuestos también puede estar involucrada en la regulación de la apoptosis.45 Mientras que los fitoestrógenos pueden ser buenos agentes en la lucha contra el cáncer, también son estudiados por su posible habilidad para proteger de enfermedades cardiovasculares, osteoporosis, y síntomas menopáusicos.41
Aprenda más sobre apoptosis
Investigación Científica
Mientras que estudios de población antiguos de los años noventa indican que una dieta rica en fitoestrógenos puede reducir los cánceres relacionados con hormonas; estudios recientes han dado resultados conflictivos acerca de la efectividad de los fitoestrógenos contra el cáncer.49
Un estudio demostró que altas dosis de fitoestrógenos de la soya (genisteína) puede reducir el crecimiento de células cancerígenas de ratones in vitro.50 El aceite de linaza, también ha demostrado prevenir tumores relacionados con estrógenos in vitro y en ratones.51 Por otro lado, también se sospecha que los fitoestrógenos causan cáncer y crecimiento fetal inadecuado.47 Algunos países europeos han recomendado el consumo de niveles máximos de soya por día.47 Otros estudios apoyan el uso cauteloso de los fitoestrógenos ya que demostraron acelerar el crecimiento de cáncer de seno in vitro. 49, 52
Actualmente, los investigadores están realizando varias pruebas clínicas diseñadas para investigar el rol potencial de los fitoestrógenos en la prevención y causalidad del cáncer.49 Para información sobre pruebas clínicas que involucren fitoestrógenos que se estén realizando, por favor visite nuestra sección de Ensayos clínicos.
Aprobación de la Administación de alimentos y fármacos de los Estados Unidos
No existe suficiente evidencia para apoyar la efectividad de los fitoestrógenos contra el cáncer y no han sido aprobados por la FDA como tratamiento para el cáncer.22
*Es importante tener en mente que muchos tratamientos para el cáncer, incluyendo la quimioterapia y radiación, trabajan generando radicales libres para poder destruir células cancerígenas. Si un paciente de cáncer toma antioxidantes cuando se encuentra bajo tratamiento de radiación o quimioterapia, es posible que estos compuestos protejan a las células cancerígenas de los radicales libres deseados. Los doctores pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea lo más efectivo posible. 23
Picnogenol
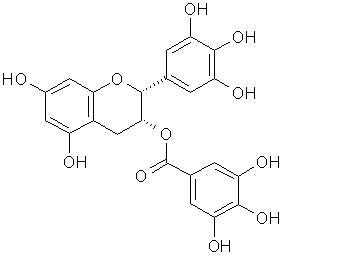
Estructura de Pycnogenol
Clasificado como:
Fitoquímico, polifenol, flavonoide, proantocianidina
Introducción y antecedentes
El Pyncogenol es un producto derivado de la corteza del pino francés (Pinus pinaster). 53 El extracto de la corteza de este árbol contiene compuestos conocidos como flavonoides, procianidinas y procantocianidinas que también son comúnmente encontradas en las uvas y la cocoa. 54, 55 En Europa es muy conocido como un suplemento alimenticio para proteger las células nerviosas, aumentar la actividad del esperma, bajar la presión sanguínea y aliviar síntomas del asma. 53 El Pycnogenol y otras proantocianidinas están siendo investigadas por sus posibles funciones como antioxidante, anti-inflamatoria y antiplaquetario. 54, 56, 55

Pinos franceses
Investigación científica
Se ha demostrado que el Pycnogenol induce a la apoptosis y desacelera la reproducción de leucemia 53, cáncer de mama 57, cáncer de ovarios, 58 en células in vitro. Una mezcla derivada de un árbol relacionado, el Pino corto de Taiwán (Pinus morrisonicola), también ha demostrado matar las células leucémicas in vitro. 59 En otro estudio, el Pycnogenol fue aplicado en piel de ratón antes de ser expuesta a rayos ultravioleta. Los investigadores observaron una disminución en la incidencia del cáncer de piel en los ratones que recibieron la loción con Pycnogenol. 55 Este extracto natural ha sido reconocido como un antioxidante importante por su habilidad para prevenir algunos de los procesos que pueden llevar al cáncer. 60 La mayoría de las investigaciones pertinentes referentes al pycnogeno y a las proantocianidinas involucran su habilidad para prevenir el cáncer.
Aprenda más acerca de la apoptosis
Existe solamente un estudio de la Universidad de Wisconsin para descubrir si el pycnogenol tiene algún beneficio para los sobrevivientes del cáncer de mama con linfedema (fluido en los ganglios linfáticos). 61 Para mayor información de las pruebas realizadas actualmente que involucran pycnogenol, favor de visitar nuestra sección de Encontrar Pruebas Clínicas. Finding Clinical Trials.
Aprobación por la FDA
La FDA es la agencia estadounidense encargada de la salud pública y de acuerdo a ésta no existe evidencia suficiente para afirmar que el pycnogenol es eficiente en contra del cáncer por lo que no ha sido aprobado para ser utilizado en el tratamiento del cáncer. 22
*Es importante tener en mente que muchos tratamientos contra el cáncer, pueden incluir quimioterapia y radiación, que funcionan con radicales libres para destruir las células cancerosas. Si un paciente con cáncer toma antioxidantes durante su tratamiento de radiación o quimioterapia, es posible que estos compuestos puedan proteger las células cancerosas de los radicales libres. Usualmente la recomendación del doctor en pacientes bajo estos tratamientos (quimioterapia o radiación) es que se evite el uso de antioxidantes para que el tratamiento sea lo más eficaz posible. 23
Resveratrol



Clasificado como:
Fitoquímicos, Polifenole, Fitoestrógeno, Antocianina
Estructura del Resveratrol
Introducción y Antecedentes
El resveratrol es un compuesto comúnmente encontrado en la cáscara y las semillas de las uvas rojas. También se puede obtener de bayas, nueces, vino, y suplementos.62, 63 En plantas, este compuesto ayuda a la defensa contra infecciones micóticas.64
El origen del tratamiento para cáncer con resveratrol se originó en 1925 cuando Johanna Brandt, un especialista en dietas de Sudáfrica, declaró que ella se pudo curar a sí misma de su cáncer de estómago ingiriendo una dieta de uvas.65 Ella abrió el Centro de curación y armonía en la ciudad de Nueva York en 1928 pero rápidamente fue acusada de practicar la medicina sin licencia.66, 67 La Sociedad americana del cáncer ha examinado la cura de uvas de Brandt cuatro veces y no encontró un valor terapéutico para su uso.66 Otra fuente del interés hacia resveratrol es la llamada paradoja francesa que indica que los franceses típicamente tienen dietas altas en grasas pero experimentan menos casos de enfermedades cardiovasculares. 68
Por favor lea nuestra nota sobre CAM y métodos quimiopreventivos
Los científicos se encuentran investigando este compuesto debido a su actividad antioxidante 69 y por que podría interferir con la angiogénesis y la metástasis70 mientras que induce la apoptosis62 de células cancerígenas. También se está examinando como una forma posible de prevenir el cáncer , proteger las células endoteliales64, y prevenir enfermedades cardiovasculares.62;El resveratrol no ha demostrado tener efectos secundarios adversos en las pruebas en animales cuando se han usado suplementos70.
Aprenda más sobre angiogénesis, apoptosis y metástasis
Investigación científica
El resveratrol ha demostrado inducir la apoptosis64;en células cancerosas y reducir el crecimiento de células con cáncer62;durante los estudios in vitro. Experimentos involucrando ratones también han indicado que el resveratrol puede inducir la apoptosis en células de cáncer.71;Alternativamente, estudios han mostrado que el resveratrol puede estimular el crecimiento de células de cáncer de seno in vitro.63;Sin embargo, debido a las diferencias en los diseños de los estudios, un número pequeño de pacientes, y un corto tiempo de tratamiento, los doctores no han podido llegar a declaraciones o conclusiones definitivas sobre la habilidad del resveratrol (y moléculas similares) para tratar el cáncer.72;Aunque en experimentos in vitro mostraron que el reveratrol es capaz de mejorar los efectos de crecimiento antitumor del fármaco de quimioterapia rapamicina. Estos experimentos también mostraron una menor incidencia de resistencia del cáncer a la rapamicina, lo cual es una posible consecuencia de las señales AKT73.
Hay un gran número de estudios clínicos siendo conducidos actualmente para determinar el valor del resveratrol como un tratamiento efectivo para el cáncer en UC Irvine, el Instituto Nacional del Cáncer, y la Universidad de Oslo74;Para información sobre pruebas clínicas que se estén llevando a cabo. Para información sobre pruebas clínicas que se están llevando a cabo involucrando al resveratrol, por favor visite nuestra sección sobre Ensayos Clínicos.
Aprobación de la Administración de alimentos y fármacos de Estados Unidos
No existen evidencias suficientes para apoyar al resveratrol como un tratamiento efectivo en la lucha contra el cáncer, y no ha sido aprobado por la FDA como tratamiento para el cáncer22.
*Es importante mantener en mente que muchos tratamientos de cáncer, incluyendo a la quimioterapia y radiación, trabajan generando radicales libres para destruir a las células cancerígenas. Si un paciente con cáncer toma antioxidantes mientras se encuentra en un tratamiento de radiación o quimioterapia, es posible que estos compuestos protejan a las células tumorales de los radicales libres. Los doctores pueden recomendar que los pacientes bajo estos tratamientos eviten los antioxidantes para que el tratamiento sea los más efectivo posible.23
Selenio
A menudo se ingiere como:
Selenometionina
Estructura de la Selenometionina
Introducción y Antecedentes
 El selenio es un componente del aminoácido selenometionina comúnmente encontrado en el suelo, forraje, y granos.75 Es aminoácido natural es esencial para una nutrición apropiada y en una dieta humana normal es ingerido frecuentemente en carnes, mariscos, y plantas.76, 77 La cantidad de selenio en plantas, animales, y humanos dependen de la concentración de selenio en el suelo donde se desarrollaron. Los investigadores comenzaron a ver al selenio como un agente anticáncer cuando un reporte sugirió que un consumo promedio de selenio era menor en naciones que mostraban un riesgo incrementado de padecer cáncer.78
El selenio es un componente del aminoácido selenometionina comúnmente encontrado en el suelo, forraje, y granos.75 Es aminoácido natural es esencial para una nutrición apropiada y en una dieta humana normal es ingerido frecuentemente en carnes, mariscos, y plantas.76, 77 La cantidad de selenio en plantas, animales, y humanos dependen de la concentración de selenio en el suelo donde se desarrollaron. Los investigadores comenzaron a ver al selenio como un agente anticáncer cuando un reporte sugirió que un consumo promedio de selenio era menor en naciones que mostraban un riesgo incrementado de padecer cáncer.78
Lea nuestra nota sobre CAM y métodos quimiopreventivos
En muchos estudios, el selenio está emparejado con la Vitamina E para investigar sus habilidades combinadas para luchar contra el cáncer. En gran parte, la investigación está enfocada en la habilidad del selenio para prevenir el cáncer en vez de luchar contra el. Se desconoce el mecanismo exacto por el cual trabaja pero puede luchar contra el cáncer causando eventos de formas distintas: mejora los procesos que normalmente luchan contra las células cancerosas79 y previene que moléculas dañinas se unan al ADN y lo cambien.80
La FDA sugiere una ingesta diaria de selenio de apróximadamente 70 µg (con un máximo 400µg/día) para adultos como parte de una dieta normal y saludable.81, 77
Investigación científica
El selenio podría ser un agente efectivo para prevenir el cáncer, pero esto todavía no está claro.82, 83 Algunos estudios sugieren que un consumo base o mínimo de selenio provee protección contra el desarrollo del cáncer.84, 77 Estudios también demostraron que los hombres tienen un riesgo reducido de padecer de cáncer de próstata cuando el selenio forma parte de su dieta.81 El tratamiento de células de cáncer de próstata con selenio in vitro puede inhibir el crecimiento del tumor e inhibir la apoptosis.75, 85
Existen algunos indicadores (incluidos en la revisión de Micke, et. al.) de que el selenio puede incrementar el riesgo para una diabetes tipo II.84
Actualmente hay varios ensayos clínicos que se están llevando a cabo, que examinan la habilidad del selenio para prevenir y/o tratar el cáncer. Estudios se están llevando a cabo para observar el impacto del selenio sobre tumores sólidos y linfoma Vea información sobre ensayos clínicos que se están llevando a cabo que involucren al selenio (Instituto Nacional del Cáncer).
Aprobación de la Administración de Alimentos y Fármacos de EE.UU
No existen suficientes evidencias para apoyas la efectividad del selenio para tratar el cáncer y no ha sido aprobado por la FDA como tratamiento contra el cáncer.22
Cannabis and Aceite de Cáñamo

Clasificado como: Fitoquímico, Terpenoide Aromático
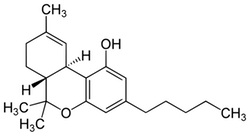
Introducción y Antecedentes
El Cannabis pertenece a la familia de plantas Cannabaceae. ésta incluye la Cannabis sativa (imagen superior; Wikimedia),Cannabis indica, y Cannabis ruderalis.86 LosCannabinoides son químicos encontrados en las plantas Cannabis. los Cannabinoides se unen a proteinas receptoras en células objetivo y producen una variedad de efectos. los Cannabinoides tammbién pueden ser producidos por animales y son clasificados según su origen. Los fitocannabinoides son hechos en planntas, otros cannabinoides, llamados endocannabinoides, son enconntrados naturalmente en humanos y animales, y cannabinoides sintéticos son hechos por el hombre. Muchos cannabinoides que son naturalmente enconttrados en plantas ahora pueden ser producidos sintéticamente. Los dos principales cannabinnoides encontrados en Cannabis son el tetrahidrocannnabinnol (THC), o más específicamente, Δ9-tetrahydrocannabinol (Δ9-THC), mostrado en la imagen superior (Wikimedia), y el cannabidiol (CBD).87, 88
THC es el principal ingrediente psicoactivo. Éste se une a los receptores CB1 y CB2 en el sistema nervioso central y es encontrado en la marihuana (la Cannabis sativa). Se cree que el THC es responsable por la euforia y la sensación de relajación que experimentan los consumidores de marihhuana. 87, 88
Por otro lado, el CBD, tiene baja afinidad por los receptores CB1 y CB2 y mientras que la forma en que actúa es menos comprendida, estudios sugieren que el CBD produce efectos antipsicóticos y ansiolíticos en humanos y reducir los efectos del THC en el cuerpo. 89. Actualmente, estos cannabinoides y otros están siendo estudiados por su uso potencial en el tratamiento de muchos cánceres distintos. Mira más detalles abajo. 90, 91, 92, 93, 94
Aceite de Cáñamo
Aceite de cáñamo es un térmmino común (no científico) para extractos hechos a partir de muchas especies diferentes de Cannabis. El aceite de cáñamo es obtenido cuando las semillas del cáñamo son presionadas. El aceite de cáñamo es legal en los Estados Unidos. Los métodos de fabricación del aceite de cáñamo modernos aseguran que casi ningún THC se encuentra en el aceite de cáñamo. Las semillas utilizadas para el aceite provienen de cepaas de Cannabis sativa cultivadas para producir sólo pequeñas cantidades de THC.95, 96
Investigación Científica
Estudios han demostrado que los cannabinoides tienen una amplia variedad de efectos en las células que crecen en la cultura y en animales. La siguiente lista nno se supone que está completa pero da una visión global de los tipos de efectos que han sido observados. Algunos de los resultadosson contradictorios, con un estudio mostrándose befenicioso pero con otro mostrando ya sea una falta de beneficio o lo que es peor, causando que el cáncer crezca o se propague más agresivamente.
Work in cells grown in dishes in the laboratory (also called cell culture or in vitro)
- Manmade (synthetic) chemicals that activate the same receptors as cannabinoids were shown to inhibit the invasive behavior of lung cancer cells and breast cancer cells.91, 92
- In a system using the major psychoactive cannabinoid found in C. sativa (Δ9-THC), research with different breast cancer cells showed that this chemical was NOT able to kill the cells. The use of this natural product actually enhanced the growth of the cancer cells in animals.93
Trabajo con animales (también llamado in vivo)
- Los químicos sintéticos que se unen a los receptores de cannabinoides mostraron reducir el crecimiento tumoral y la propagación del cáncer dde pulmón en ratones. Los químicos aparentaron causar la muerte celular mediante el bloqueo de la actividad de una proteína de 'supervivencia', AKT.91
- También en ratones, los mismos químicos mostraron reducir el crecimiento y propagación del cáncer de pecho.92
- Un estudio con el químico natural, Δ9-THC, mostró INCREMENTAR el crecimiento tumoral después de su exposición. L ainvestigación indicó que el incremennto del crecimiento tumoral se debía a la supresión del sistema inmune por Δ9-THC.97
Trabajo en humanos
- Ha habido un ensayo en personas con Δ9-THC. El ensayo involucró la inyección del fármaco en el cerebro de 9 pacientes con gioblastoma multimforme, un tipo de cáncer de cerebro. Los resultados del ensayo indicaron que, al menos para algunos pacientes, el fármaco redujo la división de las células cancerígenas in vitro e in vivo pero los pacientes no se recuperaro de su enfermedad.98
Hay indicaciiones de que los resultados contradictorios observados en algunos sistemas se deben a los diferentes efectos causados por las diferentes dosis de los cannabinoides. Esto se cubre con profundidad en una revisión del 2009, "Cannabinoides en el tratamiento del cáncer."90 Muchas revisiones recientes de los cannabinnoides y endocannabinoides en el cáncer también están disponibles. 99, 100
Una investigación publicada en el 2013 muestra que las actividades anti cancerígennas del Δ9-THC son, en gran parte, causadas por sus efectos en una proteína llamada pseudoquinasa homóloga tribble- 3 (TRIB3 por sus siglas en inglés). la TRIB3 es parte de un sistema de respuesta al estrés y cuando está presente en altos noveles, es capaz de bloquear las actividades de las proteínas que mantienen vivas a las células (incluyendo el AKT y mTOR). El Δ9-THC mostró incrementar los niveles de TRIB3 y causar la muerte de células cancerígenas. No era capaz de eliminar las células de TRIB3 faltantes,, mostrando la importancia de ésta proteína en los efectos del Δ9THC.101 Debido a que los mecanismos moleculares de los receptores de cannabinoides aún están siendo descifrados, estudios posteriores en Δ9-THC y otros cannabinnoides en una variedad de cánceres son necesarios.
Ningún estudio ha mostradoo que el Δ9-THC u otros cannabinoides encontrados en la marihuana o el aceite de cáñamo, cure cualquier forma de cáncer.
Tenga en cuenta que los cannabinoides también han sido estudiados por su habilidad para ayudar a reducir los efectos del cáncer y los efectos secundarios de los tratamientos conttra el cáncer. Ésto incluye dolor, náusea y pérdiida de apetito (anorexia). 99, 102, 103, 100, 104
Mira ensayos clínicos involucranddo cannabinoides y cáncer. (abre una nueva ventana)Aprobación de la Administración de Alimentos y Fármacos de los E.E.U.U.
No existe evidencia suficiente para apoyar que los cannabinoides son efectivos en la lucha contra el cáncer y no han sido aprobados por la FDA para el tratamiento contra el cáncer.22
Please be sure to see our notice on complementary therapies. To better understand and evaluate the research described above, read our Introduction to Scientific Research.
Essiac®, Flor-Essence®
Introducción y Antecedentes
Essiac® es una mezcla de cuatro hierbas: raíz de bardana (Arctium lappa), ruibarbo indio (Rheum palmatum), acedera de las ovejas (Rumex acetosella) y la corteza interna del olmo (Ulmus fulva o U. rubra).105 Flor-Essence® contiene las cuatro hierbas mencionadas anteriormente así como trébol rojo (Trifolum pretense), cardo bendito (Carduus benedictus), quelpo (Laminaria digitata), y berro (Nasturt officinale).106 Se cree que los curanderos de la tribu Nativo Americana Ojibwa fueron los creadores de la mezcla de cuatro hierbas encontradas en Essiac.107 El tratamiento se hizo popular a principios de la segunda decada del siglo XX cuando una enfermera canadiense, Rene Caisse, comenzó a tratar a pacientes con esta mezcla de hierbas.108 Ella afirmaba que Essiac® (su apellido escrito al revés) mejoraba la calidad de vida de sus pacientes, prolongaba su supervivencia, y hasta podía curar el cáncer.109 El uso de estos productos por pacientes con cáncer es alimentado en gran parte por evidencia anecdótica (pocos casos raros) de que puede tratar o curar el cáncer.106 Supuestamente, también es un remedio para alergias, hipertensión, y osteoporosis.110
Investigación Científica
Essiac® ha demostrado bloquear radicales libres y ha exhibido la habilidad de poder proteger el ADN de daño que algún día podría llevar al cáncer.110 También, investigadores encontraron que Essiac® peviene el crecimiento de células de cáncer in vitro.107 Otro estudio mostró que Essiac® y Flor-Essence® apenas tenían un pequeño efecto sobre el crecimiento de células de cáncer en la leucemia y en el seno in vitro y sólo a concentraciones muy altas en el cuerpo.108 Este estudio también encontró que la mezcla de hierbas incrementaba la diferenciación de las células de cáncer. De forma alternativa, un estudio más reciente de 2006 encontró que Essiac® y Flor-Essence® no sólo fallan en detener el crecimiento del tumor, pero que pueden estimular el crecimiento de células de cáncer de seno in vitro.106 Un ensayo clínico que involucró a Essiac encontró que no tenía efecto en la calidad de vida de mujeres con cáncer de seno.105
Actualmente no se están realizado pruebas clínicas que investiguen a Essiac® o Flor-Essence® y su habilidad para luchar contra el cáncer.111 Para información sobre pruebas clínicas que se estén llevando a cabo que involucren a Essiac® o Flor-Essence®, por favor visite nuestra sección sobre Ensayos Clínicos.
Aprobación de la Administración de Alimentos y Fármacos de EE.UU.
No hay suficiente evidencia para afirmar que Essiac® y Flor-Essence® son efectivos en la lucha contra el cáncer y no han sido aprobados por la FDA como tratamiento para el cáncer.112, 10
Gerson Therapy
La Terapia Gerson se enfoca en enfermedades crónicas como el cáncer usando "una dieta orgánica y vegetariana, jugos crudos, enemas de café y suplementos naturales," de acuerdo a la página de la compañía. Solo dos clínicas están licenciadas a practicar esta terapia, una en México y otra en Hungría.113
Sin embargo, la FDA no ha aprovado la Terapia Gerson y ningún estudio preclínico (animal o laboratorio) que lo estudie se puede encontrar en la literatura científica. Hay varios estudios clínicos (involucrando humanos) disponibles, casi todos hechos y publicados por el Dr. Gerson, pero no proveen evidencia conclusiva del régimen.114
Para más información, vea El Resumen de Información de Cáncer de La Consulta de Médicos del Instituto Nacional de Cáncer sobre interrogantes de la Terapia Gerson.
Guanabaná (Graviola)

Image obtained from Wikimedia.
Clasificación
Fitoquímicos (químicos de plantas). Cadena larga de ácidos grasos. Acetogeninas Annonaceous.
Introducción/Antecedentes
La Graviola (también conocida como guanábana o guyabano). Algunas veces se la refiere como papaya brasileña o chirimoya - a pesar de que no son lo mismo. Usualmente se refiere a la fruta del árbol tropical Annona muricata. Extractos de la corteza, hojas, raíces y frutos de la Annona muricata son medicinas tradicionales que han sido utilizadas por muchos años para tratar una amplia variedad de dolencias incluyendo infecciones bacterianas, infecciones con el virus del herpes y cáncer. Sin embargo, han habido muy pocos estudios científicos conducidos en humanos que prueban las propiedades médicas de los extractos.115, 116
Las hojas de la graviola contienen derivados de largas cadenas de ácidos grasos conocidos como acetogeninas annonaceous.117, 118, 116, las cuales se cree que ejercen al menos parte de sus efectos biológicos para inhibir la producción de la energía celular transportada (adenosin trifosfato; ATP)119, 120 Debido a que las células cancerosas requieren más ATP que las células normales, las acetogeninas annonaceous se cree que inducen la muerte de células cancerosas quitándoles su suplemento de energía. Los químicos presentes en la graviola hanmbién han mostrado inhibir la producción (replicación) del ADN.121, 122
Investigación Científica
La siguiente lista no se supone que esté completa, pero provee algunos ejemplos relevantes de la investigación del cáncer realizada con extractos de graviola.
En un estudio in vivo, ratones de 6-7 semanas de edad fueron tratados con químicos que podían causar (inhibir) y acelerar (promover) el crecimiento del cáncer de piel. Algunos de los ratones también tenían extractos de Annona muricata colocados en su piel para ver si el extracto podía retrasar o prevenir el crecimiento del cáncer de piel. Se encontró que el extracto de graviola supromía la inhibición tumoral y prevenía la promoción del tumor en las más altas dosis.No se observaron efectos secundarios tóxicos en el ratón (en el estudio corto).123
En los estudios de laboratorio, el extracto de graviola ha demostrado causar función impar y mierte de las líneas de células cancerosas del páncreas (FG/COL0357 y CD18/HPAF). Las células cancerosas fueron expuestas a elevadas cantidades de extracto de graviola. El extracto bloqueó las funciones metabólicas, redujo los niveles de proteínas involucradas en la división celular (ciclina D1),, y causaron un incremento en especies de oxígeno reactivo extracelular (ROS). la baja regulación del metabolismo de las células cancerosas y el incremento en las especies de oxígeno reactivo intracelular lleva a la necrosis (muerte) de algunas de las células cancerosas. En ratones inmunosuprimidos, el tratamiento oral con extracto de graviola mostró reducir el crecimiento y propagación de las células cancerosas pancreáticas inyectadas.124
El extracto de la fruta de la graviola ha demostrado regular la baja del oncogen receptor del factor de crecimiento epidermmial (EGFR) e inhibir el crecimiento de las células cancerosas del pecho en estudios in vitro e in vivo utilizando EGFR sobreexpresado de células cancerosas de pecho humano (MDA-MB-468). Sin embargo, el extracto de graviola no tuvo un efecto en células epiteliales de pecho humano no mutagénicas.125
Debido al estado temprano de la investigación, los estudios científicos no han sido realizados para probar la efectividad del extracto de graviola contra el cáncer en humanos.
Efectos Secundarios
Apesar de que varios estudios sugieren que los extractos de graviola pueden tener propiedades anticancerígenas, el mayor componente bioactivo del extracto, Annonaceous acetogenins, también puede causar problemas mentales y/o del sistema nervioso. El consumo de la fruta ha sido ligado a problemas del sistema nervioso, incluyendo una forma atípica de la enfermedad de Parkinson.126, 127, 128, 129, 130 En un estudio en el cual las ratas fueron suministradas por vía intravenosa con Acetogeninas Annonaceous durante 28 días, una reducción en los niveles de ATP cerebrales y fueron observadas anormalidades silimares a aquellas encontradas en pacientes de Parkinson atípico.131
Varios estudios sugieren que los químicos en la graviola (guanábana) pueden ser tóxicos y deberían ser consumidos con precaución.
Aprobación de la Administración de Alimentos y Fármacos de los E.E.U.U.
No existe evidencia suficiente para apoyar que la graviola (guanábana) sea efectiva en la lucha contra el cáncer. Aún no ha sido aprobada por la FDA para el tratamiento contra el cáncer de cualquier tipo. 22
Asegúrese de leer nuestro aviso sobre terapias complementarias. Para mejor entender y evaluar la investigación descrita arriba, lea nuestra Introducción de Investigaciones Científicas (inglés).
- 1abc Prior RL, Wu X. Anthocyanins: structural characteristics that result in unique metabolic patterns and biological activities. Free Radic Res. (2006) 40(10): 1014-28 [PUBMED]
- 2ab Zafra-Stone S, YAsmin T., Baqchi M., Chatterjee A., Vinson J.A., Bachi D.Berry anthocyanins as novel antioxidants in human health and disease prevention. Molecular Nutrition & Food Research. (2007) 51:6, 675-683 [PUBMED]
- 3 Wu QK, Koponen JM, Mykkanen HM, Torronen AR. Berry phenolic extracts modulate the expression of p21(WAF1) and Bax but not Bcl-2 in HT-29 colon cancer cells. J Agric Food Chem. (2007) 55(4): 1156-63 [PUBMED]
- 4 Valcheva-Kuzmanova S.V., Belcheva A. Colon-available raspberry polyphenols exhibit anti-cancer effects on in vitro models of colon cancer. Journal of Carcinogenesis (2007) Apr 18; 6: 4 [PUBMED]
- 5 Ferguson, P. J.; Kurowska, E.; Freeman, D. J.; Chambers, A. F.; Koropatnick, D. J. A flavonoid fraction from cranberry extract inhibits proliferation of human tumor cell lines. Journal of Nutrition. 2004, 134, 1529-1535. [PUBMED]
- 6 Seeram, N. P.; Adams, L. S.; Hardy, M. L.; Heber, D. Total cranberry extract versus its phytochemical constituents: antiproliferative and synergistic effects against human tumor cell lines. Journal of Agric. Food Chem. 2004, 52, 2512-2517 [PUBMED]
- 7 Anwar S, Fratantonio D, Ferrari D, Saija A, Cimino F, Speciale A. Berry anthocyanins reduce proliferation of human colorectal carcinoma cells by inducing caspase-3 activation and p21 up regulation. Mol Med Rep. 2016 Jun 13. [PUBMED]
- 8 Stopper H, Schmitt E, Kobras K. Genotoxicity of phytoestrogens. Mutat Res. (2005) 574(1-2):139-55 [PUBMED]
- 9 Neuromed IRCCS. Supplementation With Dietary Anthocyanins and Side Effects of Radiotherapy for Breast Cancer (ATHENA). Apr 2015. [https://clinicaltrials.gov/ct2/show/NCT02195960?term=NCT02195960&rank=1]
- 10ab US Food and Drug Adminstration website. Accessed 6/20/2016. [http://www.fda.gov/]
- 11ab Borek C. Dietary antioxidants and human cancer. Integr Cancer Ther (2004). 3: 333-341. [PUBMED]
- 12 Duvoix A. et al. Chemopreventive and therapeutic effects of curcumin. Cancer Letters 223 (2005): 181-190 [PUBMED]
- 13abcd Araujo CAC, Leon LL. Biological activities of Curcuma longa L. Mem Inst Oswaldo Cruz. (2001) 96(5): 723-728 [PUBMED]
- 14 Garcia-Alloza M, Borrelli LA, Rozkalne A, Hyman BT, Bacskai BJ. Curcumin labels amyloid pathology in vivo, disrupts existing plaques, and partially restores distorted neurites in an Alzheimer mouse model. J Neurochem. (2007) Apr 30 [PUBMED]
- 15 Aggarwal S, Ichikawa H, Takada Y, Sandur SK, Shishodia S, Aggarwal BB. Curcumin (diferuloylmethane) down-regulates expression of cell proliferation and antiapoptotic and metastatic gene products through suppression of IkappaBalpha kinase and Akt activation. Mol Pharmacol. (2006) 69(1): 195-206 [PUBMED]
- 16 T. Devasenam K.N. Rajasekaran, G. Gunasekaran, P. Viswwanathan, V.P. Menon, Anti Carcinogenic effect of bis-1,7-(2-hydroxyphenyl)-hepta-1,6-diene-3,5-dione a curcumin analog on DMH-induced colon cancer model. Pharmacol. Res. 27 (2003) 133-140 [PUBMED]
- 17 Lin Y.G., Kunnumakkara A., et al. Curcumin Inhibits Tumor Growth and Angiogenesis in Ovarian Carcinoma by targeting the Nuclear Factor-ºB Pathway. Clin Cancer Res 2007 13: 3423-3430 [PUBMED]
- 18 E. Tourkina, P. Gooz, J.C. Oats, A. Ludwicka-Bradley, R.M. Silver, S. Hoffman, Curcumin-induced apoptosis in scleroderma lung fibroblasts: role of protein kinase cepsilon. American Journal of respiratory Cellular Molecular Biology 31(2004): 28-35 [PUBMED]
- 19ab Mirzaei H, Naseri G, Rezaee R, Mohammadi M, Banikazemi Z, Reza Mirzaei H, Salehi H, Peyvandi M, Pawelek JM, Sahebkar A. Curcumin: A new candidate for melanoma therapy? Int J Cancer. 2016 Jun 9. [PUBMED]
- 20ab Polymeric nanoparticle-encapsulated curcumin (nanocurcumin): a novel strategy for human cancer therapy. Journal of Nanobiotechnology. (2007) 5: 3 [PUBMED]
- 21 Shindikar A, Singh A, Nobre M, Kirolikar S. Curcumin and Resveratrol as Promising Natural Remedies with Nanomedicine Approach for the Effective Treatment of Triple Negative Breast Cancer. J Oncol. 2016;2016:9750785. [PUBMED]
- 22abcdefgh US Food and Drug Adminstration website. Accessed 6/20/2016. [http://www.fda.gov/]
- 23abcde Borek C. Dietary antioxidants and human cancer. Integr Cancer Ther (2004). 3: 333-341. [PUBMED]
- 24abc Cabrera C, Artacho R, Gimenez R. Beneficial effects of green tea--a review. J Am Coll Nutr. (2006) 2: 79-99 [PUBMED]
- 25 Crespy V, Williamson G. A review of the health effects of green tea catechins in in vivo animal models. Journal of Nutrition (2004). 134: 3431-3440. [PUBMED]
- 26 Moyers SB, Kumar NB. Green tea polyphenols and cancer chemoprevention: multiple mechanisms and endpoints for phase II trials. Nutrition Reveiws (2004). 62: 204-211 [PUBMED]
- 27 Yang Cs, Landau JM, Huang MT, Newmark HL. Inhibition of carcinogenesis by dietary polyphenolic compounds. Annual Review of Nutrition (2001). 21: 381-406. [PUBMED]
- 28 Paul B, Hayes CS, Kim A, Athar M, Gilmour SK. Elevated polyamines lead to selective induction of apoptosis and inhibition of tumorigensis by (-)-epigallocatechin-3-gallate (EGCG) in ODC/Ras transgenic mice. Carcinogenesis (2005). 26: 119-124. [PUBMED]
- 29 Jung YD, Kim MS, Shin BA, Chay KO, Ahn BW, Liu W, Bucana CD, Gallick GE, Ellis LM. EGCG, a major component of green tea, inhibits tumour growth by inhibiting VEGF induction in human colon carcinoma cells. British Journal of Cancer. (2001) 84(6):844-50 [PUBMED]
- 30abcd Peter B, Bosze S, Horvath R. Biophysical characteristics of proteins and living cells exposed to the green tea polyphenol epigallocatechin-3-gallate (EGCg): review of recent advances from molecular mechanisms to nanomedicine and clinical trials. Eur Biophys J. 2016 Jun 16. [PUBMED]
- 31 Zhu BH, Zhan WH, Li ZR, Wang Z, He YL, Peng JS, Cai SR, Ma JP, Zhang CH. Epigallocatechin-3-gallate inhibits growth of gastric cancer by reducing VEGF production and angiogenesis. World Journal of Gastroenterology. (2007) 13(8): 1162-9. [PUBMED]
- 32 US Food and Drug Adminstration website. Accessed 6/20/2016. [http://www.fda.gov/]
- 33 Mueller LA, et al, (2005) The tomato sequencing project, the first cornerstone of the international solanaceae project (SOL). In: ENCYCLOPEDIA OF LIFE SCIENCES. John Wiley & Sons, Ltd: Chichester [http://www3.interscience.wiley.com/cgi-bin/fulltext/110473756/PDFSTART]
- 34 Stacewicz-Sapuntzakis M, Bowen PE. Role of lycopene and tomato products in prostate health. Biochim Biophys Acta. (2005) 1740(2): 202-5. Review [PUBMED]
- 35ab Ellinger S, Ellinger J, Stehle P. Tomatoes, tomato products and lycopene in the prevention and reatment of prostate cancer: do we have the evidence from intervention studies? Curr Opin Clin Nutr Metab Care. (2006) 9(6): 722-7. [PUBMED]
- 36 Ramos-Bueno RP, Romero-González R, González-Fernández MJ, Guil-Guerrero JL. Phytochemical composition and in vitro antitumor activities of selected tomato varieties. J Sci Food Agric. 2016 Apr 7. [PUBMED]
- 37 T.W.-M. Boileau, Z. Liao, S. Kim, S. Lemeshow, J.W. Erdman Jr., S.K. Clinton. Prostate carcinogenesis in N-methyl-N-nitrosourea(NMU)-testosterone-treated rats fed tomato powder, lycopene or energy-restricted diets. Journal Natl. Cancer Inst. 95 (2003) 1578 1586 [PUBMED]
- 38 Gann PH, Deaton RJ, Rueter EE, van Breemen RB, Nonn L, Macias V, Han M, Ananthanarayanan V. A Phase II Randomized Trial of Lycopene-Rich Tomato Extract Among Men with High-Grade Prostatic Intraepithelial Neoplasia. Nutr Cancer. 2015;67(7):1104-12. [PUBMED]
- 39 Brown, Powel H. Lycopene in Treating Patients Undergoing Radical Prostatectomy for Prostate Cancer. 2013. University of Texas MD Anderson Phase I/II Prevention Consortium and National Cancer Institute. [NCT00450749]
- 40 National Library of Medicine. (2007). ClinicalTrials.gov Retrieved June 6, 2007 from the National Institutes of Health Web Site: http://www.clinicaltrials.gov/ct/search;jsessionid=77C2E74E90EC0B1C27B8F039E1FA6244?term=lycopene%2C+tomato%2C+cancer&submit=Search
- 41abc Thompson LU, Boucher BA, Liu Z, Cotterchio M, Kreiger N. Phytoestrogen content of foods consumed in Canada, including isoflavones, lignans, and coumestan. Nutr Cancer. (2006) 54(2):184-201 [PUBMED]
- 42 Thompson LU, Boucher BA, Liu Z, Cotterchio M, Kreiger N. Phytoestrogen content of foods consumed in Canada, including isoflavones, lignans, and coumestan. Nutr Cancer. (2006) 54(2):184-201 [PUBMED]
- 43ab Yano S, Umeda D, Yamashita T, Ninomiya Y, Sumida M, Fujimura Y, Yamada K, Tachibana H. Dietary flavones suppresses IgE and Th2 cytokines in OVA-immunized BALB/c mice. Eur J Nutr. (2007) May 11 [PUBMED]
- 44 Horn-Ross PL, Barnes S, Lee M, Coward L, Mandel JE, Koo J, John EM, Smith M. Assessing phytoestrogen exposure in epidemiologic studies: development of a database (United States). Cancer Causes Control. (2000) 11(4):289-98 [PUBMED]
- 45ab Cotterchio M, Boucher BA, Manno M, Gallinger S, Okey A, Harper P. Dietary phytoestrogen intake is associated with reduced colorectal cancer risk. J Nutr. (2006) 136(12): 3046-53. [PUBMED]
- 46 Kurzer MS, Xu X, Dietary Phytoestrogens. Annual Review of Nutrition (1997) 17:359-81 [PUBMED]
- 47abc Sitori CR, Arnold A, Johnson SK. Phytoestrogens: End of Tale? Ann Med. 2005; 37(6): 423-38 [PUBMED]
- 48 Markiewicz L. Garey J, Adlercreutz H, Gurpide E, In Vitro Bioassay of Non-Steroidal Phytoestrogens. Journal of Steroid Biochemistry Molecular Biology (1993) 45(5): 299-405 [PUBMED]
- 49abc Tempfer CB, Bentz EK, Leodolter S, Tscherne G, Reuss F, Cross HS, Huber JC. Phytoestrogens in clinical practice: a review of the literature. Fertil Steril. (2007) 87(6): 1243-9 [PUBMED]
- 50 Chen YC, Nagpal ML, Stocco DM, Lin T. Effects of Genistein, Resveratrol, and Quercetin on Steroidogenesis and Proliferation of MA-10 mouse Leydig Tumor Cells. Journal of Endocrinology. (2007) 192 (3); 527-37 [PUBMED]
- 51 Bergman Jungestrom M, Thompson LU, Dabrosin C. Flaxseed and its lignans inhibit estradiol-induced growth, angiogenesis, and secretion of vascular endothelial growth factor in human breast cancer xenografts in vivo. Clin Cancer Res. (2007) 13(3):1061-7. [PUBMED]
- 52 Rice S. Whitehead SA. Phytoestrogens and Breast Cancer- Promoters or Protectors? Endocrin- Related Cancer. (2006) 13(4): 995-1015 [PUBMED]
- 53abc Huang WW, Yang JS, Lin, CF, HO WJ, Lee MR. Pycnogenol induces differentiation and apoptosis in human promyeloid leukemia HL-60 cells. Leuk Res. (2005) 6: 685-92. [PUBMED]
- 54ab Golanski J, Muchova J, Golanski R, Durackova Z, Markuszewski L, Watala C. Does pycnogenol intensify the efficacy of acetylsalicylic acid in the inhibition of platelet function? In vitro experience. Postepy Hig Med Dosw (Online). (2006) 60: 316-21. [PUBMED]
- 55abc Sime S, Reeve VE. Protection from inflammation, immunosuppression and carcinogenesis induced by UV radiation in mice by topical Pycnogenol. Photochem Photobiol. (2004) 79(2): 193-8 [PUBMED]
- 56 Baliga MS, Katiyar SK. Chemoprevention of photocarcinogenesis by selected dietary botanicals. Photochem Photobiol Sci. 2006 Feb;5(2):243-53. Epub 2005 Aug 12. [PUBMED]
- 57 H.T. Huynh and R.W. Teel. Selective induction of apoptosis in human mammary cancer cells (MCF-7) by Pycnogenol. Anticancer Res (2000) 20: 24172420 [PUBMED]
- 58 BuzZard AR, Lau BHS. Pycnogenol® reduces talc-induced neoplastic transformation in human ovarian cell cultures. Phytother Res. 2007 Jun;21(6):579-86. [PUBMED]
- 59 Hsu TY, Sheu SC, Liaw ET, Wang TC, Lin CC. Anti-oxidant activity and effect of Pinus morrisonicola Hay. on the survival of leukemia cell line U937. Phytomedicine. (2005) 12(9): 663-9 [PUBMED]
- 60 Peng Q, Wei Z, Lau BH. Pycnogenol inhibits tumor necrosis factor-alpha-induced nuclear factor kappa B activation and adhesion molecule expression in human vascular endothelial cells. Cell Mol Life Sci. (2000) 57(5): 834-41. [PUBMED]
- 61 National Library of Medicine. (2007). ClinicalTrials.gov Retrieved June 6, 2007 from the National Institutes of Health Web Site: http://www.clinicaltrials.gov/ct/search;jsessionid=C04DF10415809DE91678716AA35115A4?term=pycnogenol%2C+cancer&submit=Search
- 62abcd Alkhalaf M. Resveratrol-induced growth inhibition in MDA-MB-231 breast cancer cells is associated with mitogen-activated protein kinase signaling and protein translation. Eur J Cancer Prev. (2007)16(4):334-41 [PUBMED]
- 63ab Basly JP, Marre-Fournier F, Le Bail JC, Habrioux G, Chulia J. Estrogenic/antiestrogenic and scavenging properties of (E)- and (Z)-resveratrol. Life Sci. (2000) 66(9): 769-77. [PUBMED]
- 64abc Alkhalaf M. Resveratrol-induced growth inhibition in MDA-MB-231 breast cancer cells is associated with mitogen-activated protein kinase signaling and protein translation. Eur J Cancer Prev. (2007)16(4):334-41 [PUBMED]
- 65 Brandt, Johanna. How to Conquer Cancer, Naturally (The Grape Cure). 2nd edition. Tree of Life Publications, 1996
- 66ab Barrett S. The Grape Cure. (2001). Accessed 2 June 2010 [http://www.quackwatch.org/01QuackeryRelatedTopics/Cancer/grape.html]
- 67 Cease and Desist Orders. Abstracts of Certain Federal Trade Commission Releases. Grape Cure for Cancer. JAMA 116:2525, 1941 File accessed 6/1/2010 [http://jama.ama-assn.org/content/vol116/issue22/index.dtl]
- 68 Opie LH, Lecour S. The red wine hypothesis: from concepts to protective signaling molecules. Eur Heart J. (2007) 7 [PUBMED]
- 69 de Almeida LM, Pineiro CC, et al, "Pritecteive effects of resveratrol on hydrogen peroxide induced toxicity in primary cortical astrocyte cultures." Neurochem Res. (2007) Jun 27. [PUBMED]
- 70ab Delmas D, Lancon A, Colin D, Jannin B, Latruffe N. Resveratrol as a chemopreventative agent: a promising molecule for fighting cancer. Curr Drug Targets. (2006) 7(4): 423-42. [PUBMED]
- 71 Fulda S. and Debatin, KM. Resveratrol modulation of signal transduction in apoptosis and cell survival. Cancer Detection and Prevention (2006) 30:3, 217-223 [PUBMED]
- 72 Von Low E.C, Perabo F.G., Siesner N., Muller S.C. Review. Facts and fiction of phytotherapy for prostate cancer: a critical assessment of preclinical and clinical data. In Vivo. (2007) 21:2, 189-204. [PUBMED]
- 73 "Resveratrol enhances the anti-tumor activity of the mTOR inhibitor rapamycin in multiple breast cancer cell lines mainly by suppressing rapamycin-induced AKT signalling." [http://www.ncbi.nlm.nih.gov/pubmed/21168265]
- 74 National Library of Medicine. National Institutes of Health. Clinicaltrials.gov. Retrieved August 2016.
- 75ab Menter DG, Sabichi AL, Lippman SM. Selenium effects on prostate cell growth. Cancer Epidemiol Biomarkers Prev. (2000) 11: 1171-82 [PUBMED]
- 76 Hu H, Jiang C, Ip C, Rustum YM, Lu J. Methylseleninic acid potentiates apoptosis induced by chemotherapeutic drugs in androgen-independent prostate cancer cells. Clinical Cancer Research (2005). 11: 2379-2388. [PUBMED]
- 77abc USDA. Dietary Reference Intakes: Elements National Academy of Sciences. Institute of Medicine. Food and Nutrition Board. Accessed 2 June 2010. [http://fnic.nal.usda.gov/nal_display/index.php?info_center=4&tax_level=3&tax_subject=256&topic_id=1342&level3_id=5140]
- 78 Rayman MP. Selenium in cancer prevention: a review of the evidence and mechanism of action. Proc Nutr Soc. (2005) 64(4): 527-42 [PUBMED]
- 79 Zhao H, Brooks JD. Selenomethionine induced transcriptional programs in human prostate cancer cells. J Urol. (2007) 177(2): 743-50 [PUBMED]
- 80 Whanger PD. Selenium and its relationship to cancer: an update dagger. British Journal of Nutrition (2004). 91: 11-28. [PUBMED]
- 81ab Duffield-Lillico AJ, Dalkin BL, Reid ME, et al. Selenium supplementation, baseline plasma selenium status and incidence of prostate cancer: an analysis of the complete treatment period of the Nutritional Prevention of Cancer Trial. BJU Int. (2003) 91(7): 608-12. [PUBMED]
- 82 A.J. Duffield-Lillico, B.L. Dalkin, M.E. Reid, B.W. Turnbull, E.H. Slate and E.T. Jacobs et al. Selenium supplementation, baseline plasma selenium status and incidence of prostate cancer: an analysis of the complete treatment period of the Nutritional Prevention of Cancer Trial. British Journal of Urology International. (2003) 91: 608. [PUBMED]
- 83 Clark LC, Dalkin B, Krongrad A et al. Decreased incidence of prostate cancer with selenium supplementation: results of a double-blind cancer prevention trial. British Journal of Urology 1998; 81: 730-734 [PUBMED]
- 84ab Micke O, Schomburg L, Buentzel J, Kisters K, Muecke R. Selenium in oncology: from chemistry to clinics. Molecules. 2009 Oct 12;14(10):3975-88. [PUBMED]
- 85 Zu K, Ip C. Synergy between selenium and vitamin E in apoptosis induction is associated with activation of distinctive initiator caspases in human prostate cancer cells. Cancer Research. (2003) 63(20): 6988-95 [PUBMED]
- 86 Plant profile for Cannabis sativa from the USDA. Accessed 04-10-2013 [http://plants.usda.gov/java/profile?symbol=casa3]
- 87ab Adams IB, Martin BR. Cannabis: pharmacology and toxicology in animals and humans. Addiction. 1996 Nov;91(11):1585-614. [PUBMED]
- 88ab Sharma P, Murthy P, Bharath MM. Chemistry, metabolism, and toxicology of cannabis: clinical implications. Iran J Psychiatry. 2012 Fall;7(4):149-56. [PUBMED]
- 89 Resstel LB, Tavares RF, Lisboa SF, Joca SR, Corrêa FM, Guimarães FS. 5-HT1A receptors are involved in the cannabidiol-induced attenuation of behavioural and cardiovascular responses to acute restraint stress in rats. Br J Pharmacol. 2009 Jan;156(1):181-8. doi: 10.1111/j.1476-5381.2008.00046.x. [PUBMED]
- 90ab Alexander A, Smith PF, Rosengren RJ. Cannabinoids in the treatment of cancer. Cancer Lett. 2009 Nov 18;285(1):6-12. doi: 10.1016/j.canlet.2009.04.005. Epub 2009 May 12. [PUBMED]
- 91abc Preet A, Qamri Z, Nasser MW, Prasad A, Shilo K, Zou X, Groopman JE, Ganju RK. Cannabinoid receptors, CB1 and CB2, as novel targets for inhibition of non-small cell lung cancer growth and metastasis. Cancer Prev Res (Phila). 2011 Jan;4(1):65-75. doi: 10.1158/1940-6207.CAPR-10-0181. Epub 2010 Nov 19. [PUBMED]
- 92abc Qamri Z, Preet A, Nasser MW, Bass CE, Leone G, Barsky SH, Ganju RK. Synthetic cannabinoid receptor agonists inhibit tumor growth and metastasis of breast cancer. Mol Cancer Ther. 2009 Nov;8(11):3117-29. doi: 10.1158/1535-7163.MCT-09-0448. Epub 2009 Nov 3. [PUBMED]
- 93ab McKallip RJ, Nagarkatti M, Nagarkatti PS. Delta-9-tetrahydrocannabinol enhances breast cancer growth and metastasis by suppression of the antitumor immune response. J Immunol. 2005 Mar 15;174(6):3281-9. [PUBMED]
- 94 De Petrocellis L, Ligresti A, Schiano Moriello A, Iappelli M, Verde R, Stott CG, Cristino L, Orlando P, Di Marzo V. Non-THC cannabinoids inhibit prostate carcinoma growth in vitro and in vivo: pro-apoptotic effects and underlying mechanisms. Br J Pharmacol. 2013 Jan;168(1):79-102. doi: 10.1111/j.1476-5381.2012.02027.x. [PUBMED]
- 95 USDA Economic Research Service website page on industrial hemp. http://www.ers.usda.gov/publications/ages/ages001e.aspx#.UWXo-itASmu Published January 2000 Accessed 04-10-2013 [http://www.ers.usda.gov/publications/ages/ages001e.aspx#.UWXo-itASmu]
- 96 Holler JM, Bosy TZ, Dunkley CS, Levine B, Past MR, Jacobs A. Delta9-tetrahydrocannabinol content of commercially available hemp products. J Anal Toxicol. 2008 Jul-Aug;32(6):428-32. [PUBMED]
- 97 McKallip RJ, Nagarkatti M, Nagarkatti PS. Delta-9-tetrahydrocannabinol enhances breast cancer growth and metastasis by suppression of the antitumor immune response. J Immunol. 2005 Mar 15;174(6):3281-9. [PUBMED]
- 98 Guzmán M, Duarte MJ, Blázquez C, Ravina J, Rosa MC, Galve-Roperh I, Sánchez C, Velasco G, González-Feria L. A pilot clinical study of Delta9-tetrahydrocannabinol in patients with recurrent glioblastoma multiforme. Br J Cancer. 2006 Jul 17;95(2):197-203. Epub 2006 Jun 27. [PUBMED]
- 99ab Hermanson DJ, Marnett LJ. Cannabinoids, endocannabinoids, and cancer. Cancer Metastasis Rev. 2011 Dec;30(3-4):599-612. doi: 10.1007/s10555-011-9318-8. [PUBMED]
- 100ab Bowles DW, O'Bryant CL, Camidge DR, Jimeno A. The intersection between cannabis and cancer in the United States. Crit Rev Oncol Hematol. 2012 Jul;83(1):1-10. Epub 2011 Oct 21. [PUBMED]
- 101 Salazar M, Lorente M, García-Taboada E, Hernández-Tiedra S, Davila D, Francis SE, Guzmán M, Kiss-Toth E, Velasco G. The pseudokinase tribbles homologue-3 plays a crucial role in cannabinoid anticancer action. Biochim Biophys Acta. 2013 Apr 5. pii: S1388-1981(13)00085-1 [Epub ahead of print] [PUBMED]
- 102 Todaro B. Cannabinoids in the treatment of chemotherapy-induced nausea and vomiting. J Natl Compr Canc Netw. 2012 Apr;10(4):487-92. [PUBMED]
- 103 Glare P, Miller J, Nikolova T, Tickoo R. Treating nausea and vomiting in palliative care: a review. Clin Interv Aging. 2011;6:243-59. Epub 2011 Sep 12. [PUBMED]
- 104 Carter GT, Flanagan AM, Earleywine M, Abrams DI, Aggarwal SK, Grinspoon L. Cannabis in palliative medicine: improving care and reducing opioid-related morbidity. Am J Hosp Palliat Care. 2011 Aug;28(5):297-303. Epub 2011 Mar 28.
- 105ab Zick SM, Sen A, Feng Y, Green J, Olatunde S, Boon H. Trial of Essiac to ascertain its effect in women with breast cancer (TEA-BC). J Altern Complement Med. (2006) 10: 971-80 [PUBMED]
- 106abc Kulp KS, Montgomery JL, Nelson DO, Cutter B, Latham ER, Shattuck DL, Klotz DM, Bennett LM. Essiac and Flor-Essence herbal tonics stimulate the in vitro growth of human breast cancer cells. Breast Cancer Res Treat. (2006) 98(3): 249-59 [PUBMED]
- 107ab Ottenweller J, Putt K, Blumenthal EJ, Dhawale S, Dhawale SW. Inhibition of prostate cancer-cell proliferation by Essiac. J Altern Complement Med. (2004) 10(4): 687-91. [PUBMED]
- 108ab Tai J, Cheung S, Wong S, Lowe C. In vitro comparison of Essiac and Flor-Essence on human tumor cell lines. Oncol Rep. (2004) 11(2): 471-6 [PUBMED]
- 109 Cassie RM. The Story of Essiac: Her Healing Journey. The Resperin Corporation, Waterloo, Ontaria, Canada. Accessed 6/1/2010. [http://www.resperin.ca/]
- 110ab Leonard SS, Keil D, Mehlman T, Proper S, Shi X, Harris GK. Essiac tea: scavenging of reactive oxygen species and effects on DNA damage. J Ethnopharmacol. (2006) 103(2): 288-96. [PUBMED]
- 111 National Library of Medicine. 2016. ClinicalTrials.gov Retrieved 22 June 2016 from the National Institutes of Health Web Site: http://www.clinicaltrials.gov/ct/search;jsessionid=77C2E74E90EC0B1C27B8F039E1FA6244?term=Essiac%2C+cancer&submit=Search
- 112 PDQ® Integrative, Alternative, and Complementary Therapies Editorial Board. PDQ Essiac/Flor Essence. Bethesda, MD: National Cancer Institute. Updated 20 Aug 2015. Available at: http://www.cancer.gov/about-cancer/treatment/cam/hp/essiac-pdq. Accessed 22 June 2016. [http://www.cancer.gov/about-cancer/treatment/cam/hp/essiac-pdq] [PUBMED]
- 113 Gerson Institute website [http://gerson.org/gerpress/about-us/]
- 114 PDQ® Integrative, Alternative, and Complementary Therapies Editorial Board. PDQ Gerson Therapy. Bethesda, MD: National Cancer Institute. Updated 04-11-2016. Accessed 06-08-2016. [http://www.cancer.gov/about-cancer/treatment/cam/hp/gerson-pdq] [PUBMED]
- 115 Cassileth B. Complementary therapies, herbs, and other OTC agents. Oncology (Williston Park). 2008 Sep;22(10):1202. [PUBMED]
- 116ab L. Taylor. Technical Data Report for Graviola: Annona Muricata. Sage Press, Inc. Herbal Secrets of the Rainforest second ed., 2002. [http://www.rain-tree.com/reports/graviola-techreport.pdf]
- 117 Le Ven J, Schmitz-Afonso I, Lewin G, Laprévote O, Brunelle A, Touboul D, Champy P. Comprehensive characterization of Annonaceous acetogenins within a complex extract by HPLC-ESI-LTQ-Orbitrap® using post-column lithium infusion. J Mass Spectrom. 2012 Nov;47(11):1500-9. [PUBMED]
- 118 Liaw CC, Wu TY, Chang FR, Wu YC. Historic perspectives on Annonaceous acetogenins from the chemical bench to preclinical trials. Planta Med. 2010 Sep;76(13):1390-404. Epub 2010 Jun 24. [PUBMED]
- 119 de Pedro N, Cautain B, Melguizo A, Vicente F, Genilloud O, Peláez F, Tormo JR. Mitochondrial complex I inhibitors, acetogenins, induce HepG2 cell death through the induction of the complete apoptotic mitochondrial pathway. J Bioenerg Biomembr. 2013 Feb;45(1-2):153-64. Epub 2012 Nov 21. [PUBMED]
- 120 Torres MP, Rachagani S, Purohit V, Pandey P, Joshi S, Moore ED, Johansson SL, Singh PK, Ganti AK, Batra SK. Graviola: a novel promising natural-derived drug that inhibits tumorigenicity and metastasis of pancreatic cancer cells in vitro and in vivo through altering cell metabolism. Cancer Lett. 2012 Oct 1;323(1):29-40. [PUBMED]
- 121 López-Lázaro M, Martín-Cordero C, Bermejo A, Cortes D, Ayuso MJ. Cytotoxic compounds from Annonaceus species as DNA topoisomerase I poisons. Anticancer Res. 2001 Sep-Oct;21(5):3493-7. [PUBMED]
- 122 Calderón-Montaño JM, Burgos-Morón E, Orta ML, Pastor N, Austin CA, Mateos S, López-Lázaro M. Alpha, beta-unsaturated lactones 2-furanone and 2-pyrone induce cellular DNA damage, formation of topoisomerase I- and II-DNA complexes and cancer cell death. Toxicol Lett. 2013 Jul 15. pii: S0378-4274(13)01131-4. [Epub ahead of print] [PUBMED]
- 123 Hamizah S, Roslida AH, Fezah O, Tan KL, Tor YS, Tan CI. Chemopreventive potential of Annona muricata L leaves on chemically-induced skin papillomagenesis in mice. Asian Pac J Cancer Prev. 2012;13(6):2533-9. [PUBMED]
- 124 Torres MP, Rachagani S, Purohit V, Pandey P, Joshi S, Moore ED, Johansson SL, Singh PK, Ganti AK, Batra SK. Graviola: a novel promising natural-derived drug that inhibits tumorigenicity and metastasis of pancreatic cancer cells in vitro and in vivo through altering cell metabolism. Cancer Lett. 2012 Oct 1;323(1):29-40. [PUBMED]
- 125 Dai Y, Hogan S, Schmelz EM, Ju YH, Canning C, Zhou K. Selective growth inhibition of human breast cancer cells by graviola fruit extract in vitro and in vivo involving downregulation of EGFR expression. Nutr Cancer. 2011;63(5):795-801. Epub 2011 Jun 22. [PUBMED]
- 126 Caparros-Lefebvre D, Elbaz A. Possible relation of atypical parkinsonism in the French West Indies with consumption of tropical plants: a case-control study. Caribbean Parkinsonism Study Group. Lancet. 1999 Jul 24;354(9175):281-6. [PUBMED]
- 127 Champy P, Melot A, Guérineau Eng V, Gleye C, Fall D, Höglinger GU, Ruberg M, Lannuzel A, Laprévote O, Laurens A, Hocquemiller R. Quantification of acetogenins in Annona muricata linked to atypical parkinsonism in guadeloupe. Mov Disord. 2005 Dec;20(12):1629-33. [PUBMED]
- 128 Lannuzel A, Höglinger GU, Verhaeghe S, Gire L, Belson S, Escobar-Khondiker M, Poullain P, Oertel WH, Hirsch EC, Dubois B, Ruberg M. Atypical parkinsonism in Guadeloupe: a common risk factor for two closely related phenotypes? Brain. 2007 Mar;130(Pt 3):816-27. Epub 2007 Feb 15. [PUBMED]
- 129 Lannuzel A, Höglinger GU, Champy P, Michel PP, Hirsch EC, Ruberg M. Is atypical parkinsonism in the Caribbean caused by the consumption of Annonacae? J Neural Transm Suppl. 2006;(70):153-7. [PUBMED]
- 130 Schapira AH. Complex I: inhibitors, inhibition and neurodegeneration. Exp Neurol. 2010 Aug;224(2):331-5. Epub 2010 Apr 1. [PUBMED]
- 131 Champy P, Höglinger GU, Féger J, Gleye C, Hocquemiller R, Laurens A, Guérineau V, Laprévote O, Medja F, Lombès A, Michel PP, Lannuzel A, Hirsch EC, Ruberg M. Annonacin, a lipophilic inhibitor of mitochondrial complex I, induces nigral and striatal neurodegeneration in rats: possible relevance for atypical parkinsonism in Guadeloupe. J Neurochem. 2004 Jan;88(1):63-9. [PUBMED]