原发性脑癌是指在脑中或在源自大脑的神经中形成的恶性肿瘤。脑癌不经常扩散(转移)到中枢神经系统(Central Nervous System, CNS)之外。1 其中中枢神经系统是包括脑和脊髓的神经系统的一部分2, 3, 4。初级脑癌占所有成人新癌症病例的2%至3%,并且是儿童癌症的第二常见形式(除白血病外)。原发性脑癌是儿童中癌症死亡的主要原因,并且是15至34岁成人中癌症死亡的第三常见原因。5, 6
继发性脑癌是指起源于别处但已扩散(转移)至脑部的恶性肿瘤。实例包括但不限于已转移至脑的乳腺癌和肺癌。继发性脑癌比原发性脑癌更常见。7, 1
在较发达国家的脑癌发病率高于较不发达国家。8拒美国癌症协会估计,2016年在美国约23,770人将被诊断为脑或脊柱癌,而约16,050人将死于脑或脊髓肿瘤。9
大脑解剖和功能
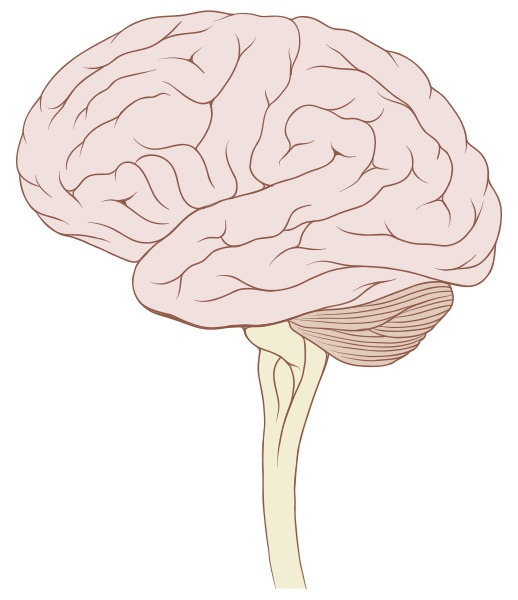
大脑和脊髓构成中枢神经系统(Central Nervous System, CNS)。大脑,一个非常复杂的器官,包含超过万亿的神经元。这些神经元一起工作,使我们能够理解,领会,推理和记忆。 由于大脑的许多区域错综复杂地一起工作以完成某些任务,因此可能难以精准地定位对某一大脑活动负责的特定区域。
脑的3个主要部分是前脑,小脑和脑干。前脑包括大脑和间脑。 大脑分为左半球和右半球,是大脑最前面的部分。间脑包含脑的部分结构,例如负责控制、情感、疼痛、体温和压力丘脑和下丘脑。有关这些部件的更多信息,请参见下面。脑和脊髓由几层结缔组织膜的保护,统称为脑膜。10, 11中枢神经系统还受脑脊液(Cerebrospinal Fluid, CSF)保护,其中脑脊液是一种无色液体,由被称为脑室的四个中空结构分泌。脑脊液有助于吸收头部的冲击,并负责调节和维持中枢神经系统功能所需的最适化学环境。12
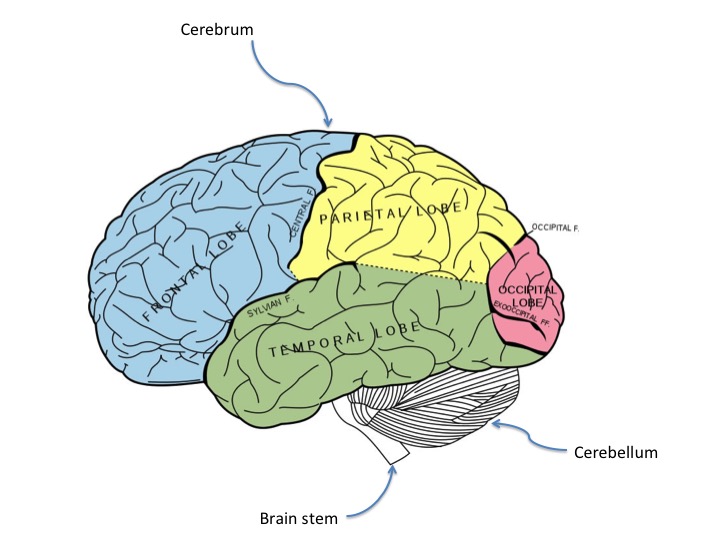
大脑主叶和裂的侧面观察。图片来自盖里的解剖13。
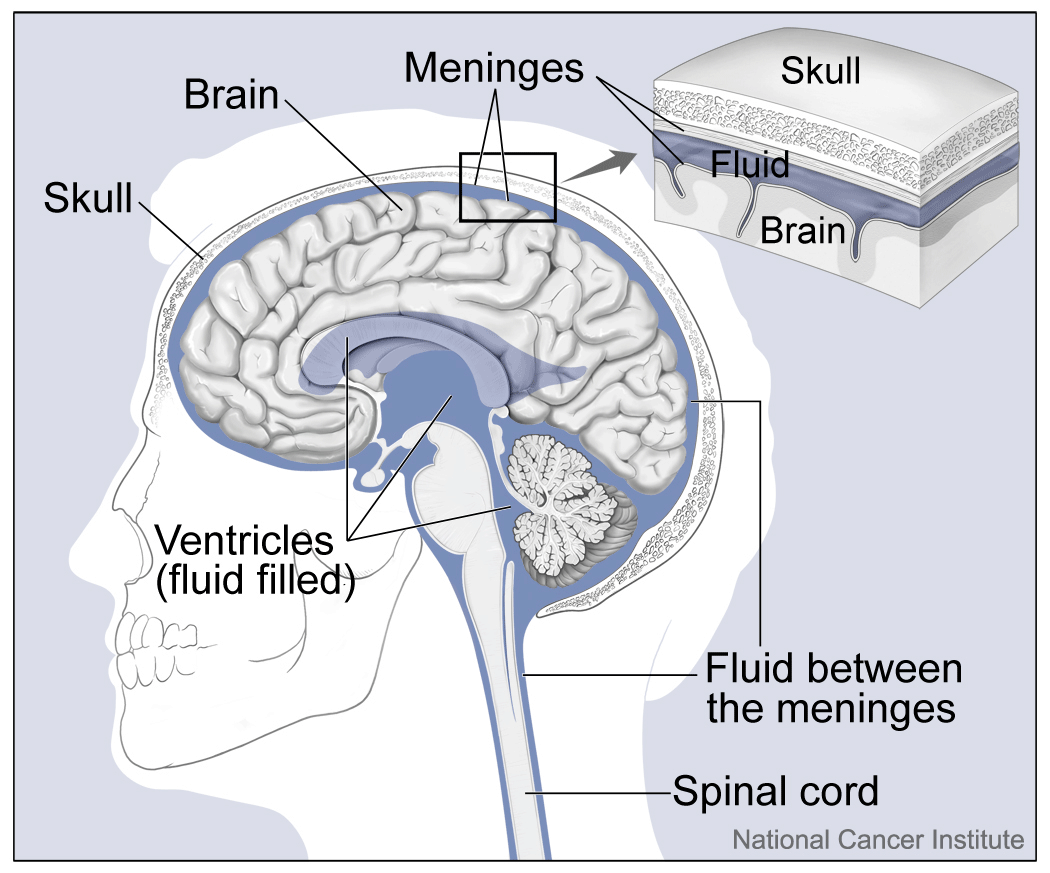
来自国家癌症研究所的颅骨和颈部结构图。14
大脑区域的一些功能:
前脑:前脑由大脑和间脑组成。该区域负责感知,学习,记忆,骨骼肌肉协调,意识,行为调节(例如饮食),控制体温和产生情绪。
小脑:小脑负责运动的协调和姿势平衡的控制。12
脑干:脑干包括中脑,脑桥和延髓。12脑干传递脊髓,前脑和小脑之间的信息,同时它也具有属于自己的几个重要功能。脑干控制运动,呼吸,心脏功能,以及对睡眠或意识的调节。10, 11
大脑的细胞:
与所有其他器官一样,大脑也由许多不同类型的细胞组成。最常见于脑癌的细胞有:
神经细胞(神经元):神经细胞负责将信号从脑传输到脊髓和身体,这些细胞也负责将来自身体的其他部分的信号带回大脑。
神经胶质细胞:神经胶质细胞通过隔离、喂养、提供结构支持来维持神经元细胞。 这些细胞也负责清除死亡神经元。胶质细胞分为几种不同类型,每种都有自己的功能。胶质细胞类型包括星形胶质细胞,少突胶质细胞和室管膜细胞。
种类
有超过100种类型的癌症可以影响中枢神经系统。15正如前面所提到的,在其它位置(乳腺,肺等)发生然后在脑中扩散(转移)的癌症不被认为是脑癌。他们仍然被视为发生于原始位点的癌症。在这里,我们将只讨论原发性脑癌(那些起源于大脑的癌症)。
神经胶质瘤
恶性神经胶质瘤是最常见和最致命的脑癌。它们起源于中枢神经系统的神经胶质细胞。神经胶质瘤可被分为3种主要类型:星形细胞瘤,少突神经胶质瘤和室管膜瘤。16在过去的几年中,神经胶质瘤患者的中位生存时间有所增加,但仍然只有15个月,很少有能够生存2年以上的患者。17研究表明,这种类型的脑癌或许能抵抗治疗,因为它包含负责驱动血管形成(血管生成),肿瘤扩散(转移)和抗治疗的干细胞。18, 19
星形细胞瘤:星形胶质细胞瘤是在星形胶质细胞中形成的肿瘤,并且被发现于大脑和小脑中。 星形细胞瘤约占所有原发性脑肿瘤的50%。多形性胶质母细胞瘤,一种星形细胞瘤亚型,是最具侵袭性的脑肿瘤,与预后不良有关。20。
少突神经胶质瘤:少突神经胶质瘤是在少突胶质细胞中发展的肿瘤,更常见于在大脑半球中发现的少突胶质细胞中。 少突胶质细胞是产生髓磷脂的胶质细胞,其中髓磷脂是可以增加脉冲速度的一种脑组分。21少突神经胶质瘤约占原发性脑肿瘤的4%。大约有55%的少突神经胶质瘤病例出现在40至64岁的人群中。22, 23
室管膜瘤:室管膜瘤是在室管膜细胞中发生的肿瘤。室管膜细胞是脑中的细胞,产生并储存脑脊液。24室管膜瘤占所有原发性脑瘤的2%至3%,但占儿童脑肿瘤的8%至10%。室管膜瘤通常发现于心室内衬,脊髓或小脑附近区域。25
非神经胶质瘤即不是由神经胶质细胞产生的肿瘤。非神经胶质瘤更普遍的实例包括脑膜瘤和成神经管细胞瘤。较不普遍的实例包括髓质垂体腺瘤,原发性CNS淋巴瘤和中枢神经系统生殖细胞瘤。
脑膜瘤:脑膜瘤是在脑膜中发展的肿瘤,膜能够覆盖脑和脊髓。脑膜瘤通常由蛛网膜细胞形成,这些细胞负责脑脊液的吸收。脑膜瘤肿瘤占颅骨肿瘤所有病例的13%至30%。在颅内产生的肿瘤也称为颅内肿瘤。大多数脑膜瘤都是良性的。 恶性脑膜瘤非常罕见,每年每百万人中发病率约为2例。 发生脑膜瘤的风险随年龄增加而增加,并且在妇女中更普遍。26, 27
成神经管细胞瘤:成神经管细胞瘤是儿童中最常见的恶性脑肿瘤。这些癌症发生在后颅窝,一个包含脑干和小脑的颅骨(颅内腔)内部的特定区域。第四脑室区参与约80%的儿童期病例的发展。28, 29
风险
对于大多数类型的脑癌,特定的危险因素尚未确定。但是,一些风险因素(潜在风险因素)已经被描述,它们包括:
1. 年龄:大多数癌症的风险随年龄增加而增加。然而,神经母细胞瘤是一个例外, 它最常发生于于幼儿。
2. 遗传:一些遗传疾病已被确定为脑癌的可能危险因素。它们包括:
a. 1型神经纤维瘤病:以皮肤颜色变化,皮肤、脑和身体其他部位小肿瘤生长为特征的病症。具有这种病症的人有更大的风险发展出神经鞘瘤,脑膜瘤,神经纤维瘤和其他类型的神经胶质瘤。患有这种病症的成人会发生沿着神经生长的癌性肿瘤。30
b. 2型神经纤维瘤病:这是比起1型神经纤维瘤病更不常见的病症。NF2基因中的突变与该疾病相关。大约50%的所有2型神经纤维瘤病病例中,NF2基因突变是遗传自父母。该疾病可能与声学神经瘤,脑膜瘤和脊髓室管膜瘤有关。这种病症的迹象和症状通常出现在青春期或当个体达到其二十几岁(18-24岁)时。一些症状包括平衡功能障碍和听力损失。31
c. 结节性脑硬化:这是一种导致皮肤、脑或神经系统、肾脏和心脏中的肿瘤生长的遗传性遗传紊乱。这种疾病的肿瘤往往是非癌性肿瘤(良性),但也有可能癌变。 大多数结节性脑硬化的病例是由于TSC1和TSC2基因中的随机突变。除了患有该疾病的父母之外,没有已知的该疾病的风险因素。然而在大多数情况下,通常没有结节性硬化的家族史。32
d. Von Hippel-Lindau(VHL)综合征:这种病症与身体不同部位的良性和恶性肿瘤的发展相关。VHL基因是负责该综合征的肿瘤抑制基因。VHL基因的突变会产生不能正确调节细胞存活和细胞增殖的异常VHL蛋白。33
e. Li-Fraumeni综合征:这种罕见疾病关系到更大的风险发展脑胶质瘤和其他类型癌症。研究表明,CHEK2基因和TP53基因与Li-Fraumeni综合征有关。约有一半有Li-Fraumeni综合征的家族在TP53基因中有遗传突变。34
3. 感染:病毒,如反转录病毒、乳多泡病毒和腺病毒已被证明在会导致动物的脑肿瘤,但很少有研究显示病毒感染和人类脑肿瘤之间的联系。然而,病毒仍被视为潜在的危险因素,并且在该领域中仍在进行研究。35
4. 头部损伤和创伤:头部损伤和脑膜瘤之间的可能关系目前正在研究中。研究发现,许多诊断为脑肿瘤的儿童在出生时有头部受伤或头部创伤。35
5. 维生素:研究表明怀孕期间亚硝基化合物的食用和后代中脑肿瘤发展的风险增加之间有潜在的联系。35, 36, 37
症状和检测
脑肿瘤症状取决于肿瘤的大小、位置、类型以及肿瘤肿瘤是否已经侵入身体的其他区域。最常见的症状是头痛,其发生在35%的患者中,并且可伴随恶心、呕吐和多种特定神经功能的问题,称为局灶性神经功能缺陷。头痛可能是一个警告标志,特别是在通常不患头痛的患者中。局部(局灶性)问题取决于肿瘤的位置。 如果头痛变得越来越频繁或严重,医生通知患者也很重要。38
几种医学测试可用于检测或排除脑肿瘤:
神经系统检查:神经系统检查是指对患者进行的一组初步测试,以收集关于他/她的精神状态、感觉系统、神经系统和运动功能的信息。基于神经系统检查结果,医生将决定是否需要额外的测试。39了解更多关于神经系统检查的信息。
脑血管造影术:脑血管造影术是对患者进行的程序,通过病人大脑中的血管可视化血液流动。进行该程序以识别脑中可能的血栓和血管问题,例如动脉瘤、动脉阻塞和血管炎。该程序也可用于确认脑肿瘤的存在。
如何进行
脑血管造影通常在医院或放射中心进行。可以告诉患者在测试前的某个时间段内不要食用固体食物或流食。在该过程中,患者将躺在X射线台上,病人头部通过绑带或胶带等固定。这是为了防止可能扰乱检查的任何可能的移动。在脑血管造影期间将使用心电图(ECG)来监测患者的心脏活动。在手术开始之前,将在患者身体(通常是腹股沟)的区域中施用局部麻醉剂,随后将插入细管导管。导管将进入动脉,并且将小心地向上操作,通过腹部区域到达患者颈部中的动脉。一旦导管处于其预期位置,一种特殊的染料将被注入,然后将采用x射线扫描作为追踪染料在脑动脉和血管中运动的方法。这些X射线扫描将帮助医生识别任何动脉和血管阻塞的位置并且定位患者的大脑中的任何可能的异常血管和动脉结构缺陷。40
CT扫描: 了解更多关于CT扫描的信息。
MRI 扫描: 了解更多关于MRI扫描的信息。
手术活组织检查: 了解更多关于活组织检查的信息。
分期和病理学
如果怀疑某人可能患有脑癌,可以取样组织样品进行检查。在进行手术活检之后,进行手术活检的医生会将样本送至神经病理学家。神经病理学家是专门研究神经系统疾病的病理学家。神经病理学家在宏观(肉眼可见)和微观(需要放大)水平检查样本,并向医生提供病理报告。病理报告包含关于组织外观、细胞组成、疾病状态或正常状态的信息。有关病理报告的更多信息,请参阅 诊断和检测部分。
由神经病理学专家做出的一份准确的病理报告是非常重要的。38
根据美国癌症协会,由于涉及中枢神经系统肿瘤因素的很多,脑癌没有能够准确预测癌症的发展和可能的结果的特定分期系统。 T/N/M 分期系统不是一个合适的工具,因为大多数脑和脊柱癌症不能传播到其他器官(转移)。41然而,世界卫生组织(WHO)已经开发了一个组织学分类系统,关注肿瘤的生物学行为。该系统可基于中枢神经系统肿瘤特征,进而对肿瘤分级(I至IV)来分类。一旦该分级信息与其他可用的临床数据一起被分析,则可以进行预后。I级到II级肿瘤(低级肿瘤)具有一些异常结构,但是大部分这些肿瘤看起来像正常的脑组织。III级肿瘤具有更多的异常特征,比如血管数目增加和细胞密度增大。IV级肿瘤是最恶性的原发性脑肿瘤。IV级肿瘤的癌细胞具有最异常的特征,增多的血管数目、增加的细胞生长和极高的细胞密度。42
肿瘤的生物学
近年来,研究表明癌症干细胞,或更具体地,神经胶质瘤干细胞可能在脑癌发展和肿瘤复发中具有重要作用。CD133是在细胞表面上发现的蛋白质,是通常用于鉴定脑肿瘤干细胞的干细胞标记物。已经在多类脑癌例如多形性成胶质细胞瘤,室管膜瘤,星形细胞瘤,成神经管细胞瘤和其它神经胶质瘤和非神经瘤中发现了脑肿瘤干细胞。由于多种因素,包括抗细胞死亡(抗细胞凋亡)因子的过表达,DNA修复检查点的激活和增加的血管发育(血管生成),脑肿瘤干细胞可能对化疗和/或放疗有抗性。43
有许多与脑癌发展和传播相关的基因,其中一些比另外更普遍。其中的一些基因是:
TP53: 该基因是负责调节细胞分裂和细胞死亡(细胞凋亡)的肿瘤抑制基因。大约有一半的人类肿瘤中在TP53肿瘤抑制基因中发生突变。研究表明约40%的星形细胞瘤具有突变或缺失的TP53基因。35
NF1: 该基因编码产生神经纤维瘤蛋白。神经纤维瘤蛋白通过调节涉及癌症发展的另一种蛋白质Ras的表达而作为肿瘤抑制剂。44
NF2: 该基因编码梅林蛋白,其调节细胞形状,细胞运动和细胞间的通讯。梅林蛋白还在神经系统的细胞中作为肿瘤抑制剂。 研究表明,在大约40%至50%的脑膜瘤或神经鞘瘤患者中,NF2基因缺失或突变。45, 35
Bcl2: 该基因编码抑制细胞死亡的Bcl2蛋白。研究表明,Bcl2蛋白的过表达使得肿瘤对细胞毒性药物的抗性显著增加。46
Myc: 这个基因家族编码Myc转录因子蛋白,其参与肿瘤发生和细胞周期调节。在许多类型的神经胶质瘤中 Myc蛋白过表达,包括成神经管细胞瘤,星形细胞瘤和多形性成胶质细胞瘤。47, 48
EGFR: 该基因编码表皮生长因子受体(EGFR)。49EGFR属于受体酪氨酸激酶(RTK)家族,是结合细胞信号因子例如生长因子和细胞因子的细胞表面受体。通过PI3K-AKT-mTOR和Ras-MAPK两种致癌途径增加的RTK信号与恶性胶质瘤的病例相关。50研究显示约40%的成胶质细胞瘤和间变性星形细胞瘤具有EGFR基因的过量拷贝(基因扩增)和/或EGFR基因的改变(突变)。35, 51
VEGF: 该基因编码血管内皮生长因子(VEGF),是血管形成和血管通透性的关键蛋白质。 其受体,血管内皮生长因子受体(VEGFR),也属于受体酪氨酸激酶(RTK)家族。 研究表明,VEGF通常在脑膜瘤以及恶性神经胶质瘤(例如毛细胞性星形细胞瘤和胶质母细胞瘤)中过表达。52
治疗
脑癌治疗方法的选择取决于肿瘤的位置,肿瘤影响脑和脊髓功能的程度,以及患者的健康史。一些治方案包括化疗、放射治疗、手术、辅助治疗剂和切除。38
由于Cancer Quest的重点是癌症的生物学和可能治疗手段的生物学,我们不提供详细的治疗指导。不过,我们提供创造治疗方案的美国组织的链接。
请在此了解国家综合癌症网络(NCCN)为中枢神经系统(CNS)癌症提供的治疗方案。
有关临床试验的信息:
脑癌的资源
脑癌的风险
脑癌的检测与诊断
脑癌的治疗
脑癌存活率
脑癌幸存者的长期风险
国际资源
部分总结
引言
原发性脑癌是儿童中因癌症死亡的主要原因。
原发性脑癌是15至34岁成人中因癌症死亡的第三大常见原因。
脑癌的种类
原发性脑癌可以分为2种类型:神经胶质瘤和非神经瘤。
恶性神经胶质瘤起源于CNS的神经胶质细胞,并且是更常见和更致命的脑恶性肿瘤形式。 有3种主要类型的神经胶质瘤:星形细胞瘤,少突神经胶质瘤和室管膜瘤。
非神经胶质瘤不起源于中枢神经系统的神经胶质细胞。这些肿瘤在脑的其他部分发展。非神经胶质瘤的一些实例包括脑膜瘤和成神经管细胞瘤。
风险因素
遗传疾病,如1型和2型神经纤维瘤病已被确定为脑癌的可能风险因素。
脑癌风险随年龄增加而增加,除了通常发生在幼儿中成神经细胞瘤。
头部损伤和脑膜瘤之间的可能关系仍在调查中。
怀孕期间N-亚硝基化合物的食用可能与后代中脑肿瘤发生的风险增加有关。
症状和检测
头痛可能是脑肿瘤的警告信号。
几种医学测试可以用于检测或排除脑肿瘤。实例包括:神经病学检查,脑血管造影,CT扫描,MRI扫描和手术活检。
分期和病理
脑癌不具有能够准确预测癌症发展和可能结果的特异性分期系统。 T/ N/M系统不是针对脑癌的适当方法,因为大多数脑和脊柱癌症不能扩散到其他器官(转移)。
脑癌根据世界卫生组织(WHO)的组织学分类系统进行分类,该系统关注肿瘤的生物学行为。
治疗
治疗取决于特定的因素,例如患者的年龄、患者的健康状况、癌症分期、肿瘤的位置等。
治疗手段可以包括手术、放射治疗、化疗、切除术和辅助治疗剂。
- 1ab Lu-Emerson C, Eichler AF. Brain metastases. Continuum (Minneap Minn). 2012 Apr;18(2):295-311. [PUBMED]
- 2 Volavsek M, Lamovec J, Popovic M. Extraneural metastases of anaplastic oligodendroglial tumors. Pathol Res Pract. 2009;205(7):502-7. Epub 2009 May 2. [PUBMED]
- 3 Kural C, Pusat S, Sentürk T, Seçer HI, Izci Y. Extracranial metastases of anaplastic oligodendroglioma. J Clin Neurosci. 2011 Jan;18(1):136-8. [PUBMED]
- 4 Overview of the Nervous System. Nachum Dafny, Ph.D., Department of Neurobiology and Anatomy, The UT Medical School at Houston. Copyright 2012 [http://nba.uth.tmc.edu/neuroscience/s2/chapter01.html]
- 5 American Cancer Society. Cancer Facts & Figures 2015. Atlanta: American Cancer Society; 2015. [http://www.cancer.org/acs/groups/content/@editorial/documents/document/acspc-044552.pdf]
- 6 Ries LAG, Smith MA, Gurney JG, Linet M, Tamra T, Young JL, Bunin GR (eds). Cancer Incidence and Survival among Children and Adolescents: United States SEER Program 1975-1995, National Cancer Institute, SEER Program. NIH Pub. No. 99-4649. Bethesda, MD, 1999. [http://seer.cancer.gov/publications/childhood/]
- 7 Nguyen TD, Abrey LE. Brain metastases: old problem, new strategies. Hematol Oncol Clin North Am. 2007;21(2):369-388. [PUBMED]
- 8 Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin. 2005 Mar-Apr;55(2):74-108. [PUBMED]
- 9 American Cancer Society. Cancer Facts & Figures 2016. Atlanta: American Cancer Society; 2016. [http://www.cancer.org/acs/groups/content/@research/documents/document/acspc-047079.pdf]
- 10ab Human Physiology: The Mechanisms of Body Function. AJ Vander, J Sherman, D Luciano, EP Widmaier, H Raff, H Strang; published by McGraw-Hill, New York (2004).
- 11ab Neuroscience. 2nd edition. Purves D, Augustine GJ, Fitzpatrick D, et al., editors. Sunderland (MA): Sinauer Associates; 2001. [http://www.ncbi.nlm.nih.gov/books/NBK10799/]
- 12abc Brain Components. Medline Plus. [http://www.nlm.nih.gov/medlineplus/ency/anatomyvideos/000016.htm]
- 13 Brain Lobe image. Wikipedia [http://www.cancerquest.org/sites/default/files/assets/image/brain-lobes.png]
- 14 Brain and nearby structures image. Wikipedia [http://www.cancerquest.org/sites/default/files/assets/image/brain-and-nearby-structures.gif]
- 15 Louis DN, Ohgaki H, Wiestler OD, Cavenee WK, Burger PC, Jouvet A, Scheithauer BW, Kleihues P. The 2007 WHO classification of tumours of the central nervous system. Acta Neuropathol. 2007 Aug;114(2):97-109. Epub 2007 Jul 6. [PUBMED]
- 16 Parsons DW, Jones S, Zhang X, Lin JC, Leary RJ, Angenendt P, Mankoo P, Carter H, Siu IM, Gallia GL, Olivi A, McLendon R, Rasheed BA, Keir S, Nikolskaya T, Nikolsky Y, Busam DA, Tekleab H, Diaz LA Jr, Hartigan J, Smith DR, Strausberg RL, Marie SK, Shinjo SM, Yan H, Riggins GJ, Bigner DD, Karchin R, Papadopoulos N, Parmigiani G, Vogelstein B, Velculescu VE, Kinzler KW. An Integrated Genomic Analysis of Human Glioblastoma Multiforme. Science. 2008 Sep 26;321(5897):1807-12. doi: 10.1126/science.1164382. Epub 2008 Sep 4. [PUBMED]
- 17 Van Meir EG, Hadjipanayis CG, Norden AD, Shu HK, Wen PY, Olson JJ. Exciting new advances in neuro-oncology: the avenue to a cure for malignant glioma. CA Cancer J Clin. 2010 May-Jun;60(3):166-93. [PUBMED]
- 18 Huang Z, Cheng L, Guryanova OA, Wu Q, Bao S. Cancer stem cells in glioblastoma--molecular signaling and therapeutic targeting. Protein Cell. 2010 Jul;1(7):638-55. Epub 2010 Jul 29. [PUBMED]
- 19 Frosina G. Frontiers in targeting glioma stem cells. Eur J Cancer. 2011 Mar;47(4):496-507. Epub 2010 Dec 22. [PUBMED]
- 20 Astrocytomas and Glioblastomas. Neurology and Neurosurgery. Johns Hopkins Medicine. [http://www.hopkinsmedicine.org/neurology_neurosurgery/specialty_areas/brain_tumor/center/glioma/types/astrocytoma.html]
- 21 Dugdale, D. C. (2013, April 18). Myelin. [http://www.nlm.nih.gov/medlineplus/ency/article/002261.htm]
- 22 Van den Bent MJ, Reni M, Gatta G, Vecht C. Oligodendroglioma. Crit Rev Oncol Hematol. 2008 Jun;66(3):262-72. Epub 2008 Feb 12. [PUBMED]
- 23 Oligodendroglioma. Neurology and Neurosurgery. Johns Hopkins Medicine. [http://www.hopkinsmedicine.org/neurology_neurosurgery/specialty_areas/brain_tumor/center/glioma/types/oligodendroglioma.html]
- 24 National Brain Tumor Society. Tumor types- ependymomas. [http://braintumor.org/brain-tumor-information/understanding-brain-tumors/tumor-types/#Ependymoma]
- 25 Ependymoma. Neurology and Neurosurgery. Johns Hopkins Medicine. [http://www.hopkinsmedicine.org/neurology_neurosurgery/specialty_areas/brain_tumor/center/glioma/types/ependymoma.html]
- 26 Marta GN, Correa SF, Teixeira MJ. Meningioma: review of the literature with emphasis on the approach to radiotherapy. Expert Rev Anticancer Ther. 2011 Nov;11(11):1749-58. [PUBMED]
- 27 Link M., and Perry, A. Meningioma Tumorigenesis: An Overview of Etiologic Factors. From 'Meningiomas'. Published by Springer London. Joung Lee, Editor (2009) [http://dx.doi.org/10.1007/978-1-84628-784-8_11]
- 28 Schroeder K, Gururangan S. "Molecular variants and mutations in medulloblastoma." Pharmgenomics Pers Med. 2014 Feb 4;7:43-51. eCollection 2014. [PUBMED]
- 29 General Information About Central Nervous System (CNS) Embryonal Tumors. Childhood Central Nervous System Embryonal Tumors Treatment (PDQ®) [http://www.cancer.gov/cancertopics/pdq/treatment/childCNSembryonal/healthprofessional#Section_633]
- 30 Williams VC, Lucas J, Babcock MA, Gutmann DH, Korf B, Maria BL. Neurofibromatosis type 1 revisited. Pediatrics. 2009 Jan;123(1):124-33. doi: 10.1542/peds.2007-3204. [PUBMED]
- 31 Evans GR, Lloyd SK, Ramsden RT. Neurofibromatosis type 2. Adv Otorhinolaryngol. 2011;70:91-8. doi: 10.1159/000322482. Epub 2011 Feb 24. [PUBMED]
- 32 Wu J, Shin J, Xie D, Wang H, Gao J, Zhong XP. Tuberous Sclerosis 1 Promotes Invariant NKT Cell Anergy and Inhibits Invariant NKT Cell-Mediated Antitumor Immunity. J Immunol. 2014 Feb 14. [PUBMED]
- 33 Sharma P, Dhull VS, Bal C, Malhotra A, Kumar R. Von Hippel-Lindau Syndrome: Demonstration of Entire Disease Spectrum with (68)Ga-DOTANOC PET-CT. Korean J Radiol. 2014 Jan;15(1):169-72. doi: 10.3348/kjr.2014.15.1.169. Epub 2014 Jan 8. [PUBMED]
- 34 Malkin D. Li-fraumeni syndrome. Genes Cancer. 2011 Apr;2(4):475-84. doi: 10.1177/1947601911413466. [PUBMED]
- 35abcdef Wrensch M, Minn Y, Chew T, Bondy M, Berger MS. Epidemiology of primary brain tumors: current concepts and review of the literature. Neuro Oncol. 2002 Oct;4(4):278-99. [PUBMED]
- 36 McKean-Cowdin R, Pogoda JM, Lijinsky W, Holly EA, Mueller BA, Preston-Martin S. Maternal prenatal exposure to nitrosatable drugs and childhood brain tumours. Int J Epidemiol. 2003 Apr;32(2):211-7. [PUBMED]
- 37 Huncharek M, Kupelnick B. "A meta-analysis of maternal cured meat consumption during pregnancy and the risk of childhood brain tumors." Neuroepidemiology (2004); 23(1-2):78-84. [PUBMED]
- 38abc Buckner JC, Brown PD, O'Neill BP, Meyer FB, Wetmore CJ, Uhm JH. Central nervous system tumors. Mayo Clin Proc. 2007 Oct;82(10):1271-86. Review. [PUBMED]
- 39 Neurological Exam. American Brain Tumor Association. [http://www.abta.org/brain-tumor-information/diagnosis/neurological-exam.html]
- 40 Cerebral Angiography. MedlinePlus. [http://www.nlm.nih.gov/medlineplus/ency/article/003799.htm]
- 41 "How are brain and spinal cord tumors in adults staged?" American Cancer Society. [http://www.cancer.org/Cancer/BrainCNSTumorsinAdults/DetailedGuide/brain-and-spinal-cord-tumors-in-adults-staging]
- 42 Persano L, Rampazzo E, Basso G, Viola G. "Glioblastoma cancer stem cells: role of the microenvironment and therapeutic targeting." Biochem Pharmacol. 2013 Mar 1;85(5):612-22. doi: 10.1016/j.bcp.2012.10.001. Epub 2012 Oct 11. [PUBMED]
- 43 Cheng JX, Liu BL, Zhang X. "How powerful is CD133 as a cancer stem cell marker in brain tumors?" Cancer Treat Rev. 2009 Aug;35(5):403-8. doi: 10.1016/j.ctrv.2009.03.002. Epub 2009 Apr 14. [PUBMED]
- 44 Friedman JM. Neurofibromatosis 1. GeneReviews [Internet]. [PUBMED]
- 45 Evans DG. Neurofibromatosis 2. GeneReviews [Internet]. [PUBMED]
- 46 Fels C, Schäfer C, Hüppe B, Bahn H, Heidecke V, Kramm CM, Lautenschläger C, Rainov NG. "Bcl-2 expression in higher-grade human glioma: a clinical and experimental study." J Neurooncol. 2000 Jul;48(3):207-16. [PUBMED]
- 47 Faria MH, Khayat AS, Burbano RR, Rabenhorst SH. "c -MYC amplification and expression in astrocytic tumors." Acta Neuropathol. 2008 Jul;116(1):87-95. doi: 10.1007/s00401-008-0368-0. Epub 2008 Mar 28. [PUBMED]
- 48 Swartling FJ. "Myc proteins in brain tumor development and maintenance." Ups J Med Sci. 2012 May;117(2):122-31. doi: 10.3109/03009734.2012.658975. Epub 2012 Feb 21. [PUBMED]
- 49 Lo HW, Hsu SC, Ali-Seyed M, Gunduz M, Xia W, Wei Y, Bartholomeusz G, Shih JY, Hung MC. Nuclear interaction of EGFR and STAT3 in the activation of the iNOS/NO pathway. Cancer Cell. 2005 Jun;7(6):575-89. [PUBMED]
- 50 Huse JT, Holland EC. "Targeting brain cancer: advances in the molecular pathology of malignant glioma and medulloblastoma." Nat Rev Cancer. 2010 May;10(5):319-31. doi: 10.1038/nrc2818. [PUBMED]
- 51 Hatanpaa KJ, Burma S, Zhao D, Habib AA. Epidermal growth factor receptor in glioma: signal transduction, neuropathology, imaging, and radioresistance. Neoplasia. 2010 Sep;12(9):675-84. [PUBMED]
- 52 Stockhammer G, Obwegeser A, Kostron H, Schumacher P, Muigg A, Felber S, Maier H, Slavc I, Gunsilius E, Gastl G. Vascular endothelial growth factor (VEGF) is elevated in brain tumor cysts and correlates with tumor progression. Acta Neuropathol. 2000 Jul;100(1):101-5. [PUBMED]
