
La sangre consta de tres tipos de células y fragmentos celulares que flotan en un líquido que se llama plasma. Estos componentes celulares son:
- Glóbulos rojos ("eritrocitos") - células portadoras de oxígeno
- Glóbulos blancos ("leucocitos") - células que ayudan a formar el sistema inmunológico del cuerpo
- Plaquetas ("trombocitos") - fragmentos de células que desempeñan un papel importante en la formación de coágulos sanguíneos
El número total de glóbulos blancos normalmente varía de 4 a 11 millones de células por mililitro de sangre. 1 Una cucharadita se contiene cinco mililitros. Las leucemias son un grupo de enfermedades caracterizadas por un exceso de glóbulos blancos en la sangre y la médula ósea.2
En el 2021, la sociedad americana de cáncer estimó que se diagnosticarían 61 090 casos nuevos de leucemia y que 23 660 personas morirían a causa de la enfermedad en los Estados Unidos.3
Aprenda acerca de la perspectiva de un sobreviviente de leucemia: entrevista con Tony LaRocco
Visite las siguientes secciones para obtener más información sobre la leucemia:
- Glóbulos blancos
- Tipos de leucemia
- Factores de riesgo
- Síntomas
- Detección y diagnóstico
- Biología tumoral
- Tratamiento
- Fuentes de información
- Resumen de la sección
Glóbulos blancos
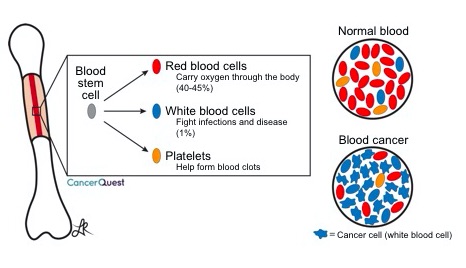
Las células que se encuentran en la sangre comienzan su vida en la parte media (médula) de algunos huesos. La médula ósea es la fuente de todas las células sanguíneas en los adultos. Cuando el cáncer surge de una de estas células, la sangre ya no tiene el equilibrio correcto de tipos de células. Esto puede provocar muchos de los síntomas que se observan con los cánceres de células sanguíneas. A continuación se ofrece información más detallada.
Existen cinco tipos de leucocitos (glóbulos blancos) que se pueden encontrar en la sangre:
- Basófilos
- Eosinófilos
- Linfocitos
- Monocitos
- Neutrófilos
Cada tipo de célula tiene un papel específico que desempeña en el sistema inmunológico de nuestro cuerpo. Las funciones generales importantes del sistema inmunológico incluyen a:
- defensa contra ciertos invasores
- eliminación de células muertas o dañadas
- destrucción de células cancerosas
Aprenda más sobre el sistema inmunológico
La formación de células sanguíneas comienza con una célula especial ubicada en la médula ósea llamada célula madre hematopoyética. A diferencia de la mayoría de las células, la célula madre hematopoyética (y las células madre en general) tiene la capacidad de autorrenovarse y de convertirse en cualquiera de los tipos separados de células sanguíneas. Esto significa que a medida que la célula madre se divide en dos, una sustituye a la célula madre original y la otra comienza el proceso de múltiples pasos para convertirse en una célula sanguínea madura.
Tome en cuenta que las células madre hematopoyéticas son diferentes de las células madre embrionarias. Mientras que las células madre hematopoyéticas pueden convertirse en cualquier tipo de célula sanguínea, las células madre embrionarias pueden convertirse en cualquier tipo de célula en todo el cuerpo.
Los precursores de células sanguíneas generalmente pasan por una serie de etapas en la médula ósea antes de ingresar al torrente sanguíneo circulante. Las señales de las células circundantes en la médula ósea pueden ayudar a estimular la división, el desarrollo y la maduración de las células madre hacia ciertos tipos de células sanguíneas. La división celular normal también está regulada por un proceso importante conocido como el ciclo celular. La interrupción de este proceso es fundamental para el desarrollo de la leucemia.4Aprenda más sobre el ciclo celular.
Tipos
De la misma manera que los árboles genealógicos se dividen en linajes familiares, los cinco tipos de leucocitos (glóbulos blancos) se dividen en dos grupos (linajes), según su forma de desarrollo. Las células mieloides incluyen a los monocitos, neutrófilos, eosinófilos y a los basófilos. Las células linfoides incluyen a los linfocitos B, linfocitos T, y a las células asesinas naturales (Natural Killer cells en inglés o NK). Aprenda más sobre los linfocitos.
Las leucemias se clasifican en 4 categorías principales, según el tipo de glóbulo blanco que se ve afectado (linfoide versus mieloide) y las características de la enfermedad (aguda versus crónica):
- Leucemia linfoblástica aguda
- Leucemia mieloide aguda (leucemia mielógena aguda)
- Leucemia linfoide crónica (leucemia linfocítica crónica)
- Leucemia mieloide crónica (leucemia mielógena crónica)
Por lo general, las leucemias agudas son enfermedades agresivas en las que se produce una transformación cancerígena en las primeras etapas del desarrollo del glóbulo afectado. Si no se tratan, estas enfermedades pueden ser rápidamente fatales.2
Las leucemias crónicas se caracterizan por una progresión más lenta que las leucemias agudas. Estas leucemias son más difíciles de curar, por lo que el enfoque terapéutico suele ser conservador y tiene como objetivo controlar los síntomas.5
Leucemia aguda
Las leucemias agudas son causadas por el daño a las células madre o a las células en las primeras etapas de desarrollo en la médula ósea. Las mutaciones que afectan el control de la división celular, la diferenciación y la muerte celular conducen a la acumulación de precursores de células sanguíneas tempranas conocidas como células blásticas.2
La siguiente animación es un breve resumen de la leucemia aguda:
Leucemia linfoide aguda (LLA)
La leucemia linfoide aguda es la forma más común de leucemia que se diagnostica en niños.6 La incidencia de la leucemia linfoide aguda alcanza su punto máximo entre los 3 y los 7 años, disminuye a los 10 años y vuelve a aumentar después de los 40.7
Leucemia mieloide aguda (LMA)
La leucemia mieloide aguda representa el 10-15% de las leucemias que se diagnostican en la infancia y es el tipo más común de la leucemia aguda en adultos.8
Las leucemias linfoides crónicas son enfermedades caracterizadas por la acumulación de linfocitos maduros B o T en la sangre. Estas enfermedades tienen un vínculo fuerte con los linfomas, produciendo aglomeraciones de linfocitos los ganglios y vasos linfáticos.9
Leucemia linfocítica crónica (LLC)
El tipo más común de la leucemia linfoide crónica involucra a los linfocitos B. La leucemia linfocítica crónica principalmente afecta a aquellas personas que tienen una edad avanzada, con una incidencia máxima entre los 60 y los 80 años.9 Es la forma más común de leucemia en los países occidentales.10 La leucemia linfocítica crónica puede progresar de múltiples maneras, por ende, el tiempo de supervivencia varía de meses a décadas.10
Otros tipos de leucemias linfoides crónicas incluyen:9
- Leucemia prolinfocítica (PLL)
- Tricoleucemia
- Leucemia de células plasmáticas
- Leucemia linfocítica granular grande
- Leucemia prolinfocítica de células T (T-PLL)
Leucemia mieloide crónica (LMC)
La leucemia mieloide crónica es un trastorno de una célula madre hematopoyética. La enfermedad representa aproximadamente el 15% de los casos de leucemia y ocurre con mayor frecuencia entre las edades de 40 y 60 años. Las pruebas de laboratorio revelan que aquellos que sufren de esta condición tienen un mayor número de células pertenecientes a la línea celular mieloide (monocitos, neutrófilos, basófilos, eosinófilos), en diversas etapas de su desarrollo, que circulan en el torrente sanguíneo.5
Factores de riesgo
Aunque se desconoce la causa de la leucemia en la mayoría de los pacientes, varios factores están asociados con un mayor riesgo de desarrollar la enfermedad. Los factores que influyen en el riesgo de desarrollar leucemia incluyen a:
- Edad
- Quimioterapia previa
- Etnia y género
- Síndromes heredados (como el síndrome de Down)
- Radiación ionizante
- Infección con ciertos virus
- Fumar
Los efectos relativos de estos y otros factores de riesgo en cualquier caso de cáncer son variables. Algunos de estos y otros factores de riesgo se analizan a continuación.
Edad
Por lo general, el riesgo de desarrollar cualquier tipo de leucemia aumenta de manera constante con la edad. Sin embargo, los grupos de edad más comunes para el desarrollo de leucemia linfoblástica aguda (LLA) se encuentran entre los 3 y los 7 años y también después de los 40. 11La razón de este pico en la incidencia de esta condición durante la infancia aún no se ha definido.
Encuentre más información sobre la relación entre el cáncer y la edad en nuestra página dedicada a la mutación.
Quimioterapia previa
Leucemia mieloide aguda (LMA) tiene una subcategoría que se conoce como leucemia mieloide aguda secundaria o relacionada con la terapia; esta condición puede desarrollarse tras haber recibido tratamientos previos de quimioterapia. Aunque el nombre implica una relación causal, el mecanismo exacto sigue siendo desconocido. 12 El pronóstico de la leucemia mieloide aguda secundaria suele ser peor en comparación con la leucemia mieloide aguda primaria.8
Etnia/Género
Con la excepción de la leucemia mieloide crónica (LMC), que tiene una incidencia similar entre todos los grupos étnicos, la leucemia ocurre con mayor frecuencia en personas con ascendencia blanca en comparación con los aquellos con ascendencia asiática, hispana y negra. La leucemia también ocurre con más frecuencia en hombres que en mujeres.11
Síndromes hereditarios
Los niños con síndrome de Down (SD) tienen un riesgo 20 veces mayor de desarrollar una leucemia infantil en comparación con los niños sin esta condición.13 Aproximadamente el 10% de los niños con síndrome de Down nacen con una "leucemia transitoria" que se resuelve espontáneamente a los pocos meses del nacimiento. Sin embargo, del uno al dos por ciento de estos casos se convierten en una leucemia aguda maligna que requiere el tratamiento con quimioterapia a los 4 años de edad. 14Aunque se han propuesto varias hipótesis, la razón de este aumento de riesgo sigue siendo incierta.
Otros síndromes hereditarios que incrementan el riesgo de la leucemia son:
- Ataxia-telangiectasia15
- Síndrome de Bloom
- Síndrome de Fanconi16
- Síndrome de Klinefelter17
- Neurofibromatosis
Radiación ionizante
Se ha observado un aumento de leucemia en los supervivientes del bombardeo atómico en algunas ciudades japonesas. Aunque el riesgo asociado con la exposición a niveles más bajos de radiación no está claro, los estudios han demostrado que el riesgo de desarrollar la leucemia puede incrementar con el uso de la radioterapia para la espondilitis anquilosante (una forma de artritis) y de a radiografías de diagnóstico de fetos durante el embarazo.18
Virus
Las infecciones con el virus-1 (HTLV-I) linfotrópico de células T están relacionadas con el desarrollo de la leucemia/linfoma de células T del adulto, un cáncer de linfocitos maduros activados.19 Aprenda más sobre los linfocitos T.
La incidencia tanto del HTLV-I, como de la leucemia de células T del adulto, se ha propagado por algunas regiones del mundo como la cuenca del Caribe, Japón y algunas partes de Sur América y África; es muy raro encontrarlo en otras partes del mundo. 19La mayoría de las personas que se infectan con el HTLV-I no desarrollan leucemia. 20 Los registros del cáncer en Japón indican que el riesgo de desarrollar la leucemia de células T del adulto, es 2,1% para las mujeres infectadas y 6,6% para los hombres infectados.21
Aunque no se conoce el mecanismo exacto por el cual el HTLV-I provoca el cáncer, algunos estudios de laboratorio han identificado mecanismos que están relacionados. 21 Aprenda más acerca de los virus y el cáncer
Síntomas
La leucemia provoca la acumulación de células cancerígenas en la médula ósea y la sangre. La presencia de una gran cantidad de células anormales en la médula ósea puede impedir que la médula produzca células sanguíneas normales y sanas. Los síntomas que causa la insuficiencia de la médula ósea incluyen la palidez, el cansancio, la dificultad para respirar, el sangrado excesivo y una mayor susceptibilidad a las infecciones. Las células cancerígenas también pueden infiltrarse dentro de ciertos órganos, como en los ganglios linfáticos, el bazo y el hígado, provocando hinchazón.22
Sin embargo, muchos pacientes no experimentan ningún síntoma durante las primeras etapas de la enfermedad.
Aprenda más sobre la detección del cáncer.
Mira la entrevista completa con los sobrevivientes: Tony LaRocco y Julio Farach (en Español)
Detección y diagnóstico
El diagnóstico de leucemia se suele dar después de realizar un análisis de sangre que indica un recuento anormal de células sanguíneas.23 Una vez que se sospecha la presencia de la leucemia, el médico puede tomar muestras de la médula ósea y de sangre para examinar la morfología (forma) celular. Las muestras también se envían al laboratorio de patología para identificar qué proteínas están presentes en la superficie de las células anormales y cualquier cambio cromosómico y molecular dentro de las mismas. Esta información es importante para el diagnóstico, el pronóstico y para poder adaptar la terapia para pacientes individuales.18
Aprenda más sobre la detección de cáncer
Biología tumoral
Los cambios genéticos que ocurren en el cáncer incluyen a la mutación de genes reguladores clave y los cambios en los productos proteicos y sus cantidades (expresión genética). A medida que se van acumulando estas modificaciones, las células se vuelven más anormales y el cáncer progresa. Puede encontrar detalles sobre los cambios genéticos asociados con el cáncer en nuestra sección acerca de la Mutación.
Los avances en la investigación de la leucemia en las últimas décadas han aumentado nuestro conocimiento sobre los cambios que ocurren en la enfermedad. Existe una gran variedad de alteraciones, como las mutaciones puntuales, las amplificaciones, inserciones, deleciones y las trisomías, que pueden tener un rol vital en el desarrollo de la leucemia. ¡Hasta la fecha, se ha logrado identificar a más de 300 traslocaciones cromosómicas! Una traslocación es la reorganización de ciertas partes de un cromosoma. La comprensión de los cambios que ocurren y sus efectos sobre la función celular da paso a la clasificación de la leucemia en subgrupos con pronósticos y estrategias de tratamiento distintos.10
A continuación se detalla un ejemplo de una translocación común: el cromosoma Filadelfia. Aprenda más sobre las translocaciones
Cromosoma Filadelfia
Las traslocaciones constan de una ruptura en los cromosomas y el intercambio de estos fragmentos. Una de esas traslocaciones, que se encuentra en más del 95% de las leucemias mieloides crónicas (LMC), así como en algunas leucemias linfoblásticas agudas (LLA), se produce entre los cromosomas 9 y 22: parte del protooncogén abl se extrae del cromosoma 9 y se une al gen bcr en el cromosoma 22. Asimismo, parte del cromosoma 22 se extrae y se traslada al cromosoma 9.24 El intercambio conduce a la creación de una forma abreviada del cromosoma 22, llamado cromosoma Filadelfia (por la ubicación de su descubrimiento).
La proteína ABL normal funciona como una tirosina quinasa. Las tirosina quinasas son enzimas que transfieren grupos fosfato del trifosfato de adenosina hacia otras moléculas. Este tipo de activación de enzimas reguladoras clave resulta en una cascada de eventos que finalmente resulta en la división celular. El gen de fusión BCR-ABL está ubicado en el cromosoma Filadelfia, y codifica la producción de una proteína que realza la actividad de las tirosina quinasas y, por lo tanto, conduce a una mayor estimulación de la división celular, en comparación con la proteína ABL normal.5
Imatnib (Gleevec) es un fármaco diseñado para unirse a la proteína de fusión BCR-ABL. La presencia del fármaco bloquea la unión del trifosfato de adenosina a la proteína, previniendo así que esta funcione como una tirosina quinasa.25 El imatinib (Gleevec) es el punto de referencia para el tratamiento de leucemia mieloide crónica (LMC).10
Tratamiento
Nosotros nos enfocamos en informar acerca de la biología del cáncer y sus tratamientos, por lo tanto, no contamos con información detallada sobre los protocolos de tratamiento. Sin embargo, le proveemos enlaces a organizaciones estadounidenses las cuales que sí producen tales protocolos de tratamiento.
El National Cancer Institute (Instituto nacional del cáncer) reconoce la validez de los siguientes tratamientos en contra la leucemia:
- Quimioterapia
- Inmunoterapia
- Radioterapia
- Trasplante de Células Progenitoras
- Cirugía
- Terapia con Vacuna
Para más información sobre cómo funcionan estos y otros tratamientos contra el cáncer, acuda a nuestra sección dedicada a los tratamientos contra el cáncer.
Vea las entrevistas con los sobrevivientes de leucemia Tony LaRocco y Julio Farach (en Español)
Información sobre ensayos o estudios clínicos:
- Haga clic aquí para información general sobre ensayos o estudios clínicos en CancerQuest
- Haga clic aquí para información sobre ensayos clínicos en el National Cancer Institute
- Haga clic aquí para información sobre ensayos clínicos en el Instituto de Cáncer Winship.
- Haga clic aquí para información sobre ensayos clínicos de Georgia Clinical Trials Online
Fuentes informativas acerca de la leucemia
Factores de riesgo de la leucemia
Factores de riesgo de la leucemia (Mayo Clinic)
Factores de riesgo: Leucemia (página web en inglés)
Factores de riesgo de la leucemia infantil (ACS)
Sociedad americana de cáncer: Leucemia
Detección y diagnóstico de la leucemia
Instituto de cáncer Winship: Diagnóstico de la leucemia y sus etapas Haga una cita
Tratamientos de la leucemia
Tratamiento de la leucemia linfoblástica aguda en adultos
Tratamiento de la leucemia mieloide aguda en adultos
Tratamiento de la leucemia linfocítica crónica
Tratamiento de la leucemia mieloide crónica
Tratamiento de la tricoleucemia
Tratamiento de la leucemia linfoblástica aguda infantil
Tratamiento de la leucemia mieloide agunda inflantil
Supervivencia de la leucemia
Riesgos a largo plazo para los sobrevivientes de la leucemia
Efectos a largo plazo del tratamiento de la leucemia
Fuentes informativas internacionales
Leukemia and Lymphoma Society of Canada
Canadian Cancer Society: Leukemia
Leukaemia Foundation (Australia)
Cancer Council Australia: Leukaemia
Dharamshila Hospital on Leukemia (India)
Resumen
Introducción
- El componente celular de la sangre contiene glóbulos rojos, glóbulos blancos y plaquetas.
- La leucemia se caracteriza por un aumento en la cantidad de glóbulos blancos en la sangre y la médula ósea.
Glóbulos blancos
- Existen cinco tipos de glóbulos blancos o leucocitos.
- Los leucocitos desempeñan un papel importante en el sistema inmunológico
- Todas las células sanguíneas provienen de las células madre hematopoyéticas.
- Las células precursoras de células sanguíneas maduran en la médula ósea antes de ingresar al torrente sanguíneo.
- La interrupción del proceso de maduración celular es fundamental para el desarrollo de la leucemia.
Tipos de leucemia
- La leucemia se clasifica en cuatro categorías distintas según el tipo de célula que afecta:
- Leucemia mieloide aguda o crónica - - Leucemia linfoide aguda o crónica
- Las leucemias agudas son trastornos agresivos y mientras que las leucemias crónicas avanzan lentamente.
Factores de riesgo
- El riesgo de desarrollar cualquier tipo de leucemia aumenta progresivamente con la edad.
- La leucemia mieloide aguda secundaria se puede desarrollar después de un tratamiento previo con quimioterapia.
- En comparación con otros grupos, la leucemia es más frecuente en hombres de raza blanca.
- Los niños con síndrome de Down tienen un riesgo aproximadamente 20 veces mayor de desarrollar la leucemia infantil en comparación con otros niños.
- La exposición a la radiación ionizante aumenta el riesgo de desarrollar la leucemia.
- El virus-1 (HTLV-I) linfotrópico de células han sido vinculado con el desarrollo de la leucemia/linfoma de células T del adulto
Síntomas
- Palidez, cansancio, dificultad para respirar, sangrado excesivo y mayor susceptibilidad a las infecciones.
- Inflamación de los ganglios linfáticos, el bazo y el hígado.
Detección y diagnóstico
- La leucemia se puede diagnosticar con exámenes de sangre y de la médula ósea
Biología del tumor
- Se producen muchos cambios genéticos en el cáncer. Puede encontrar más información en nuestra sección sobre la mutación.
Tratamiento
- Los tratamientos contra la leucemia incluyen a: la quimioterapia, inmunoterapia, radioterapia, los trasplantes de células madre y la cirugía.
- 1 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 365.
- 2abc Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 157.
- 3 American Cancer Society.Cancer Facts & Figures 2023. Atlanta: American Cancer Society. (2023). Recuperado a partir de https://www.cancer.org/research/cancer-facts-statistics/all-cancer-facts-figures/2023-cancer-facts-figures.html
- 4 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 9.
- 5abc Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 174.
- 6 Stanulla M, Cario G, Meissner B, Schrauder A, Moricke A, Riehm H, Schrappe M. "Integrating molecular information into treatment of childhood acute lymphoblastic leukemia - A perspective from the BFM study group." Blood Cells Mol Dis. 2007 Sep-Oct;39(2):160-3. Epub 2007 May 25. [PUBMED]
- 7 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 158.
- 8ab Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 167.
- 9abc Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 188.
- 10abcd Zhou GB, Li G, Chen SJ, Chen Z. "From dissection of disease pathogenesis to elucidation of mechanisms of targeted therapies: leukemia research in the genomic era." Acta Pharmacol Sin. 2007 Sep;28(9):1434-49. [PUBMED]
- 11ab Yamamoto JF, Goodman MT. "Patterns of leukemia incidence in the United States by subtype and demographic characteristics, 1997-2002." Cancer Causes Control. 2007 Dec 7 [Epub ahead of print] [PUBMED]
- 12 Larson RA, "Etiology and management of therapy-related myeloid leukemia." Hematology Am Soc Hematol Educ Program. 2007;2007:453-9. [PUBMED]
- 13 Alderton LE, Spector LG, Blair CK, Roesler M, Olshan AF, Robison LL, Ross JA. "Child and maternal household chemical exposure and the risk of acute leukemia in children with Down's syndrome: a report from the Children's Oncology Group." Am J Epidemiol. 2006 Aug 1;164(3):212-21. Epub 2006 Jun 7. [PUBMED]
- 14 Izraeli S, Rainis L, Hertzberg L, Smooha G, Yehudit B. "Trisomy of chromosome 21 in leukemogenesis." Blood Cells Mol Dis. 2007 Sep-Oct;39(2):156-9. Epub 2007 May 29. [PUBMED]
- 15 Armata HL, Garlick DS, Sluss HK. "The ataxia telangiectasia-mutated target site ser18 is required for p53-mediated tumor suppression." Cancer Res. 2007 Dec 15;67(24):11696-703. [PUBMED]
- 16 Meyer S, Fergusson WD, Whetton AD, Moreira-Leite F, Pepper SD, Miller C, Saunders EK, White DJ, Will AM, Eden T, Ikeda H, Ullmann R, Tuerkmen S, Gerlach A, Klopocki E, Tonnies H. "Amplification and translocation of 3q26 with overexpression of EVII in Fanconi anemia-derived childhood acute myeloid leukemia with biallelic FANCDI/BRCA2 disruption." Genes Chromosomes Cancer. 2007 Apr;46(4):359-72. [PUBMED]
- 17 Swerdlow AJ, Schoemaker MJ, Higgins CD, Wright AF, Jacobs PA. "Cancer incidence and mortality in men with klinefelter syndrome: a cohort study." J Natl Cancer Inst. 2005 Aug 17;97(16):1204-10. [PUBMED]
- 18ab Boon et al. "Principles & Practice of Medicine." (20th edition) Churchill Livingstone, 2006. Pgs 1039-1047.
- 19ab Matutes E. "Adult T-cell leukaemia/lymphoma." J Clin Pathol. 2007 Dec;60(12):1373-7. [PUBMED]
- 20 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 195.
- 21ab Taylor G. "Molecular aspects of HTLV-1 infection and adult T-cell leukaemia/lymphoma." J Clin Pathol. 2007 Dec;60(12):1392-6. [PUBMED]
- 22 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 159.
- 23 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 189.
- 24 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 180.
- 25 Hoffbrand AV, Moss PAH, Pettit JE (ed). "Essential Haematology" 5th Edition. Blackwell Publishing, Oxford: 2006. Pg. 155.
